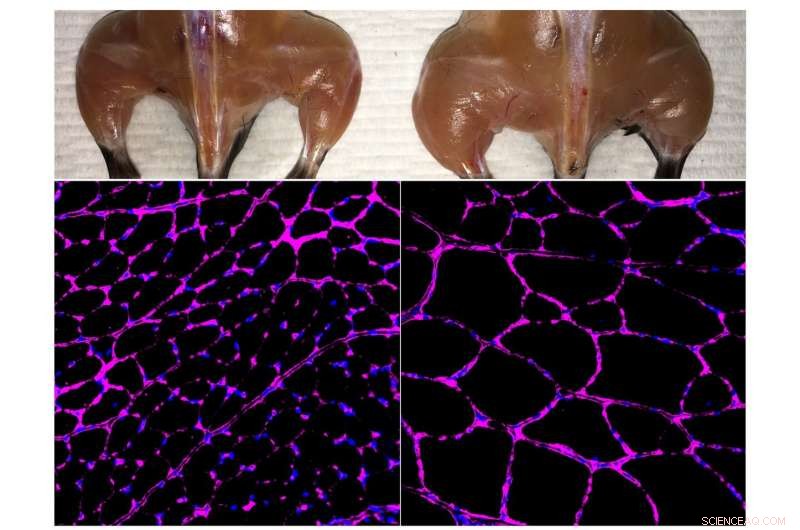
Le système avancé d'activation de gènes épigénétiques in vivo basé sur Cas9 du laboratoire Belmonte améliore la croissance de la masse musculaire squelettique (en haut) et de la taille des fibres (en bas) chez une souris traitée (à droite) par rapport à un contrôle indépendant (à gauche). Les images de microscopie à fluorescence en bas montrent une coloration violette de la glycoprotéine de laminine dans les fibres musculaires antérieures du tibial. Crédit :Institut Salk
Les scientifiques de Salk ont créé une nouvelle version de la technologie d'édition du génome CRISPR/Cas9 qui leur permet d'activer des gènes sans créer de ruptures dans l'ADN, contourner potentiellement un obstacle majeur à l'utilisation des technologies d'édition de gènes pour traiter les maladies humaines.
La plupart des systèmes CRISPR/Cas9 fonctionnent en créant des « cassures double brin » (DSB) dans les régions du génome ciblées pour l'édition ou la suppression, mais de nombreux chercheurs s'opposent à la création de telles ruptures dans l'ADN des humains vivants. Comme preuve de concept, le groupe Salk a utilisé sa nouvelle approche pour traiter plusieurs maladies, dont le diabète, maladie rénale aiguë, et la dystrophie musculaire, dans les modèles de souris.
"Bien que de nombreuses études aient démontré que CRISPR/Cas9 peut être appliqué comme un outil puissant pour la thérapie génique, il y a des inquiétudes croissantes concernant les mutations indésirables générées par les cassures double brin grâce à cette technologie, " dit Juan Carlos Izpisua Belmonte, professeur au laboratoire d'expression génétique de Salk et auteur principal du nouvel article, Publié dans Cellule le 7 décembre 2017. « Nous avons pu contourner ce problème. »
Dans le système CRISPR/Cas9 d'origine, l'enzyme Cas9 est couplée à des ARN guides qui la ciblent au bon endroit dans le génome pour créer des DSB. Récemment, certains chercheurs ont commencé à utiliser une forme "morte" de Cas9 (dCas9), qui peut encore cibler des endroits spécifiques du génome, mais ne coupe plus l'ADN. Au lieu, dCas9 a été couplé à des domaines d'activation transcriptionnelle (commutateurs moléculaires) qui activent les gènes ciblés. Mais la protéine résultante - dCas9 attachée aux commutateurs activateurs - est trop grande et encombrante pour tenir dans le véhicule généralement utilisé pour administrer ce type de thérapies aux cellules d'organismes vivants, à savoir les virus adéno-associés (AAV). L'absence d'un système d'administration efficace rend très difficile l'utilisation de cet outil dans des applications cliniques.
L'équipe d'Izpisua Belmonte a combiné Cas9/dCas9 avec une gamme de commutateurs activateurs différents pour découvrir une combinaison qui fonctionnait même lorsque les protéines n'étaient pas fusionnées les unes aux autres. En d'autres termes, Cas9 ou dCas9 a été emballé dans un AAV, et les commutateurs et les ARN de guidage ont été emballés dans un autre. Ils ont également optimisé les ARN guides pour s'assurer que tous les morceaux se retrouvent à l'endroit souhaité dans le génome, et que le gène ciblé était fortement activé.
"Les composants travaillent tous ensemble dans l'organisme pour influencer les gènes endogènes, " dit Hsin-Kai (Ken) Liao, chercheur au sein du laboratoire Izpisua Belmonte et co-premier auteur du nouvel article. De cette façon, la technologie fonctionne de manière épigénétique, ce qui signifie qu'il influence l'activité des gènes sans changer la séquence d'ADN.
Pour tester la méthode, les chercheurs ont utilisé des modèles murins de lésions rénales aiguës, diabète de type 1 et une forme de dystrophie musculaire. Dans chaque cas, ils ont conçu leur système CRISPR/Cas9 pour stimuler l'expression d'un gène endogène qui pourrait potentiellement inverser les symptômes de la maladie. En cas de maladie rénale, ils ont activé deux gènes connus pour être impliqués dans la fonction rénale, et observé non seulement des niveaux accrus de protéines associées à ces gènes, mais amélioration de la fonction rénale à la suite d'une blessure aiguë. Pour le diabète de type 1, ils visaient à stimuler l'activité des gènes qui pourraient générer des cellules productrices d'insuline. Encore une fois, le traitement a fonctionné, abaisser la glycémie dans un modèle murin de diabète. Pour la dystrophie musculaire, les chercheurs ont exprimé des gènes dont il a déjà été démontré qu'ils inversent les symptômes de la maladie, y compris un gène particulièrement volumineux qui ne peut pas être facilement délivré par les thérapies géniques traditionnelles à médiation virale.
« Nous étions très excités lorsque nous avons vu les résultats chez la souris, " ajoute Fumiyuki Hatanaka, associé de recherche au laboratoire et co-premier auteur de l'article. "Nous pouvons induire l'activation des gènes et en même temps voir des changements physiologiques."
L'équipe d'Izpisua Belmonte travaille maintenant à améliorer la spécificité de leur système et à l'appliquer à plus de types de cellules et d'organes pour traiter un plus large éventail de maladies humaines, ainsi que pour rajeunir des organes spécifiques et inverser le processus de vieillissement et les conditions liées à l'âge telles que la perte auditive et la dégénérescence maculaire. Davantage de tests de sécurité seront nécessaires avant les essais humains, ils disent.