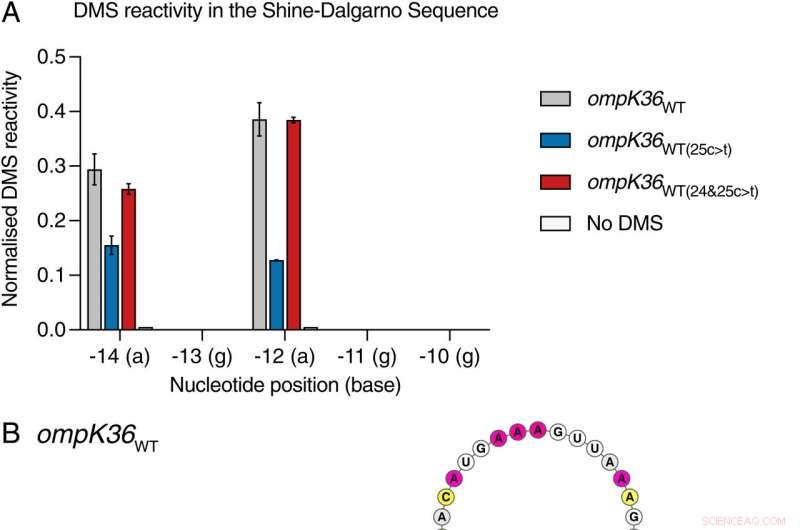
Position 25 dans l'ompK36WT(25c> t) L'ARN induit une tige impliquant le SDS. (A) Signal DMS normalisé côte à côte par nucléotide dans le SDS à partir de pleine longueur in vitro–transcrit et replié ompK36WT , ompK36WT(25c> t) , ompk36WT(24&25c> t) , et ompK36WT non traité par DMS . Des valeurs plus élevées correspondent à une accessibilité accrue de la base. Le signal DMS (± SD) de 2 répétitions biologiques pour les nucléotides -14a à -10g est affiché. (B–D). Modèles de structure sous contraintes DMS de l'extrémité 5′ de ompK36WT (B), ompK36WT(24&25c> t) (C) et ompK36WT(25c> t) (RÉ). Les nucléotides sont colorés par le signal DMS normalisé. Les SDS dans les structures d'ARN sont surlignés en gris. Les flèches indiquent la position −14 et la position 25c> t dans ompK36WT(25c> t) . Crédit :Actes de l'Académie nationale des sciences (2022). DOI :10.1073/pnas.2203593119
Des chercheurs ont découvert une nouvelle façon dont les infections nosocomiales résistent aux antibiotiques, grâce à une mutation génétique "silencieuse".
Les bactéries peuvent acquérir une résistance aux antibiotiques par le biais de mutations aléatoires dans leur ADN qui leur confèrent un avantage qui les aide à survivre. Trouver des mutations génétiques et découvrir comment elles aident les bactéries à survivre à une attaque antibiotique est essentiel pour nous aider à riposter avec de nouveaux médicaments.
Les chercheurs viennent de découvrir une mutation "silencieuse" du code génétique qui conduit à la résistance aux antibiotiques. En règle générale, les mutations de ce type seraient ignorées et pourraient déjà être présentes dans d'autres bactéries infectieuses.
L'équipe, dirigée par des chercheurs de l'Imperial College de Londres et comprenant des collaborateurs internationaux, a publié ses résultats aujourd'hui dans la revue Proceedings of the National Academy of Sciences .
Résistance croissante
Les chercheurs se sont penchés sur la bactérie Klebsiella pneumoniae, qui provoque des infections dans les poumons, le sang et les plaies des personnes hospitalisées, les patients dont le système immunitaire est affaibli, comme ceux des unités de soins intensifs, étant particulièrement vulnérables.
Comme de nombreuses bactéries, K. pneumoniae devient de plus en plus résistante aux antibiotiques, en particulier à une famille de médicaments appelés carbapénèmes. Ces médicaments importants de dernier recours sont utilisés dans les hôpitaux lorsque d'autres antibiotiques ont déjà échoué.
Étant donné que la résistance croissante aux carbapénèmes pourrait affecter considérablement notre capacité à traiter les infections, K. pneumoniae résistant aux carbapénèmes est classé comme organisme "critique" de priorité 1 de l'Organisation mondiale de la santé.
Pour être efficaces, les antibiotiques doivent pénétrer à l'intérieur des bactéries, et chez K. pneumoniae, cela se produit via un canal dans la membrane externe de la bactérie, formé par une protéine appelée OmpK36. L'équipe a découvert une mutation génétique qui fait que la bactérie produit moins de protéine, fermant efficacement certains de ces canaux et empêchant les antibiotiques carbapénèmes d'entrer.
Mutations "silencieuses"
Cette mutation, cependant, fonctionne différemment des mutations standard qui entraînent une résistance aux antibiotiques. Habituellement, les mutations modifient le code génétique de sorte que lorsqu'il est "lu" par les ribosomes et converti en protéine, il produit une chaîne différente d'acides aminés avec des fonctions différentes.
Cette mutation produit toujours la même chaîne d'acides aminés, mais modifie la structure d'un intermédiaire d'ARNm important, empêchant les ribosomes de lire le code et de produire des protéines à partir de celui-ci.
Lors de la recherche de mutations, les techniques génomiques recherchent généralement des modifications de la séquence d'acides aminés. Cependant, puisque cette mutation modifie une structure, plutôt que la séquence elle-même, elle pourrait être considérée comme une mutation "silencieuse".
Le premier auteur, le Dr Joshua Wong, du Département des sciences de la vie de l'Impérial, a déclaré :« À l'ère des mégadonnées et de la génomique, les mutations telles que celles que nous avons découvertes peuvent être considérées comme « silencieuses », car le code génétique aboutit à la même séquence protéique. .
"Cette découverte devrait changer notre façon de voir le code génétique des bactéries et indique potentiellement que nous, dans la communauté scientifique, avons négligé d'autres mutations similaires qui peuvent avoir des effets importants. Notre travail se concentre sur une seule mutation mais change fondamentalement la façon dont nous interprétons les mutations, en particulier celles que l'on croyait silencieux."
Motivé par l'utilisation d'antibiotiques
L'équipe d'Imperial, qui a caractérisé la mutation, a travaillé avec des équipes de l'Université d'Oxford, de l'Université de Florence et de l'Université de Harvard pour identifier la distribution de la mutation dans le monde, évaluer les niveaux de résistance et déterminer comment la mutation a affecté l'ARNm intermédiaire. structure.
En utilisant des données provenant d'échantillons de bactéries résistantes collectés dans le monde, l'équipe a montré que la mutation s'était produite plusieurs fois de manière indépendante. Cela suggère que ce n'est pas aléatoire, mais plutôt motivé par le besoin de la bactérie de se défendre contre les antibiotiques.
Le chercheur principal, le professeur Gad Frankel, du département des sciences de la vie de l'Imperial, a déclaré :« La mutation a évolué à plusieurs reprises indépendamment, et cela nous indique que ce nouveau mécanisme n'est pas un coup de chance ponctuel, mais plutôt motivé par la consommation d'antibiotiques. suggère que la mutation se produit sous la pression des antibiotiques et met en évidence les effets secondaires d'une utilisation excessive d'antibiotiques dans les hôpitaux et autres environnements."
L'équipe espère maintenant que leur découverte sera intégrée dans des outils bioinformatiques qui analysent les séquences génétiques pour identifier la présence de la mutation, comme cela a été fait avec un mécanisme antérieur découvert par l'équipe.
Ils continueront également à travailler avec leurs collaborateurs pour rechercher d'autres mutations importantes dans ce pathogène clé. La superbactérie commune résistante aux médicaments développe une résistance rapide aux antibiotiques de "dernier recours"