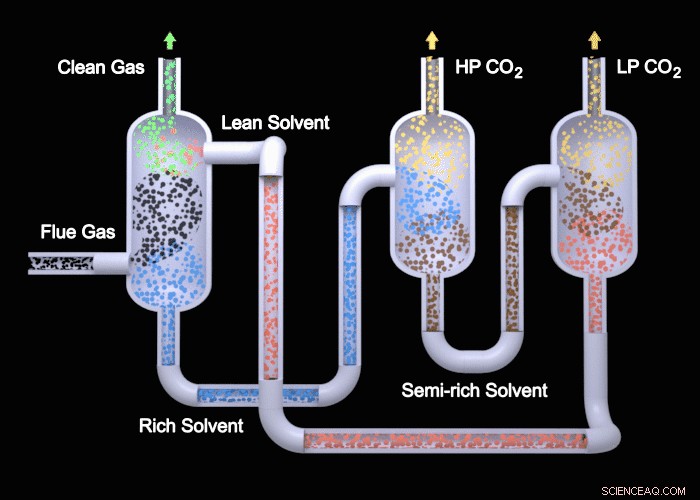
Cette animation illustre la configuration du flash à deux étages, l'un des nombreux processus décrits dans une nouvelle étude détaillant comment l'EEPA, un solvant développé par le Pacific Northwest National Laboratory, peut capter le carbone des fumées émises par les centrales électriques. De gauche à droite, EEPA (rouge) interagit d'abord avec les fumées (noir), où il absorbe le dioxyde de carbone. Puis, comme solvant saturé (bleu), L'EEPA est débarrassé du dioxyde de carbone dans des réservoirs à haute et basse pression. Finalement, le solvant extrait est réintroduit dans l'absorbeur de dioxyde de carbone, où le processus recommence. Crédit :Michael Perkins | Laboratoire national du nord-ouest du Pacifique
Dans le cadre d'un effort de recherche marathon pour réduire le coût de la capture du carbone, les chimistes ont maintenant démontré une méthode pour saisir le dioxyde de carbone (CO
Dans une étude publiée dans l'édition de mars 2021 de Journal international de contrôle des gaz à effet de serre , des chercheurs du Pacific Northwest National Laboratory du département de l'Énergie des États-Unis, ainsi que des collaborateurs de Fluor Corp. et de l'Electric Power Research Institute, décrivent les propriétés du solvant, connu sous le nom d'EEPA, qui lui permettent de contourner les demandes énergétiquement coûteuses induites par les solvants traditionnels.
« L'EMEPA a des qualités prometteuses, " a déclaré l'ingénieur chimiste Yuan Jiang, auteur principal de l'étude. "Il peut capturer le dioxyde de carbone sans teneur élevée en eau, donc c'est pauvre en eau, et il est beaucoup moins visqueux que les autres solvants pauvres en eau."
Les méthodes de captage du carbone sont diverses. Ils vont des amines aqueuses - les solvants riches en eau qui traversent les unités de capture disponibles dans le commerce d'aujourd'hui, que Jiang a utilisé comme comparaison industrielle - aux membranes écoénergétiques qui filtrent le CO
CO atmosphérique actuel
À un coût de 400 à 500 millions de dollars par unité, la technologie commerciale peut capturer le carbone à environ 58,30 $ par tonne métrique de CO
L'étude de Jiang a décrit sept processus que les centrales électriques peuvent adopter lors de l'utilisation de l'EEPA, allant de configurations simples similaires à celles décrites dans la technologie des années 1930, à des configurations à plusieurs étages de plus grande complexité. Jiang a modélisé les coûts énergétiques et matériels pour exécuter de tels processus dans une centrale électrique au charbon de 550 mégawatts, constatant que chaque méthode fusionne près de la barre des 47,10 $ par tonne métrique.
Résoudre les problèmes d'un solvant
L'un des premiers brevets connus pour la technologie de capture du carbone à base de solvants a surgi en 1930, déposé par Robert Bottoms.
"Je ne plaisante pas, " a déclaré le chimiste vert David Heldebrant, co-auteur de la nouvelle étude. « Il y a quatre-vingt-onze ans, Bottoms a utilisé presque la même conception de processus et la même chimie pour résoudre ce que nous connaissons maintenant comme un problème du 21e siècle. »
Le procédé chimique d'extraction du CO
"Nous voulions le frapper de l'autre côté et demander, pourquoi n'utilisons-nous pas la chimie du 21e siècle pour cela ?", a déclaré Heldebrant. en 2009, lui et ses collègues ont commencé à concevoir des solvants pauvres en eau comme alternative. Les premiers solvants étaient trop visqueux pour être utilisables.
"'Voir, '", a-t-il rappelé aux partenaires de l'industrie en disant :« « votre solvant gèle et se transforme en verre. Nous ne pouvons pas travailler avec ça. » Donc, nous l'avons dit, D'ACCORD. Défi accepté."
Au cours de la prochaine décennie, l'équipe du PNNL a affiné la chimie du solvant dans le but explicite de surmonter la « barrière de viscosité ». La clé, il s'est avéré, était d'utiliser des molécules qui s'alignaient de manière à favoriser la liaison hydrogène interne, laissant moins d'atomes d'hydrogène pour interagir avec les molécules voisines.
Heldebrant fait une comparaison avec des enfants qui courent dans une piscine à balles :si deux enfants se tiennent la main en passant, ils se déplacent lentement. Mais s'ils tiennent leurs propres mains à la place, ils passent pour deux plus petits, objets se déplaçant plus rapidement. La liaison hydrogène interne laisse également moins d'atomes d'hydrogène avec lesquels interagir globalement, s'apparente à retirer les balles de la fosse.
Pivoter vers le plastique
Là où le solvant de l'équipe était autrefois visqueux comme du miel, il coulait maintenant comme de l'eau de la bouilloire. L'EEPA est 99 pour cent moins visqueux que les précédentes formulations pauvres en eau du PNNL, maintenant presque à égalité avec les solvants commerciaux, leur permettant d'être utilisés dans l'infrastructure existante, qui est en grande partie construit en acier. Pivotant vers le plastique à la place de l'acier, l'équipe a trouvé, peut encore réduire les coûts d'équipement.
L'acier est cher à produire, coûteux à expédier et a tendance à se corroder avec le temps au contact des solvants. A un dixième du poids, remplacer le plastique par l'acier peut faire baisser le coût global de 5 $ supplémentaires par tonne métrique, selon une étude menée par Jiang en 2019.
L'association avec du plastique offre un autre avantage à l'EEPA, dont la surface réactive est augmentée dans les systèmes plastiques. Parce que les amines aqueuses traditionnelles ne peuvent pas non plus "mouiller" le plastique (pensez à l'eau perlant sur du téflon), cet avantage est propre au nouveau solvant.
L'équipe du PNNL prévoit d'en produire 4, 000 gallons d'EEPA en 2022 à analyser à une échelle de 0,5 mégawatt à l'intérieur des installations d'essai du National Carbon Capture Center dans le comté de Shelby, Alabama, dans un projet mené par l'Electric Power Research Institute en partenariat avec Research Triangle Institute International. Ils continueront les tests à des échelles croissantes et affineront davantage la chimie du solvant, dans le but d'atteindre l'objectif du département américain de l'Énergie de déployer une technologie disponible dans le commerce qui peut capturer le CO