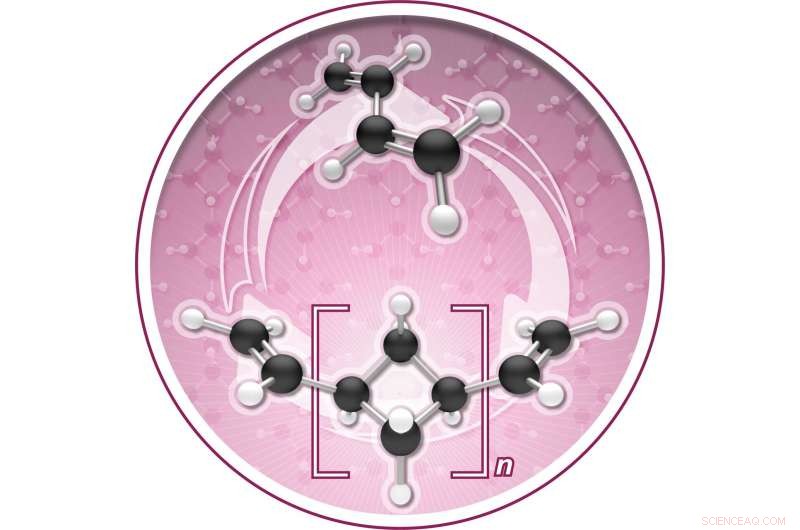
L'oligomérisation [2+2] catalysée par le fer du butadiène produit (1, n'-divinyl)oligocyclobutane, un nouveau polymère qui peut être recyclé chimiquement. Crédit :Jonathan Darmon du Département de chimie de l'Université de Princeton.
Alors que le fardeau de la planète en caoutchouc et en déchets plastiques augmente sans relâche, les scientifiques se tournent de plus en plus vers la promesse du recyclage en boucle fermée pour réduire les déchets. Une équipe de chercheurs du département de chimie de Princeton annonce la découverte d'une nouvelle molécule de polybutadiène - à partir d'un matériau connu depuis plus d'un siècle et utilisé pour fabriquer des produits courants comme des pneus et des chaussures - qui pourrait un jour faire avancer cet objectif grâce à la dépolymérisation.
Le laboratoire Chirik rapporte dans Chimie de la nature que lors de la polymérisation la molécule, nommé (1, n'-divinyl)oligocyclobutane, s'enchaîne dans une séquence répétitive de carrés, une microstructure jusqu'alors non réalisée qui permet au procédé de revenir en arrière, ou dépolymériser, sous certaines conditions.
En d'autres termes, le butadiène peut être « zippé » pour fabriquer un nouveau polymère; ce polymère peut ensuite être décompressé en un monomère vierge pour être réutilisé.
La recherche est encore à un stade précoce et les attributs de performance du matériau doivent encore être explorés en profondeur. Mais le laboratoire Chirik a fourni un précédent conceptuel pour une transformation chimique qui n'est généralement pas considérée comme pratique pour certains matériaux de base.
Autrefois, la dépolymérisation a été réalisée avec des polymères de niche ou spécialisés coûteux et seulement après une multitude d'étapes, mais jamais à partir d'une matière première aussi courante que celle utilisée pour fabriquer le polybutadiène, l'un des sept premiers produits pétrochimiques primaires au monde. Le butadiène est un composé organique abondant et un sous-produit majeur du développement des combustibles fossiles. Il est utilisé pour fabriquer des produits en caoutchouc synthétique et en plastique.
« Prendre un produit chimique très courant que les gens étudient et polymérisent depuis de nombreuses décennies et en faire un matériau fondamentalement nouveau - sans parler du fait que ce matériau possède des propriétés innées intéressantes - non seulement c'est inattendu, c'est vraiment un grand pas en avant. Vous ne vous attendriez pas nécessairement à ce qu'il y ait encore des fruits sur cet arbre, " a déclaré Alex E. Carpenter, un chimiste du personnel avec ExxonMobil Chemical, un collaborateur à la recherche.
"L'objectif de cette collaboration pour nous a été de développer de nouveaux matériaux qui profitent à la société en se concentrant sur de nouvelles molécules que [le chimiste de Princeton] Paul Chirk a découvertes et qui sont assez transformatrices, " ajouta Charpentier.
"L'homme est doué pour fabriquer du butadiène. C'est très bien quand on peut trouver d'autres applications utiles pour cette molécule, parce qu'on en a plein."
Catalyse avec du fer
Le laboratoire Chirik explore la chimie durable en étudiant l'utilisation du fer, un autre matériau naturel abondant, comme catalyseur pour synthétiser de nouvelles molécules. Dans cette recherche particulière, le catalyseur de fer clique les monomères de butadiène ensemble pour produire de l'oligocyclobutane. Mais il le fait dans un motif structurel carré très inhabituel. Normalement, l'enchaînement se produit avec une structure en forme de S qui est souvent décrite comme ressemblant à des spaghettis.
Puis, affecter la dépolymérisation, l'oligocyclobutane est mis sous vide en présence du catalyseur de fer, qui inverse le processus et récupère le monomère. Le papier du labo Chirik, "Synthèse catalysée par le fer et recyclage chimique de Telechelic, 1, 3-Oligocyclobutanes enchaînés, " identifie cela comme un exemple rare de recyclage chimique en boucle fermée.
Le matériau a également des propriétés intrigantes telles que caractérisées par Megan Mohadjer Beromi, un stagiaire postdoctoral au laboratoire Chirik, avec des chimistes du centre de recherche sur les polymères d'ExxonMobil. Par exemple, c'est téléchélique, ce qui signifie que la chaîne est fonctionnalisée aux deux extrémités. Cette propriété pourrait lui permettre d'être utilisée comme un bloc de construction à part entière, servant de pont entre d'autres molécules dans une chaîne polymérique. En outre, il est thermiquement stable, ce qui signifie qu'il peut être chauffé à plus de 250 degrés C sans décomposition rapide.
Finalement, il présente une cristallinité élevée, même à un faible poids moléculaire de 1, 000 grammes par mol (g/mol). Cela pourrait indiquer que les propriétés physiques souhaitables, telles que la cristallinité et la résistance du matériau, peuvent être obtenues à des poids inférieurs à ceux généralement supposés. Le polyéthylène utilisé dans le sac à provisions en plastique moyen, par exemple, a un poids moléculaire de 500, 000g/mol.
"L'une des choses que nous démontrons dans l'article est que vous pouvez fabriquer des matériaux très résistants à partir de ce monomère, " dit Chirik, Professeur de chimie Edwards S. Sanford de Princeton. "L'énergie entre polymère et monomère peut être proche, et tu peux aller et venir, mais cela ne signifie pas que le polymère doit être faible. Le polymère lui-même est solide.
"Ce que les gens ont tendance à supposer, c'est que lorsque vous avez un polymère chimiquement recyclable, il doit être intrinsèquement faible ou non durable. Nous avons fait quelque chose qui est vraiment, très résistant mais est également chimiquement recyclable. Nous pouvons en récupérer du monomère pur. Et cela m'a surpris. Ce n'est pas optimisé. Mais c'est là. La chimie est propre.
"Je pense honnêtement que ce travail est l'une des choses les plus importantes jamais sorties de mon laboratoire, " dit Chirik.
Abandonner l'éthylène
Le projet remonte à quelques années en 2017, quand C. Rose Kennedy, puis un post-doctorat au labo Chirik, remarqué un liquide visqueux s'accumulant au fond d'un ballon au cours d'une réaction. Kennedy a dit qu'elle s'attendait à ce que quelque chose de volatile se forme, le résultat a donc stimulé sa curiosité. En creusant dans la réaction, elle a découvert une distribution d'oligomères - ou de produits non volatils de faible poids moléculaire - qui indiquaient que la polymérisation avait eu lieu.
"Sachant ce que nous savions déjà sur le mécanisme, il était assez clair tout de suite comment il serait possible de les cliquer ensemble d'une manière différente ou continue. Nous avons immédiatement reconnu que cela pourrait être quelque chose de potentiellement extrêmement précieux, " dit Kennedy, maintenant professeur adjoint de chimie à l'Université de Rochester.
À ce stade précoce, Kennedy enchaînait le butadiène et l'éthylène. C'est Mohadjer Beromi qui a supposé plus tard qu'il serait possible d'éliminer complètement l'éthylène et d'utiliser simplement du butadiène pur à des températures élevées. Mohadjer Beromi "a donné" le butadiène à quatre carbones au catalyseur de fer, et cela a donné le nouveau polymère de carrés.
"Nous savions que le motif avait la propension à être recyclé chimiquement, " a déclaré Mohadjer Beromi. " Mais je pense que l'une des caractéristiques nouvelles et vraiment intéressantes du catalyseur de fer est qu'il peut faire [2+2] cycloadditions entre deux diènes, et c'est ce qu'est essentiellement cette réaction :c'est une cycloaddition où vous reliez deux oléfines ensemble pour former une molécule carrée encore et encore.
"C'est la chose la plus cool sur laquelle j'ai jamais travaillé dans ma vie."
Pour caractériser davantage l'oligocyclobutane et comprendre ses propriétés de performance, la molécule devait être mise à l'échelle et étudiée dans une installation plus grande avec une expertise dans les nouveaux matériaux.
"Comment sais-tu ce que tu as fait?" demanda Chirik. "Nous avons utilisé certains des outils normaux que nous avons ici chez Frick. Mais ce qui compte vraiment, ce sont les propriétés physiques de ce matériau, et finalement à quoi ressemble la chaîne."
Pour ça, Chirik s'est rendu à Baytown, Texas l'année dernière pour présenter les résultats du laboratoire à ExxonMobil, qui a décidé de soutenir les travaux. Une équipe intégrée de scientifiques de Baytown a participé à la modélisation informatique, Travaux de diffusion des rayons X pour valider la structure, et des études de caractérisation supplémentaires.
Recyclage 101
L'industrie chimique utilise un petit nombre de blocs de construction pour fabriquer la plupart des matières premières en plastique et en caoutchouc. Trois de ces exemples sont l'éthylène, propylène, et le butadiène. Un défi majeur du recyclage de ces matériaux est qu'ils doivent souvent être combinés puis renforcés avec d'autres additifs pour fabriquer des plastiques et des caoutchoucs :les additifs fournissent les propriétés de performance que nous recherchons :la dureté d'un bouchon de dentifrice, par exemple, ou la légèreté d'un sac d'épicerie. Ces "ingrédients" doivent tous être à nouveau séparés dans le processus de recyclage.
Mais les étapes chimiques impliquées dans cette séparation et l'apport d'énergie nécessaire pour y parvenir rendent le recyclage prohibitif, en particulier pour les plastiques à usage unique. Le plastique est bon marché, poids léger, et pratique, mais il n'a pas été conçu avec l'élimination à l'esprit. Cette, dit Chirik, est le principal, problème de boule de neige avec ça.
Comme alternative possible, la recherche Chirik démontre que le polymère de butadiène est presque énergétiquement égal au monomère, ce qui en fait un candidat pour le recyclage chimique en boucle fermée.
Les chimistes comparent le processus de fabrication d'un produit à partir d'une matière première au roulement d'un rocher sur une colline, avec le sommet de la colline comme état de transition. De cet état, vous faites rouler le rocher de l'autre côté et vous vous retrouvez avec un produit. Mais avec la plupart des plastiques, l'énergie et le coût pour faire rouler ce rocher vers l'arrière jusqu'à la colline pour récupérer son monomère brut sont stupéfiants, et donc irréaliste. Donc, la plupart des sacs en plastique, des produits en caoutchouc et des pare-chocs de voiture finissent dans les décharges.
"La chose intéressante à propos de cette réaction d'accrochage d'une unité de butadiène sur la suivante est que la 'destination' n'est que très légèrement plus faible en énergie que le matériau de départ, " dit Kennedy. " C'est ce qui permet de revenir dans l'autre sens. "
Dans la prochaine étape de la recherche, Chirik a dit que son laboratoire se concentrera sur l'enchaînement, qui, à ce stade, les chimistes n'ont atteint en moyenne que 17 unités. A cette longueur de chaîne, le matériau devient cristallin et si insoluble qu'il tombe du mélange réactionnel.
"Nous devons apprendre quoi faire avec ça, " a déclaré Chirik. "Nous sommes limités par sa propre force. J'aimerais voir un poids moléculaire plus élevé."
Toujours, les chercheurs sont enthousiasmés par les perspectives de l'oligocyclobutane, et de nombreuses investigations sont prévues dans cette collaboration continue vers des matériaux chimiquement recyclables.
"L'ensemble actuel de matériaux que nous avons de nos jours ne nous permet pas d'avoir des solutions adéquates à tous les problèmes que nous essayons de résoudre, " dit Carpenter. " La croyance est que, si vous faites de la bonne science et que vous publiez dans des revues à comité de lecture et que vous travaillez avec des scientifiques de classe mondiale comme Paul, alors cela va permettre à notre entreprise de résoudre des problèmes importants de manière constructive.
"Il s'agit de comprendre une chimie vraiment cool, " il ajouta, « et essayer de faire quelque chose de bien avec. »