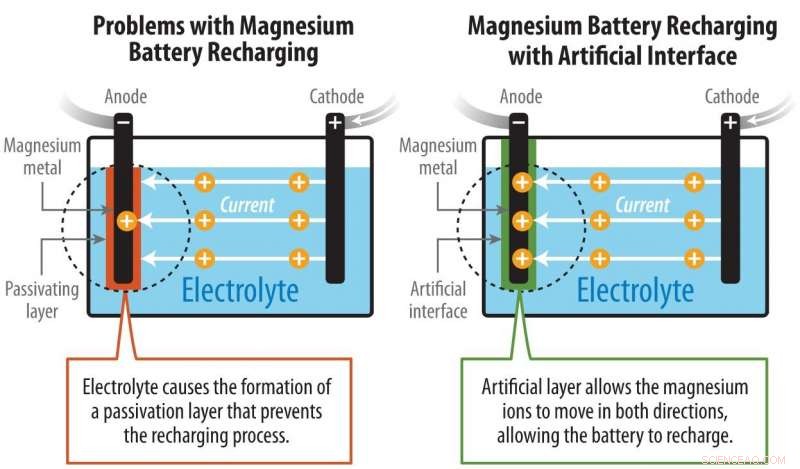
L'illustration montre comment les chercheurs du NREL ont résolu le problème de la fabrication d'une batterie rechargeable au magnésium. Crédit :John Frenzl / NREL
Des scientifiques du Laboratoire national des énergies renouvelables (NREL) du ministère de l'Énergie ont découvert une nouvelle approche pour développer une batterie rechargeable non aqueuse au magnésium-métal.
Un document de preuve de concept publié dans Chimie de la nature a expliqué comment les scientifiques ont mis au point une méthode permettant la chimie réversible du magnésium métallique dans les électrolytes non corrosifs à base de carbonate et testé le concept dans une cellule prototype. La technologie possède des avantages potentiels par rapport aux batteries lithium-ion, notamment, densité d'énergie plus élevée, une plus grande stabilité, et à moindre coût.
Chercheurs du NREL (de gauche à droite) Seoung-Bum Son, Steve Harvey, Andrew Norman et Chunmei Ban sont co-auteurs du Chimie de la nature papier blanc, "Une interphase artificielle permet une chimie réversible du magnésium dans les électrolytes carbonates" travaillant avec une spectrométrie de masse d'ions secondaires à temps de vol. L'appareil leur permet d'étudier les mécanismes de dégradation et de défaillance des matériaux à l'échelle micro à nano. (Photo de Dennis Schroeder / NREL)
« Étant des scientifiques, nous pensons toujours :quelle est la prochaine étape ?", a déclaré Chunmei Ban, un scientifique du département de science des matériaux du NREL et auteur correspondant de l'article, "Une interphase artificielle permet une chimie réversible du magnésium dans les électrolytes carbonates." La technologie dominante des batteries lithium-ion approche de la quantité maximale d'énergie pouvant être stockée par volume, elle a dit, donc "il y a un besoin urgent d'explorer de nouvelles chimies de batterie" qui peuvent fournir plus d'énergie à moindre coût.
"Cette découverte ouvrira une nouvelle voie pour la conception de batteries au magnésium, " dit Seoung-Bum Son, un ancien post-doctorant du NREL et scientifique au NREL et premier auteur de l'article. Les autres co-auteurs de NREL sont Steve Harvey, Adam Stokes, et André Normand.
Une réaction électrochimique alimente une batterie lorsque les ions circulent à travers un liquide (électrolyte) de l'électrode négative (cathode) à l'électrode positive (anode). Pour les batteries utilisant du lithium, l'électrolyte est une solution saline contenant des ions lithium. Ce qui est aussi important, est la réaction chimique doit être réversible pour que la batterie puisse être rechargée.
Les batteries au magnésium (Mg) contiennent théoriquement presque deux fois plus d'énergie par volume que les batteries lithium-ion. Mais les recherches précédentes ont rencontré un obstacle :les réactions chimiques de l'électrolyte carbonate conventionnel ont créé une barrière à la surface du magnésium qui a empêché la batterie de se recharger. Les ions magnésium pourraient s'écouler dans le sens inverse à travers un électrolyte liquide hautement corrosif, mais cela excluait la possibilité d'une batterie au magnésium haute tension réussie.
En cherchant à surmonter ces obstacles, les chercheurs ont développé une interphase artificielle d'électrolyte solide à partir de polyacrylonitrile et de sel d'ion magnésium qui protégeait la surface de l'anode de magnésium. Cette anode protégée a démontré des performances nettement améliorées.
Les illustrations côte à côte montrent comment les scientifiques du NREL ont résolu un problème avec la fabrication d'une batterie rechargeable au magnésium.
Les scientifiques ont assemblé des cellules prototypes pour prouver la robustesse de l'interphase artificielle et ont trouvé des résultats prometteurs :la cellule avec l'anode protégée a permis une chimie réversible du Mg dans l'électrolyte carbonate, ce qui n'a jamais été démontré auparavant. La cellule avec cette anode Mg protégée a également fourni plus d'énergie que le prototype sans la protection et a continué à le faire pendant des cycles répétés. Par ailleurs, le groupe a démontré la capacité de recharge de la batterie magnésium-métal, qui offre une voie sans précédent pour traiter simultanément l'incompatibilité anode/électrolyte et les limitations des ions sortant de la cathode.
En plus d'être plus facilement disponible que le lithium, le magnésium présente d'autres avantages potentiels par rapport à la technologie de batterie plus établie. D'abord, le magnésium libère deux électrons contre celui du lithium, lui donnant ainsi le potentiel de fournir près de deux fois plus d'énergie que le lithium. Et deuxieme, les batteries magnésium-métal ne connaissent pas la croissance des dendrites, qui sont des cristaux pouvant provoquer des courts-circuits et par conséquent des surchauffes dangereuses voire des incendies, rendant les batteries potentielles au magnésium beaucoup plus sûres que les batteries lithium-ion.