Le professeur Bernd Plietker et son groupe de recherche de la Chaire de chimie organique I du TUD ont spécifiquement développé une classe de substances naturelles :les acylphloroglucinols polycycliques polyprénylés (PPAP en abrégé). En raison de ses propriétés, le dérivé PPAP53 résultant se caractérise par un grand potentiel d’application dans un contexte de chimie médicinale. En collaboration avec plusieurs instituts de recherche, comme les universités d'Ulm et de Mayence, il a été démontré que le PPAP53 est très prometteur dans la lutte contre la tuberculose multirésistante et ouvre de nouvelles perspectives de traitement pour les maladies neurodégénératives.
Les résultats de ces travaux de recherche approfondis ont été publiés dans deux articles consécutifs dans le Journal of Medicinal Chemistry. .
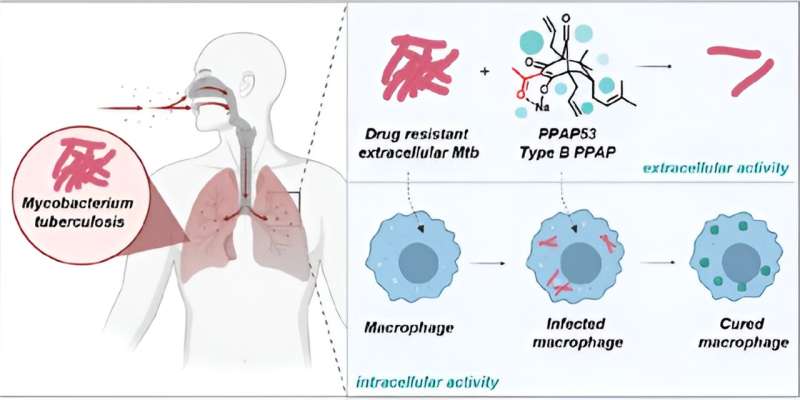
La tuberculose (TB) est une maladie infectieuse répandue qui touche des millions de personnes chaque année. C’était auparavant la principale cause de décès dû à un seul agent pathogène avant la pandémie de COVID-19. La détection précoce de la tuberculose est un défi car la bactérie Mycobacterium tuberculosis (Mtb) peut se cacher dans les macrophages humains, qui font partie du système immunitaire. Cela rend difficile pour les méthodes de diagnostic conventionnelles de détecter l'infection jusqu'à ce que les macrophages s'effondrent, conduisant à une « tuberculose ouverte ».
La tuberculose peut être traitée avec des antibiotiques courants, mais l’exposition répétée du Mtb à ces médicaments peut entraîner le développement de souches multirésistantes et extrêmement résistantes aux médicaments. Cela souligne l'importance de trouver des options de traitement alternatives pour lutter contre cette maladie difficile.
Il y a quelques années, le professeur Bernd Plietker a rendu accessible une nouvelle classe prometteuse de composés actifs à base de substances naturelles en développant une synthèse totale courte et parallélisable :les acylphloroglucinols polycycliques polyprénylés (PPAP en abrégé). "Les premières études sur l'activité antimicrobienne des dérivés non naturels que nous avons développés indiquaient déjà que cette classe de molécules offre un potentiel d'application dans un contexte de chimie médicinale grâce à des interactions avec des protéines associées à la membrane", explique Bernd Plietker, qui a occupé la chaire de chimie organique I à la TU Dresden depuis 2020.
S'appuyant sur ces premiers résultats, lui et son équipe, en coopération avec le professeur Steffen Stenger de l'hôpital universitaire d'Ulm, ont pu montrer qu'un PPAP spécifique, PPAP53, est capable d'activer les macrophages humains pour combattre les bactéries résistantes de la tuberculose sans être toxique. aux macrophages eux-mêmes.
La lutte contre la tuberculose au sein des macrophages est un moyen prometteur de lutter efficacement contre l’infection à un stade précoce et d’éviter ainsi le développement d’une résistance bien avant l’apparition des symptômes de l’infection. Plusieurs tests ont montré que PPAP53 combat exclusivement la tuberculose intracellulaire en traversant ou en activant la membrane cellulaire sans endommager le macrophage.
Un autre avantage du PPAP53 par rapport aux médicaments existants est qu’il n’entraîne pas d’augmentation de la concentration des enzymes hépatiques. Cela évite une diminution de l'efficacité du traitement due à la dégradation indésirable de la substance active dans le foie. De plus, la résistance croisée avec d'autres agents thérapeutiques est évitée, ce qui profite au traitement global de la tuberculose.
Dans la deuxième publication, l'hypothèse a été étudiée selon laquelle l'activation observée des macrophages dépendante de la PPAP pourrait être le résultat d'une interaction avec des récepteurs ou des canaux associés à la membrane. À cette fin, les canaux ioniques TRPC6, responsables du transport ciblé des ions calcium à travers la membrane cellulaire, ont été étudiés. On les trouve principalement dans les cellules neuronales et le cortex surrénalien.
"Dans une combinaison d'expériences biologiques et avec le soutien d'algorithmes d'intelligence artificielle modernes, nous avons pu montrer que PPAP53 se lie de manière très spécifique à l'extrémité C-terminale de ce canal TRPC et l'ouvre au transport du calcium. PPAP53 a ainsi un effet similaire à l'ingrédient actif bien connu, l'hyperforine, dérivé du millepertuis et également utilisé comme antidépresseur.
"Contrairement à l'hyperforine, le PPAP53 ne provoque pas d'augmentation des enzymes hépatiques et évite ainsi la résistance croisée. La solubilité totale dans l'eau du PPAP53 augmente considérablement sa biodisponibilité, tandis que la substitution spécifique sur le corps naturel de la substance permet d'obtenir une stabilité totale à la lumière. Phototoxique les effets secondaires étaient l'un des principaux inconvénients de l'hyperforine, en plus de l'augmentation des concentrations d'enzymes hépatiques.
"Pour la première fois, nous avons pu acquérir une compréhension moléculaire de la relation structure-activité de notre principe actif PPAP53. Les propriétés uniques du PPAP53 ouvrent des perspectives fascinantes dans divers domaines médicaux, par exemple dans la thérapie macrophage, l'oncologie et maladies neurologiques", explique le premier auteur Philipp Pelsalz, expliquant le potentiel du nouveau composé actif.
Plus d'informations : Philipp Peslalz et al, PPAPs d'endotype B non naturels en tant que nouveaux composés actifs contre Mycobacterium tuberculosis, Journal of Medicinal Chemistry (2023). DOI :10.1021/acs.jmedchem.3c01172
Philipp Peslalz et al, Activation sélective d'un canal ionique TRPC6 sur TRPC3 par des acylphloroglucinols polycycliques polyprénylés métallés de type B, Journal of Medicinal Chemistry (2023). DOI :10.1021/acs.jmedchem.3c01170
Informations sur le journal : Journal de chimie médicinale
Fourni par l'Université de technologie de Dresde