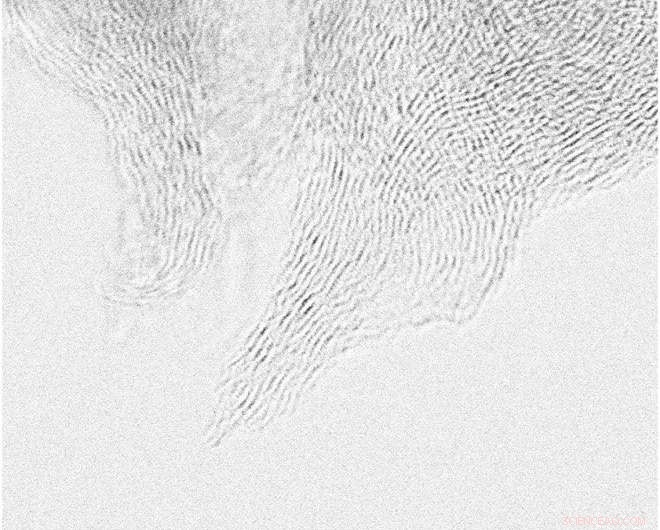
Images de microscopie électronique à transmission à balayage (STEM) corrigées des aberrations de SNC. (A) Les nanospikes vierges présentent des couches de graphène plié avec un certain désordre structurel dû à l'incorporation d'azote dans le plan basal. (B) Le CNS gravé en O conserve la structure de graphène en couches mais présente un rayon beaucoup plus grand à la pointe, abaissant ainsi le champ électrique local présent au niveau des pointes. Crédit: Avancées scientifiques (2018). DOI :10.1126/sciadv.1700336
La recherche d'une méthode de production d'ammoniac plus écoénergétique et respectueuse de l'environnement pour les engrais a conduit à la découverte d'un nouveau type de réaction catalytique.
Des chercheurs du laboratoire national d'Oak Ridge du ministère de l'Énergie ont utilisé des pointes de carbone à l'échelle nanométrique pour catalyser une réaction qui génère de l'ammoniac à partir d'azote et d'eau, aidé par le sel de lithium et l'application d'un champ électrique. L'étude, Publié dans Avancées scientifiques , révèle un type de catalyseur qui a été théoriquement suggéré mais jamais démontré.
« C'est un catalyseur qui fonctionne entièrement sur la base du champ électrique; cela n'a jamais été observé pour l'azote, " a déclaré Adam Rondinone de l'ORNL, l'auteur principal de l'étude. "Nous l'appelons un catalyseur physique, normalement un catalyseur est chimique."
Ammoniac, un composé constitué d'un atome d'azote et de trois atomes d'hydrogène, est généralement produit selon l'approche Haber-Bosch à forte intensité énergétique. Ce processus utilise une température et une pression élevées pour séparer les liaisons stables de l'azote moléculaire, nécessitant de grandes quantités de gaz naturel. La production industrielle d'ammoniac consomme environ 3 % de l'énergie mondiale et génère 3 à 5 % des émissions mondiales de gaz à effet de serre.
« La production d'ammoniac est un énorme problème que nous devons trouver des moyens de résoudre, " a déclaré Rondinone. " Dans la poursuite de cet objectif, nous avons découvert un mécanisme de réaction qui nous ouvre une nouvelle voie."
Contrairement à Haber-Bosch, le processus de l'équipe se déroule à température ambiante dans une solution d'eau, l'azote gazeux dissous et le sel de perchlorate de lithium, à l'aide d'un catalyseur unique sous la forme de pointes de carbone à l'échelle nanométrique. Ces pointes, seulement 50-80 nanomètres de long et un nanomètre de large à la pointe, agissent comme des points chauds pour amplifier le champ électrique et attirer les ions lithium chargés positivement. Le lithium est supposé entraîner des molécules d'azote, qui se concentrent autour des pointes de carbone électrifiées et commencent à réagir pour former de l'ammoniac.
"Chaque catalyseur normal fonctionne en formant une liaison chimique entre la molécule réactive et la surface du catalyseur. Dans ce cas, aucune liaison chimique n'est nécessaire. C'est simplement le champ électrique élevé qui permet à la réaction de se dérouler, ", a déclaré Rondinone.
Le faible rendement de la réaction - environ 12% - limite sa viabilité pour une utilisation industrielle, mais la découverte de son électrochimie unique peut aider à développer des approches alternatives à la génération d'ammoniac.
Les chercheurs ont également utilisé la modélisation informatique et la simulation pour comprendre leurs résultats expérimentaux. Ils ont calculé des prédictions théoriques du champ électrique, l'enrichissement en ions autour des pointes de carbone et les énergies orbitales moléculaires de l'azote pour décrire comment les molécules se sont déstabilisées dans le champ électrique.
"En raison des pointes acérées des nanospike, le champ électrique local est en effet très fort, de l'ordre de 10 volts par nanomètre, " a déclaré le théoricien de l'ORNL Jingsong Huang. " Nous avons effectué des calculs pour étudier le potentiel d'ionisation et l'affinité électronique de l'azote sous des champs électriques appliqués, et ces calculs suggèrent que l'azote autrement inerte devient réactif."
L'étude est publiée sous le titre "Un catalyseur physique pour l'électrolyse de l'azote en ammoniac".
Les coauteurs sont Yang Song de l'ORNL, Daniel Johnson, Rui Peng, Dale Hensley, Peter Bonnesen, Liangbo Liang, Jingsong Huang, Arthur Baddorf, Timothée Tschaplinski, Nancy Engle, Zili Wu, David Cullen, Harry Meyer III, Bobby Sumpter et Adam Rondinone, Fengchang Yang de Virginia Tech, Fei Zhang et Rui Qiao, et Marta Hatzell de Georgia Tech.