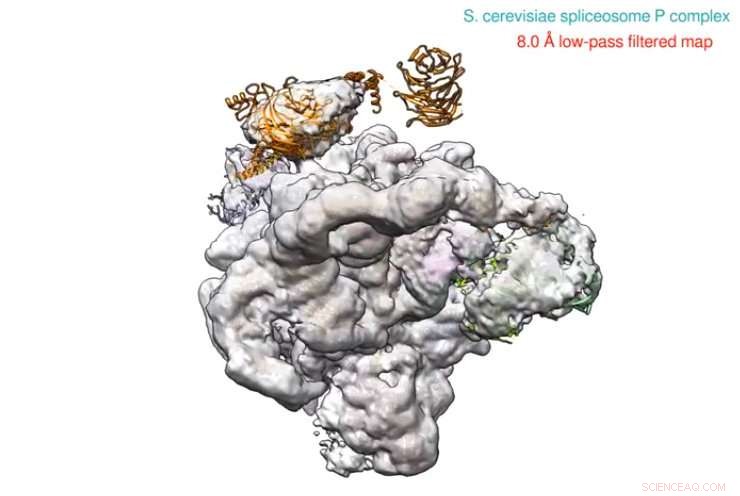
Des chercheurs de l'UCLA ont résolu la structure à haute résolution d'une machine cellulaire massive, le spliceosome, combler la dernière lacune majeure dans notre compréhension du processus d'épissage de l'ARN qui n'était pas claire auparavant.
La structure atomique de cryomicroscopie électronique (cryoEM) du complexe spliceosome P à une résolution de 3,3 Å a été publiée dans un article en ligne de la revue Science .
L'ADN contient le modèle pour qu'une cellule fonctionne, mais le code génétique doit être transcrit en ARN pour traduire le message à la cellule. Le transcrit d'ARN initial est encombré de fragments d'ARN inutiles ou "indésirables" de notre génome appelés introns qui doivent être éliminés, ou épissé, pour transmettre le bon sens – tout comme un monteur de film supprime les séquences inutiles pour créer un montage final pour les cinémas. Le spliceosome est une énorme machine moléculaire composée de 5 petits ARN non codants et de plus d'une centaine de protéines qui éliminent les introns de sorte que seuls les fragments utiles appelés exons restent. Ces exons sont réunis pour créer l'ARN messager final qui peut être traduit en protéine.
Le splicesome change radicalement au fur et à mesure qu'il fonctionne. Globalement, il existe au moins 7 formes connues qui remplissent des fonctions spécifiques. Cette découverte a élucidé le complexe P, maintenant connu dans le détail haute résolution pour être impliqué dans la reconnaissance correcte de l'ARN à couper, rejoindre les exons, et la libération de l'ARN après la coupe.
"Beaucoup de progrès ont été réalisés dans notre compréhension du fonctionnement du spliceosome, mais l'un des plus grands défis restant était de comprendre comment l'exon se dissocie du site actif, " a déclaré le co-premier auteur Shiheng Liu, un chercheur postdoctoral qui travaille avec le co-auteur principal de l'étude, Z. Hong Zhou, directeur de l'Electron Imaging Center for Nanomachines du California NanoSystems Institute de l'UCLA et professeur de microbiologie, immunologie et génétique moléculaire.
"Il y a eu beaucoup de questions liées au complexe P non résolu, " a déclaré Liu. " L'ensemble du cycle d'épissage de l'ARN est mieux compris grâce à cette découverte. "
Les erreurs d'épissage de l'ARN peuvent provoquer un large éventail de maladies humaines, soulignant l'importance d'avoir une connaissance approfondie du fonctionnement du spliceosome.
Plus immédiatement, cette recherche ouvre la porte à des expérimentations biochimiques ciblées basées sur la structure. Avec les modèles atomiques de presque toutes les principales contorsions du splicesome maintenant connus, une compréhension mécanique complète pourrait bientôt être disponible.