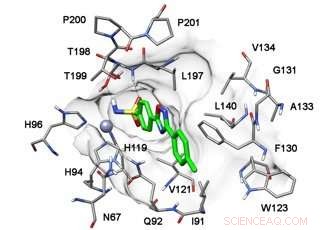
Amarrage de l'un des composés touchés dans l'isoforme humaine de l'anhydrase carbonique II. Crédit :Anton Shetnev
Le glaucome est une maladie grave associée à une augmentation de la pression intraoculaire, conduisant souvent à la cécité. Un traitement consiste à réduire la sécrétion d'humeur aqueuse dans le corps ciliaire de l'œil en inhibant l'activité d'enzymes spéciales appelées anhydrases carboniques. Des scientifiques russes de l'Université RUDN ont conçu de nouveaux composés capables de réduire efficacement la pression intraoculaire en inhibant sélectivement les isoformes de l'anhydrase carbonique humaine. Les résultats de l'étude ont été publiés dans Chimie Bioorganique .
L'étude est centrée sur les dérivés benzènesulfonamides contenant un 1, 2, fraction 4-oxadiazole. « C'était la première fois que ces composés étaient considérés comme des inhibiteurs potentiels de l'anhydrase carbonique humaine. Gérer l'activité de l'enzyme dans les processus ciliaires à l'aide de ce composé, on peut normaliser la pression intraoculaire, " dit Anton Shetnev, l'un des auteurs de l'article de l'Université RUDN.
Les anhydrases carboniques comprennent une famille d'enzymes répandues qui facilitent l'interconversion CO2-bicarbonate dans tous les tissus du corps humain. Leur fonction est de catalyser l'hydratation réversible du dioxyde de carbone, qui produit un anion bicarbonate et un proton. Cette simple réaction biochimique est essentielle à la régulation du pH dans l'espace intra et extracellulaire de divers tissus et organes. Il est à noter que l'anhydrase carbonique est réalisée par 15 isoformes (isoenzymes) localisées dans divers tissus et différant légèrement par l'architecture du site actif. Les inhibiteurs à base de sulfonamide se lient à l'ion zinc prothétique dans la cavité catalytique, supprimant ainsi l'activité de l'enzyme, ce qui peut être décrit comme une interaction "clé-verrou". La plupart des inhibiteurs de l'anhydrase carbonique connus peuvent être comparés à un passe-partout qui ouvre n'importe quelle enzyme de verrouillage (toutes les isoformes) de la famille correspondante.
Puisque l'affinité est non sélective (c'est-à-dire il n'y a pas de filetage de clé entrant exactement dans les rainures), un tel agent peut provoquer de nombreux effets indésirables. Lors du développement d'un candidat-médicament, l'une ou l'autre puissance ou sélectivité de l'inhibiteur sont cruciales. Ce dernier pourrait être réalisé en concevant de petites molécules incorporant des sulfamides portant une périphérie moléculaire appropriée. Notre étude montre qu'en attachant un cycle oxadiazole substitué au fragment benzènesulfonamide, une amélioration substantielle de la puissance et de la sélectivité de l'inhibition peut être obtenue, suggérant que cet échafaudage est prometteur pour le développement de nouveaux médicaments antiglaucomateux.
"Nous continuerons à améliorer la sélectivité de nos inhibiteurs dans les prochaines étapes de notre travail. Nous devons mener des recherches visant à modifier davantage les composés afin de maximiser l'affinité uniquement pour les isoformes cibles, régulation de la pression intraoculaire, ce qui est un grand défi, " conclut Anton Shetnev.