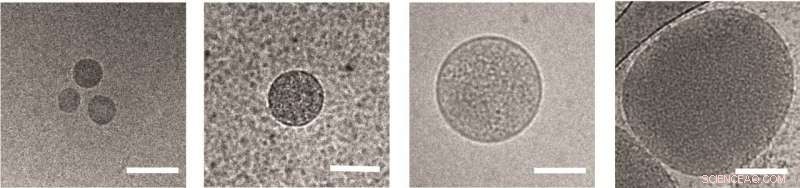
Nanovésicules libérées par les globules rouges infectés par Plasmodium falciparum , vu au microscope électronique. Barre d'échelle :100 nm Crédit :Weizmann Institute of Science
Les efforts mondiaux pour éradiquer le paludisme dépendent de manière cruciale de la capacité des scientifiques à déjouer le parasite du paludisme. Et Plasmodium falciparum est notoirement intelligent :il développe rapidement une résistance contre les médicaments et a un cycle de vie si complexe que le bloquer efficacement avec un vaccin s'est jusqu'à présent révélé insaisissable. Dans une nouvelle étude publiée dans Communication Nature , chercheurs de l'Institut des sciences Weizmann, avec des collaborateurs en Irlande et en Australie, ont montré que Plasmodium falciparum est encore plus sournois qu'on ne le pensait :non seulement il cache les défenses immunitaires du corps, il emploie une stratégie active pour tromper le système immunitaire.
Parmi les maladies transmissibles, le paludisme vient juste après la tuberculose en nombre de victimes, mettant en danger près de la moitié de la population de la Terre. Plus de 200 millions de personnes sont infectées chaque année; environ un demi-million meurent, la plupart sont des enfants de moins de cinq ans. "Le paludisme est l'une des maladies les plus dévastatrices au monde - c'est un véritable fléau pour les pays à faible revenu, où il tue un millier de jeunes enfants chaque jour, " déclare le Dr Neta Regev-Rudzki du département des sciences biomoléculaires de Weizmann. " Pour lutter contre le paludisme, nous devons comprendre la biologie fondamentale de Plasmodium falciparum et comprendre ce qui en fait un tueur si dangereux. »
Regev-Rudzki avait précédemment découvert, dans ses études postdoctorales dans le laboratoire du professeur Alan Cowman au Walter and Eliza Hall Institute of Medical Research à Melbourne, Australie, que ces parasites communiquent entre eux pendant la phase d'incubation dans le sang. Ils le font en libérant des nanovésicules en forme de sac - moins de 1 micron de diamètre - qui contiennent de petits segments de l'ADN du parasite. Apparemment, ces signaux aident les parasites à savoir quand il est temps de commencer à se transformer en formes mâle et femelle, les deux peuvent être transportés par les moustiques dans de nouveaux hôtes. Cette découverte était d'autant plus surprenante que les nanovésicules doivent traverser six membranes distinctes pour communiquer le message d'un parasite à l'intérieur d'un globule rouge à un autre.
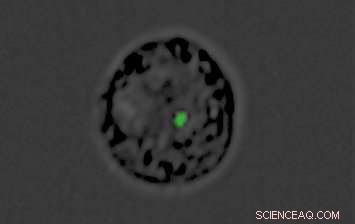
Un monocyte transformé en leurre par le parasite du paludisme :Le point vert est le matériel génétique « cargo » à l'intérieur de la nanovésicule produite par le parasite. Crédit : Institut des sciences Weizmann
Dans la nouvelle étude, réalisée en collaboration avec le professeur Andrew G. Bowie du Trinity College Dublin et d'autres chercheurs, Regev-Rudzki et son équipe Weizmann ont découvert que parallèlement à la communication avec d'autres parasites, Plasmodium falciparum utilise ce même canal de communication dans un autre but :transmettre un message trompeur au système immunitaire de la personne infectée. Dans les 12 heures suivant l'infection des globules rouges, les parasites envoient des nanovésicules remplies d'ADN qui pénètrent dans les cellules appelées monocytes. Normalement, les monocytes forment la première ligne de défense du système immunitaire contre les invasions étrangères, détecter le danger à distance et alerter les autres mécanismes immunitaires pour mettre en place une réponse efficace. Naturellement, le système immunitaire envoie sa prochaine ligne de défense à ces cellules.
Mais en fait, les nanovésicules ont transformé les monocytes en leurres. Pendant que le système immunitaire s'affaire à défendre l'organisme contre un faux danger, la véritable infection se déroule à l'intérieur des globules rouges, permettant au parasite de se multiplier sans entrave à une vitesse vertigineuse. Au moment où le système immunitaire découvre son erreur, un temps précieux a été perdu, et l'infection est beaucoup plus difficile à contenir.
L'équipe de Regev-Rudzki a identifié un capteur moléculaire clé, une protéine appelée STING qui s'active lorsque les nanovésicules du parasite pénètrent dans les monocytes. C'est STING qui délivre la fausse alerte au système immunitaire, l'amenant à « penser » que ses monocytes sont en danger. Lorsque les scientifiques ont « assommé » le gène qui fabrique STING, la chaîne des réactions moléculaires générant l'alerte trompeuse a été interrompue.
"Nous avons découvert une stratégie subversive que le parasite du paludisme utilise pour prospérer dans le sang humain, " dit Regev-Rudzki. " En interférant avec cette subversion du système immunitaire, il sera peut-être possible à l'avenir de développer des moyens de bloquer l'infection paludéenne."