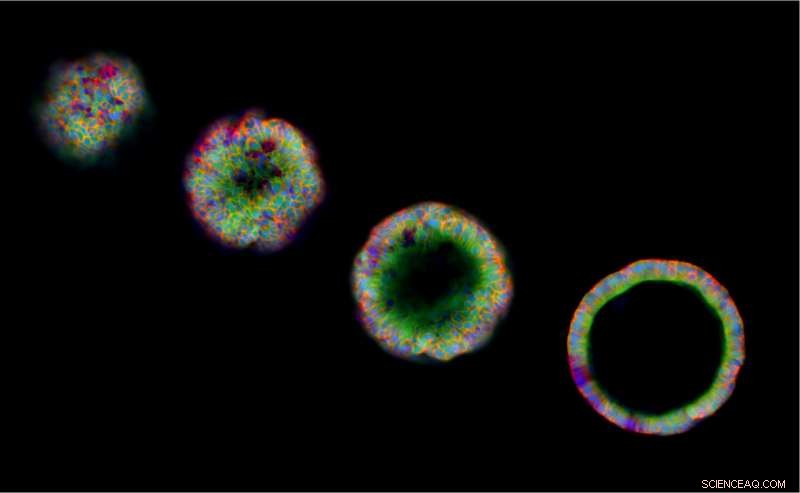
Colonie iPL creuse-luminale. Crédit :Lily Guo
Une version modifiée de la méthodologie iPS, appelé reprogrammation interrompue, permet un très contrôlé, potentiellement plus sûr, et une stratégie plus rentable pour générer des cellules de type progéniteur à partir de cellules adultes. Comme démontré le 30 novembre dans le journal Rapports sur les cellules souches , des chercheurs au Canada ont converti des cellules des voies respiratoires de souris adultes appelées cellules Club en grandes, des populations pures de cellules progénitrices induites (iPL), qui ont conservé une mémoire résiduelle de leur lignée cellulaire parentale et ont donc spécifiquement généré des cellules Club matures. De plus, ces cellules ont montré un potentiel en tant que thérapie de remplacement cellulaire chez les souris atteintes de mucoviscidose.
"Un obstacle majeur dans le chemin critique de la médecine régénérative est le manque de cellules appropriées pour restaurer la fonction ou réparer les dommages, " dit le co-auteur principal Tom Waddell, chirurgien thoracique à l'Université de Toronto. "Notre approche commence par purifier le type cellulaire que nous voulons, puis le manipuler pour donner à ces types cellulaires les caractéristiques des cellules progénitrices, qui peut croître rapidement mais ne produit que quelques types cellulaires. En tant que tel, c'est beaucoup plus direct, plus rapide, et les lots de cellules sont plus purifiés."
Dans les années récentes, Les cellules souches pluripotentes induites (iPS) ont suscité un grand intérêt en tant que source potentiellement illimitée de divers types de cellules pour la transplantation. Cette méthode consiste à reprogrammer génétiquement des cellules cutanées prélevées sur des donneurs adultes à un état semblable à une cellule souche embryonnaire, la croissance de ces cellules immatures en grand nombre, puis les convertir en types de cellules spécialisées trouvées dans différentes parties du corps. Un avantage majeur de cette approche est la capacité de générer des cellules iPS spécifiques au patient pour la transplantation, minimisant ainsi le risque de réactions immunitaires nocives.
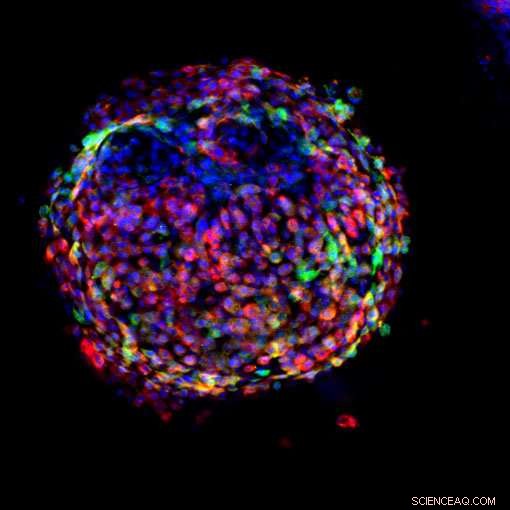
Photographie de cellules des voies respiratoires de souris (Club) dérivées de cellules traitées pendant 4 semaines avec Dox. Crédit :Lily Guo
Malgré d'importants progrès, ces protocoles restent limités par le faible rendement et la pureté des types cellulaires matures souhaités, ainsi que le potentiel des cellules immatures à former des tumeurs. De plus, il n'y a pas d'approche standard applicable à tous les types cellulaires, et le développement de thérapies personnalisées basées sur des cellules pluripotentes dérivées de patients reste très coûteux et prend beaucoup de temps. « Nous avons poursuivi la thérapie cellulaire pour les maladies pulmonaires pendant de nombreuses années, " dit Waddell. " Une question clé est de savoir comment obtenir le bon type de cellules et beaucoup d'entre elles. Pour éviter le rejet, nous devons utiliser les cellules du patient réel."
Pour résoudre ces problèmes, Waddell et l'auteur principal de l'étude Andras Nagy de l'hôpital Mount Sinai ont élaboré une stratégie de reprogrammation interrompue, qui est une version modifiée de la méthodologie iPS. Les chercheurs ont commencé à reprogrammer génétiquement des cellules Club adultes isolées de souris, exprimant de manière transitoire les quatre facteurs de reprogrammation iPS, mais interrompu le processus plus tôt, avant d'atteindre l'état pluripotent, pour générer des cellules de type progéniteur, qui sont plus attachées à une lignée spécifique et montrent une prolifération plus contrôlée que les cellules pluripotentes.
« Le processus de reprogrammation était auparavant considéré comme un processus tout ou rien, " dit Waddell. "Nous avons été surpris de constater à quel point il peut être affiné par le moment et le dosage du médicament utilisé pour activer les facteurs de reprogrammation. C'est intéressant car cela donne beaucoup d'opportunités de contrôle, mais cela signifie que nous avons beaucoup de travail à faire pour bien faire les choses."
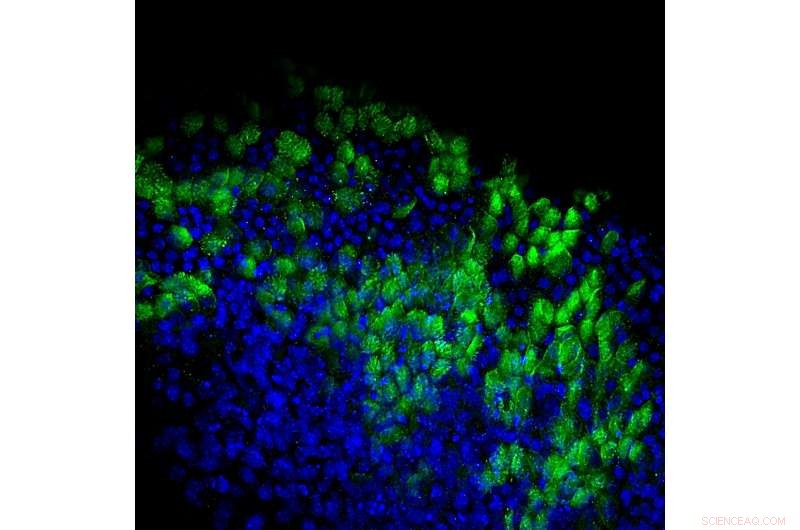
Un épithélium cilié dérivé de cellules iPL. Crédit :Lily Guo
Les chercheurs ont montré que les cellules Club-iPL résultantes pouvaient donner naissance non seulement à des cellules Club, mais aussi à d'autres cellules des voies respiratoires telles que les cellules caliciformes sécrétant du mucus et les cellules épithéliales ciliées qui produisent la protéine CFTR, qui est muté chez les patients atteints de mucoviscidose. Lorsque les cellules Club-iPL ont été administrées à des souris déficientes en CFTR, les cellules se sont incorporées dans les tissus tapissant les voies respiratoires et ont partiellement restauré les niveaux de CFTR dans les poumons sans induire la formation de tumeurs. Cette technologie peut théoriquement être appliquée à presque tous les types cellulaires pouvant être isolés et purifiés, et l'isolement de populations hautement purifiées de cellules adultes de la plupart des organes est déjà possible avec les techniques existantes.
« Créer des types de cellules spécialisées à utiliser en thérapie cellulaire nécessite seulement d'insérer les gènes (ou d'utiliser des approches non transgéniques), puis de tester la dose de médicament et le calendrier requis pour chaque type de cellule et chaque patient, elle doit donc être relativement évolutive à faible coût par rapport à d'autres approches utilisant les propres cellules de chaque patient, " dit Waddell. " Il devrait être très facile pour d'autres laboratoires d'utiliser une approche similaire. "
Selon les auteurs, l'approche pourrait être utilisée pour une variété de pratiques de médecine régénérative, y compris la thérapie de remplacement cellulaire, modélisation de la maladie, et le dépistage de médicaments pour les maladies humaines. Mais il reste encore un long chemin à parcourir avant la traduction clinique. Pour leur part, les chercheurs prévoient de tester cette approche avec d'autres types de cellules, y compris les cellules humaines. Ils essaieront également de déterminer s'il existe des moyens sûrs de greffer ces cellules dans les poumons humains. "L'étude est une preuve de principe, la façon dont ce concept peut finalement être utilisé chez l'homme pourrait être différente, et il faudra de nombreuses années avant que cela ne soit tenté chez l'homme, " dit Waddell.