Le classique de science-fiction de 1982 "Blade Runner" regorge de réflexions dystopiques sur la condition humaine – en plus, il est hautement citable. Il n'y a pratiquement pas de réplique de Rutger Hauer dans le film qui n'ait pas été échantillonnée par un DJ ou utilisée comme titre MySpace. Dans une scène, Le personnage de Hauer - un humain artificiel avec une durée de vie de quatre ans à peine - affronte le scientifique qui l'a créé. Il fait une demande très humaine :« Je veux plus de vie.
En tant que course, nous passons beaucoup de temps à fuir notre propre mortalité. Après tout, la volonté de survivre est essentielle à notre mission génétique de propagation de l'espèce. Dans nos moments les plus ambitieux, on ose même rêver d'immortalité. "L'épopée de Gilgamesh, " le plus ancien texte écrit connu, exploré ce sujet il y a plus de quatre millénaires. Pourquoi mourons-nous ? Et si nous pouvions vivre éternellement ?
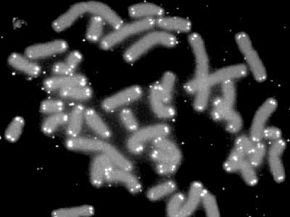
Alors que les aspects philosophiques de ces questions resteront probablement un sujet de discussion pour les siècles à venir, la science moderne a fait des progrès surprenants dans l'étude de télomères . Découvert en 1938 par le généticien Hermann J. Müller, les télomères (en grec pour « partie terminale ») sont essentiellement des capuchons protecteurs composés de courtes séquences d'ADN sur les extrémités des chromosomes. Les chromosomes qu'ils protègent, à son tour, contiennent l'ADN qui détermine l'ensemble de notre profil biologique [source :Huaire]. La généticienne Elizabeth Blackburn les a comparés aux petits capuchons en plastique au bout de vos lacets. Sans eux, les lacets commencent à se défaire.
Chaque fois qu'une cellule se divise, cependant, les télomères deviennent plus courts. S'ils deviennent trop courts, ils atteignent le Limite Hayflick , le point où ils ne peuvent plus protéger les chromosomes des dommages. Dans ce, ils sonnent moins comme des bouts de lacets et plus comme une bougie allumée. Même maintenant, vos télomères peuvent devenir plus courts à chaque division cellulaire, brûlant de plus en plus au point de s'effondrer.
Nous craignons les ténèbres inévitables - méditons sur ses profondeurs incommensurables. La recherche sur les télomères pourrait-elle détenir la clé non seulement pour éviter la mort, mais le vaincre ?
Les personnages bibliques d'Adam, Noé et Mathusalem ont tous vécu plus de 900 ans. Le personnage réplicant de Rutger Hauer dans "Blade Runner, " Roy Batty, à peine atteint son quatrième anniversaire. Aujourd'hui, l'homme moderne bénéficie d'une espérance de vie d'un peu moins de 80 ans dans certaines parties du monde développé [source :NCHS].
Peu importe à quel point vos croyances sont fondamentales ou fantastiques votre fan de science-fiction, vous savez probablement mieux que d'appliquer trop de science dure à l'un de ces exemples. Néanmoins, sur la base de ce que nous savons de la génétique, nous pouvons faire quelques suppositions scientifiques sur les raisons pour lesquelles Noé et ses amis ont vécu si longtemps.
D'une part, Noah est peut-être né avec des télomères assez longs, tandis que Batty tirait la paille la plus courte proverbiale. En réalité, certaines personnes naissent avec des télomères plus longs que d'autres. Comme les télomères raccourcissent à chaque division cellulaire, il vaut mieux commencer à l'avance. Une fois que vous approchez de la limite Hayflick, les effets cellulaires de la vieillesse commencent à s'installer en raison de la mort et des dommages cellulaires. La situation peut même commencer à se dégrader avant.
Les généticiens de l'Université de l'Utah ont découvert que les sujets de test avec des télomères plus courts étaient huit fois plus susceptibles de mourir d'une maladie et trois fois plus susceptibles de mourir d'une crise cardiaque [source :Biever]. Les épidémiologistes de la Harvard Medical School ont également découvert que les femmes ayant des télomères plus courts que la moyenne sont 12 fois plus susceptibles de développer des précurseurs de la démence [source :Scientific American Mind].
Une autre possibilité est que les télomères de Noah et de Batty se soient simplement raccourcis à des rythmes différents. Les télomères ne rétrécissent pas de manière significative chez les humains en bonne santé pendant des décennies en raison d'une enzyme appelée télomérase , qui les répare partiellement et les allonge après chaque raccourcissement.
La télomérase apparaît le plus fréquemment dans les cellules souches, ainsi que dans les cellules qui se divisent fréquemment (comme celles qui participent aux fonctions immunitaires). La production de télomérase est principalement dormante dans la plupart des cellules adultes, mais certains facteurs peuvent augmenter la production. Une étude menée par le Preventive Medicine Research Institute de Californie a constaté une augmentation de 29 % de la production de télomérase chez 24 patients qui sont passés d'un mode de vie sédentaire à un mode de vie défini par l'exercice. alimentation saine et gestion du stress. Noah était-il un fou de santé? Batty était-il simplement stressé ?
Comme vous pouvez l'imaginer, la télomérase a suscité beaucoup d'intérêt. Si cette précieuse enzyme peut éviter le raccourcissement des télomères, alors ne peut-il pas aussi nous permettre de prévenir la mort – ou même d'inverser les effets du vieillissement ?
Si nous n'avons rien appris d'autre de la légende et de la fantaisie, c'est que les quêtes d'immortalité ne se déroulent généralement pas comme nous l'espérons. Qu'il s'agisse de science folle ou de sorcellerie noire, vivre pour toujours s'accompagne souvent de son lot de complications.
Jusque là, des études suggèrent qu'une production accrue de télomérase peut entraîner une durée de vie plus longue et une fonction immunitaire accrue. En théorie, un bon bricolage pourrait empêcher le vieillissement ou même revenir en arrière, créant efficacement des cellules qui n'atteignent jamais la limite Hayflick. Cependant, les cellules immortelles ne sont guère une fontaine de jouvence. Par exemple, les oiseaux de mer connus sous le nom de pétrel tempête de Leach connaissent en fait une croissance des télomères à mesure qu'ils vieillissent - une anomalie inexpliquée dans le règne animal [source:Yeoman]. L'espèce jouit certainement d'une longue durée de vie pour un petit oiseau (jusqu'à 36 ans), pourtant ils meurent encore.
Sur le plan humain, au moins un être humain possédait des cellules immortelles -- et elles ont été trouvées dans une tumeur. En 1951, Henrietta Lacks s'est rendue pour une biopsie de routine à Baltimore, Md. Alors qu'une partie de ses cellules tumorales est allée à un laboratoire pour diagnostic, un autre a été envoyé, sans son autorisation, aux chercheurs de la Johns Hopkins University Medical School [source :Highfield]. Lacks est décédé d'un cancer du col de l'utérus en 1951, mais ses cellules vivent dans les laboratoires du monde entier. Appelées cellules HeLa, ils se divisent indéfiniment. Avant cette découverte, les cellules utilisées dans les laboratoires avaient toujours une durée de conservation liée au raccourcissement des télomères.
Pourquoi ces cellules immortelles ont-elles été trouvées dans une tumeur mortelle ? Alors que la production de télomérase diminue presque entièrement dans les cellules adultes saines, il augmente dans les cellules cancéreuses. En réalité, 90 pour cent des tumeurs humaines présentent plus d'activité télomérase. Rappelles toi, le cancer est essentiellement une réplication cellulaire incontrôlée. Comme les cellules plus âgées sont plus susceptibles de devenir cancéreuses, le rétrécissement des télomères peut en fait avoir évolué comme un moyen de réprimer la croissance tumorale [source :Biever].
Comme vous pouvez vous y attendre, ces faits compliquent l'idée de stimuler la production de télomérase pour arrêter le vieillissement. En réalité, certains scientifiques proposent de diminuer la production de télomérase comme moyen de lutter contre le cancer. En 2009, des chercheurs de la Stanford University School of Medicine ont identifié une protéine appelée TCAB1 qui contrôle le mouvement de la télomérase. En bloquant son expression dans les cellules cancéreuses, les médecins pourront peut-être laisser la nature suivre son cours sur ces cellules incontrôlables.
Scientifiquement parlant, il y a beaucoup à faire sur la recherche sur les télomères, du vieillissement et de la prévention du cancer à l'avenir du clonage. Les scientifiques du monde entier continuent de faire avancer leurs recherches, alors même que leurs propres télomères s'usent régulièrement.
Explorez les liens sur la page suivante pour en savoir encore plus sur la génétique.