Les cellules communiquent entre elles par la sécrétion et l’absorption de vésicules extracellulaires (VE). Les véhicules électriques transportent une multitude de marchandises, notamment des protéines, des lipides et des acides nucléiques. Leur absorption affecte la fonction des cellules réceptrices en influençant les processus de signalisation et l'expression des gènes.
Cependant, malgré des études approfondies sur les véhicules électriques, on sait peu de choses sur leur absorption spécifique par les cellules réceptrices.
"Comprendre comment les cellules réceptrices absorbent les véhicules électriques est essentiel pour déchiffrer les mécanismes plus larges régissant la communication de cellule à cellule dans les processus cellulaires, tant en matière de santé que de maladie", explique Koshi Imami du Centre RIKEN pour les sciences médicales intégratives.
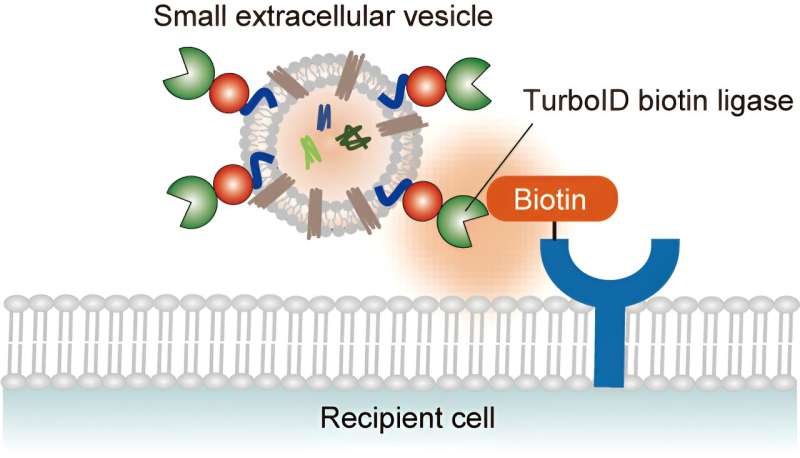
Imami et ses collègues ont maintenant développé une nouvelle méthode pour suivre l'interaction entre les véhicules électriques et les cellules réceptrices. Le système TurboID-EV fonctionne en marquant les protéines cellulaires réceptrices proches des véhicules électriques avec de la biotine (vitamine B7). La recherche est publiée dans la revue Analytical Chemistry .
"Contrairement aux techniques traditionnelles qui marquent les véhicules électriques avec des protéines fluorescentes ou utilisent la microscopie, notre méthode fournit une vue globale des protéines impliquées dans l'absorption des véhicules électriques et les interactions au sein des cellules réceptrices", explique Imami.
En identifiant les protéines marquées à la biotine à l'aide de l'enrichissement biochimique et de la spectrométrie de masse, les chercheurs peuvent obtenir des indices sur les mécanismes moléculaires qui sous-tendent l'absorption des EV.
Imami et ses collègues ont exprimé une biotine ligase conçue pour fusionner avec les membranes EV dans les cellules rénales embryonnaires humaines sans interférer avec la sécrétion EV. En collectant les TurboID-EV sécrétés et en les incubant avec des cellules réceptrices marquées avec des acides aminés lourds et complétées par de la biotine, ils ont pu examiner les événements de biotinylation qui se produisent lors de l'absorption des EV.
Les chercheurs ont identifié plus de 450 protéines réceptrices biotinylées. Ils comprenaient des protéines bien connues impliquées dans le processus par lequel les cellules engloutissent des substances externes pour les y introduire. L'équipe a également découvert des protéines impliquées dans le transport intracellulaire et des protéines associées à la membrane, qui pourraient être essentielles à l'absorption des EV dans ce modèle.
La méthode peut être adaptée à différents sous-types d’EV et types de cellules. "La polyvalence de notre système permet aux chercheurs d'étudier la spécificité des mécanismes d'absorption des EV dans de nombreux contextes biologiques", explique Imami.
La découverte des protéines impliquées dans l'absorption des EV pourrait approfondir notre compréhension de la façon dont les cellules cancéreuses se propagent et aider à développer des systèmes d'administration de médicaments basés sur les EV qui ciblent des types de cellules spécifiques.
L'équipe d'Imami tente maintenant d'appliquer le système TurboID-EV à un modèle de souris pour comprendre comment le cancer se propage entre les organes. "On sait que les véhicules électriques dérivés de tumeurs sont absorbés par des cellules spécifiques d'un organe pour préparer la propagation du cancer à de nouveaux organes", explique Imami. "Nous voulons caractériser la fonction de ces véhicules électriques."
Plus d'informations : Yuka Li et al, TurboID-EV :Cartographie protéomique des protéines cellulaires réceptrices à proximité des petites vésicules extracellulaires, Chimie analytique (2023). DOI :10.1021/acs.analchem.3c01015
Informations sur le journal : Chimie analytique
Fourni par RIKEN