Des recherches récentes ont identifié MYT1 comme une nouvelle cible thérapeutique prometteuse pour le cancer du sein et gynécologique et ont découvert une série d'inhibiteurs nouveaux, puissants et hautement sélectifs ciblant spécifiquement MYT1.
Ces résultats, publiés dans le Journal of Medicinal Chemistry , ont été soutenus par le moteur de biologie et de chimie générative piloté par l'IA d'Insilico Medicine.
Partout dans le monde, les cancers du sein et gynécologiques constituent de graves menaces pour la santé, la fertilité et la qualité de vie globale des femmes. Afin d'identifier des cibles potentielles pour de nouveaux traitements, l'équipe de recherche a exploité PandaOmics, la plateforme exclusive d'identification de cibles basée sur l'IA d'Insilico, pour analyser les données sur cinq formes de cancers gynécologiques, notamment le cancer de l'ovaire, de l'endomètre, du col de l'utérus et du sein, en particulier le cancer triple négatif. cancer du sein.
Remarquablement, MYT1 s'est systématiquement classé au premier rang pour toutes les maladies en termes de pertinence.
MYT1 est un membre de la famille des Wee1-kinase, rarement exprimé dans la plupart des tissus normaux mais fortement exprimé dans la plupart des types de cancer. Il a été rapporté que l'inhibition de MYT1 et l'amplification de CCNE1, une condition connue sous le nom de létalité synthétique, jouent des fonctions cruciales dans la régulation du cycle cellulaire, ce qui indique que l'inhibition de MYT1 est une stratégie thérapeutique létale synthétique prometteuse pour le traitement des cancers présentant une instabilité du génome (par exemple, amplification de CCNE1) .
Cependant, MYT1 est hautement homologue à Wee1, ce qui rend difficile la conception d’inhibiteurs sélectifs de MYT1. Dans cette étude, Insilico a comblé le manque d'inhibiteurs sélectifs de MYT1 avec le soutien de Chemsitry42, la plateforme de génération de petites molécules basée sur l'IA d'Insilico.
En utilisant des stratégies de conception de médicaments basées sur la structure (SBDD) et en appliquant des filtres rigoureux de similarité et de sélectivité, Insilico a conçu une gamme de composés ciblant MYT1 à partir de zéro. Parmi ces nouveaux composés, une série s'est révélée être un composé à succès.
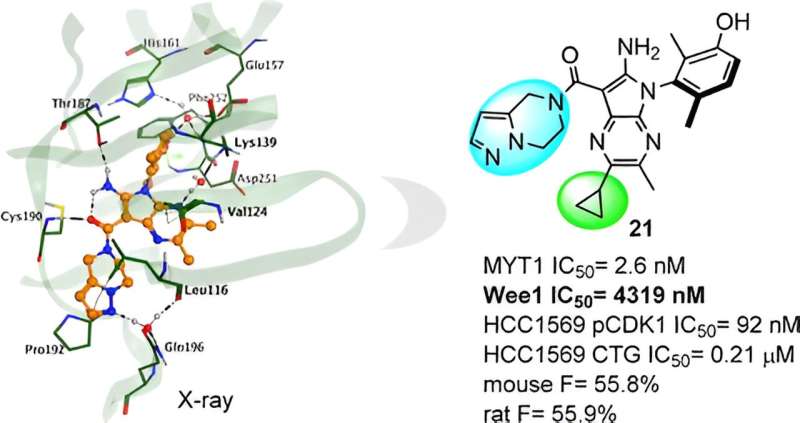
Insilico a ensuite effectué une analyse de la structure cristalline aux rayons X du complexe et a découvert un impact significatif sur l'activité de modifications subtiles de la structure chimique. Ces connaissances ont fourni des conseils pour une optimisation moléculaire plus poussée, conduisant Insilico à la découverte du composé principal, le composé 21.
Le composé 21 présente une bonne activité MYT1 et une excellente sélectivité par rapport à Wee1, et l'autre panel de kinases réduit le risque potentiel d'effets hors cible et pourrait se traduire par un profil plus sûr. Dans les études précliniques, il montre également une puissante efficacité antitumorale in vivo et un profil prometteur en matière d'ADME et de PK/PD.
« L'approche innovante de ce programme a non seulement présenté une méthode d'identification efficace des cibles, mais a également conduit au développement d'un inhibiteur sélectif prometteur de MYT1 », a déclaré Yazhou Wang, Ph.D., responsable de la chimie médicinale du programme MYT1 d'Insilico. Medicine, et premier auteur de cet article. "Le composé 21 élargit le pipeline synthétique létal d'Insilico et ouvre la voie à un avenir thérapeutique plus sûr et plus efficace pour les patientes luttant contre des cancers gynécologiques et du sein."
Plus d'informations : Yazhou Wang et al, Découverte de dérivés de la tétrahydropyrazolopyrazine en tant qu'inhibiteurs puissants et sélectifs de MYT1 pour le traitement du cancer, Journal of Medicinal Chemistry (2023). DOI :10.1021/acs.jmedchem.3c01476
Informations sur le journal : Journal de chimie médicinale
Fourni par InSilico Medicine