Crédit :Wiley
L'oxyde nitrique (NO) et le sulfure d'hydrogène (H 2 S) agissent comme des molécules de signalisation gazeuses avec des effets physiologiques similaires. Bon nombre des questions critiques sur l'interaction entre ces deux gazotransmetteurs dépendent de leur réactivité chimique et de l'existence éphémère de HSNO, un produit clé de la réaction entre eux. Une équipe de chercheurs a pu stabiliser, isoler, et caractériser deux des espèces liées à ces voies de signalisation par liaison à un complexe de zinc, comme indiqué dans le journal, Angewandte Chemie .
Le NO est une molécule de signalisation centrale en biologie qui régule de nombreuses fonctions physiologiques qui incluent la dilatation vasculaire, transmission de l'influx nerveux, et la protection cellulaire. De façon intéressante, H 2 S présente des effets similaires, relaxant les cellules musculaires lisses impliquées dans la vasodilatation. HSNO peut donc jouer un rôle clé dans le chevauchement de ces voies de signalisation. Cette espèce extrêmement réactive est si instable, cependant, que sa biochimie et ses voies réactionnelles discrètes sont très difficiles à déterminer. HSNO traverse facilement les membranes cellulaires et peut nitrosyler les protéines, transférer son groupe nitrosyle (–N=O) à d'autres résidus, en particulier la cystéine, qui représente une étape importante dans un certain nombre de mécanismes de régulation cellulaire. Au pH biologique, HSNO existe probablement sous forme d'anion thionitrite SNO
−
qui est instable vis-à-vis de la conversion en anion perthionitrite SSNO
−
.
L'étudiant diplômé Valiallah Hosseininasab dans l'équipe dirigée par Timothy H. Warren à l'Université de Georgetown (Washington, D.C., États-Unis) a stabilisé le SNO
−
et SSNO
−
anions par liaison à un complexe de zinc spécial inspiré d'un environnement commun pour le zinc en biologie. Le zinc est un métal physiologiquement important qui est impliqué dans une myriade de processus qui incluent la régulation du pH sanguin par l'intermédiaire de l'enzyme anhydrase carbonique. De plus, molécules impliquées dans la signalisation du monoxyde d'azote, comme H 2 S et S-nitrosothiols (molécules à groupement –S–N=O), réagissent facilement avec les liaisons zinc-soufre qui forment des unités structurelles importantes dont la modification des protéines entraîne un changement fonctionnel.
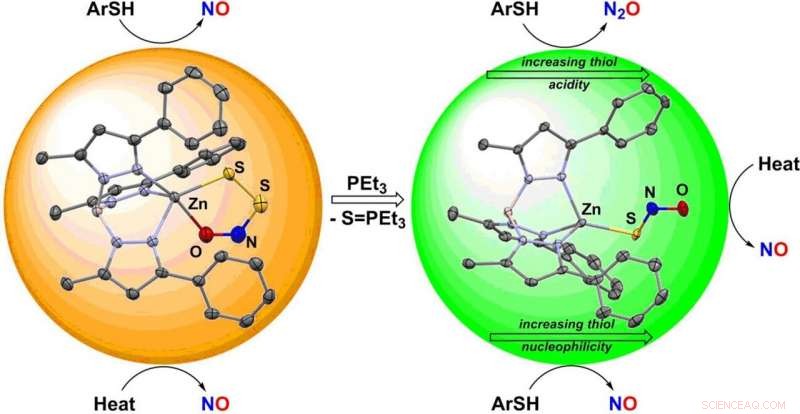
L'équipe de Georgetown a révélé que les complexes de zinc contenant le SNO
−
et SSNO
−
les anions pourraient être isolés et caractérisés. L'étude de leurs schémas de réactivité a montré des différences intéressantes dans leurs réactions avec les thiols (substances avec un groupe sulfure,
–
SH), antioxydants omniprésents qui aident à protéger les cellules contre les dommages. Alors que les réactions avec le perthionitrite forment NO, le thionitrite forme soit de l'oxyde de diazote (gaz hilarant) N 2 O ou S-nitrosothiols, qui représentent des réservoirs prêts de NO. Ces résultats suggèrent que les plus petites différences au cours des voies de signalisation physiologiques peuvent conduire à des signaux de sortie différents qui résultent finalement de l'interaction entre NO et H. 2 S.
