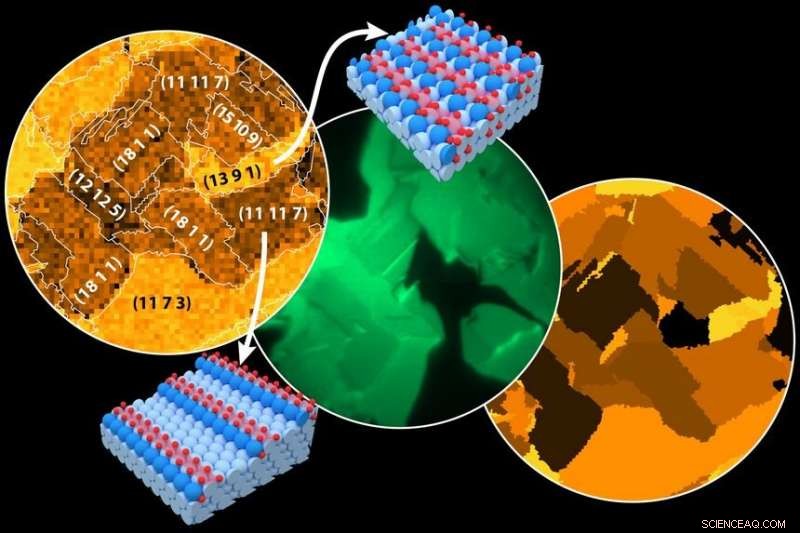
De gauche à droite :Sites favoris de l'oxygène :carte de l'oxydation du Rh, mesuré par Microscopie Photoélectronique à Balayage (SPEM); microscopie électronique à photoémission in situ (PEEM) de l'oxydation catalytique de l'hydrogène sur Rh ; carte d'activité. Champ de vision 500 µm. Modèles :terrasse- (bleu clair) et marche- (bleu) atomes de Rh, atomes de Rh oxydés (rouge clair), O atomes (rouge). Crédit :Université de technologie de Vienne
Les surfaces métalliques jouent un rôle de catalyseur pour de nombreuses applications importantes, des piles à combustible à la purification des gaz d'échappement des voitures. Cependant, leur comportement est affecté de manière décisive par les atomes d'oxygène incorporés dans la surface.
Ce phénomène est connu depuis longtemps, mais jusqu'à présent, il n'a pas été possible d'étudier avec précision le rôle de l'oxygène dans les surfaces complexes point par point afin de comprendre le fond chimique au niveau atomique. Ceci a maintenant été réalisé à TU Wien en coopération avec une équipe du synchrotron Elettra à Trieste. Il est devenu possible d'expliquer pourquoi dans les études précédentes des résultats en partie contradictoires avaient été obtenus :les atomes d'oxygène ne sont pas répartis uniformément, mais s'installent particulièrement facilement dans des endroits bien précis.
Mesures de précision au lieu de valeurs moyennes
"C'est un grand défi d'examiner une surface métallique directement pendant la catalyse, ", déclare le professeur Günther Rupprechter de l'Institut de chimie des matériaux de la TU Wien. "Vous pouvez, bien sûr, placez le catalyseur entier dans un réacteur et mesurez exactement quels produits chimiques sont produits, mais vous n'obtenez qu'une valeur moyenne. Vous ne pouvez pas savoir quels sites sur le catalyseur ont contribué à la réaction chimique et de quelle manière. »
Une autre possibilité est de ne pas utiliser de vrai catalyseur, mais un simple, très propre, morceau idéalisé de celui-ci - comme un minuscule monocristal, aux propriétés reconnues, que vous pourrez ensuite étudier au microscope. Dans ce cas, tu deviens précis, résultats reproductibles, mais ils n'ont pas grand-chose à voir avec des applications pratiques.
Le groupe de recherche dirigé par Günther Rupprechter et Yuri Suchorski a donc combiné les avantages des deux approches. Ils utilisent des feuilles minces en rhodium, qui sont constitués de petits grains. Sur chaque grain, les atomes de surface peuvent être disposés différemment. Dans un seul grain, ils forment un lisse, surface régulière avec les atomes extérieurs tous exactement dans le même plan ; à côté de cela, les atomes peuvent s'arranger pour former une structure plus compliquée composée de nombreuses étapes atomiques.
Les endroits préférés des atomes d'oxygène
Ce sont précisément ces étapes qui s'avèrent cruciales. "Pour l'activité catalytique, l'état d'oxydation du catalyseur joue un rôle central, c'est-à-dire que l'oxygène s'attache ou non aux atomes métalliques, " dit Philipp Winkler, le premier auteur de l'article. « Dans des expériences antérieures, nous avons découvert que nous avions souvent affaire à un certain état entre « oxydé » et « non oxydé » – une situation difficile à interpréter. »
Cependant, cela peut être compris quand on se rend compte que tous les grains de la feuille de rhodium ne sont pas oxydés au même degré. L'oxydation commence de préférence dans les coins, bords et marches - là, il est particulièrement facile pour les atomes d'oxygène de se lier à la surface. Par conséquent, différents grains avec différentes structures de surface sont oxydés à des degrés différents.
Microscope électronique et synchrotron à Trieste
Cela pourrait être étudié en utilisant une combinaison de technologies très développées :« Dans un microscope électronique spécial, l'échantillon est irradié avec de la lumière UV pendant la réaction catalytique et l'émission d'électrons résultante est enregistrée avec une résolution spatiale micrométrique, " explique Youri Suchorski, "cela nous permet de déterminer exactement quels grains de la feuille de rhodium sont particulièrement actifs sur le plan catalytique. Le même échantillon est ensuite réexaminé avec un tout autre microscope :grain par grain avec des rayons X au synchrotron, obtenir des informations très précises sur l'oxydation de surface de l'échantillon."
Si vous combinez les deux résultats, vous pouvez déterminer exactement quel comportement chimique est caractéristique pour des structures particulières. Le principal avantage :il est possible d'examiner la totalité de la feuille de rhodium contenant des centaines de grains différents en une seule expérience. Au lieu d'étudier séparément de minuscules monocristaux, un échantillon contenant de nombreuses structures différentes utilisées pour la catalyse est étudié en conditions réelles, et des informations sur les propriétés de ces structures sont obtenues à la fois.
"C'est une étape importante dans la recherche sur la catalyse, " nous dit Rupprechter. " Désormais, nous n'avons plus à nous contenter de mesurer une valeur moyenne qui décrit de manière inadéquate l'ensemble de l'échantillon, mais nous pouvons vraiment comprendre en détail quelles structures atomiques présentent quels effets. Cela permettra également d'améliorer spécifiquement les catalyseurs importants qui sont nécessaires pour de nombreuses applications dans les technologies énergétiques et environnementales. »