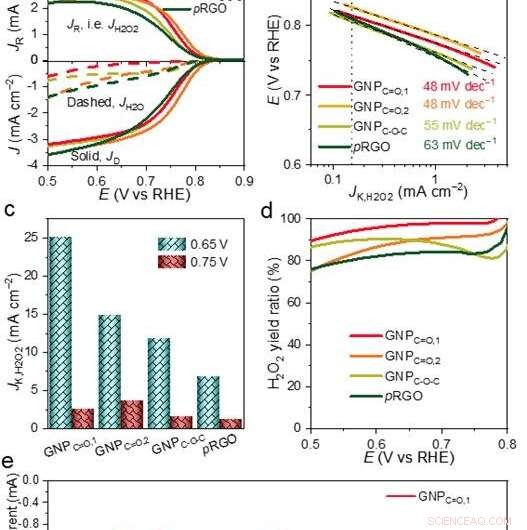
Figure 1. Les caractérisations des performances de l'ORHP. Crédit :Professeur Jong-Beom Baek, UNIST
Peroxyde d'hydrogène (H
Une équipe de recherche, dirigé par le professeur Jong-Beom Baek de l'École d'ingénierie énergétique et chimique de l'UNIST a développé un catalyseur électrochimique à haute efficacité à base de carbone destiné à produire H
Peroxyde d'hydrogène (H
L'équipe de recherche s'est concentrée sur la méthode électrochimique comme méthode de production de peroxyde d'hydrogène pour remplacer le procédé à l'anthraquinone. Il s'agit d'induire une réduction de l'oxygène en peroxyde d'hydrogène en développant des catalyseurs à haut rendement basés sur des matériaux carbonés peu coûteux. Ils ont synthétisé le catalyseur en attachant des groupes fonctionnels tels que la quinone, éther, et du carbonyle aux matériaux à base de carbone minces tels que le graphène. Par conséquent, il a réussi à synthétiser un catalyseur avec un rendement élevé de 97,8%.
L'étude a également identifié le site actif exact où la réaction catalytique a lieu. Le matériau à base d'oxyde de carbone précédemment rapporté comme catalyseur générant du peroxyde d'hydrogène contient divers groupes fonctionnels d'oxygène, on ne sait donc pas exactement quel groupe fonctionnel est le site actif du catalyseur. Cette fois, les sites actifs exacts ont été analysés en synthétisant des matériaux d'oxyde de carbone avec des groupes fonctionnels d'oxygène séparés tels que la quinone, éther, et carbonyle. Par conséquent, il a été confirmé que le matériau d'oxyde de carbone ayant de nombreux groupes fonctionnels quinone présente l'efficacité catalytique la plus élevée.
"Cette étude vise à accroître la compréhension des sites actifs importants pour la production de peroxyde d'hydrogène, " dit Gao-Feng Han, l'auteur principal de l'étude. « En plus de l'expérience, la méthode de calcul de la théorie de la fonction de densité a été utilisée pour confirmer que le groupe fonctionnel quinone avait une activité catalytique élevée et une très faible surtension dans la réaction de production de peroxyde d'hydrogène (ORHP)."
"Nos résultats fournissent des lignes directrices pour la conception de catalyseurs à base de carbone, qui ont simultanément une sélectivité et une activité élevées pour H