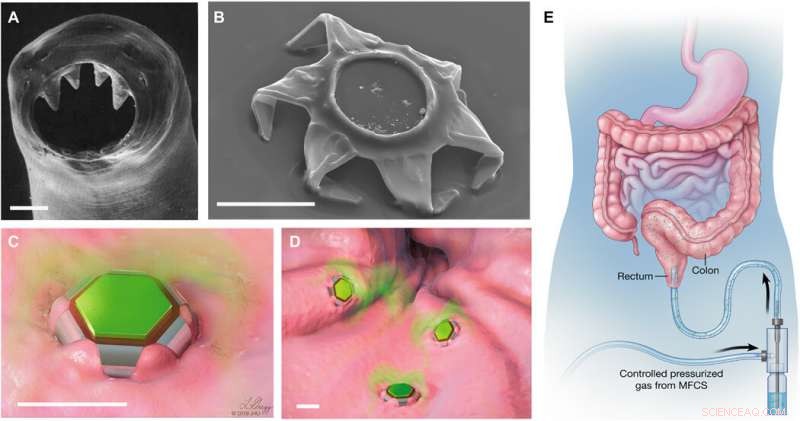
Thérapeutes à changement de forme en tant que dispositifs d'administration de médicaments à verrouillage automatique. (A) Image en microscopie électronique à balayage (MEB) des dents ventriculaires de l'ankylostome A. duodenale. Le ver utilise ces dents pointues pour pénétrer dans la muqueuse et adhère au tractus gastro-intestinal jusqu'à 2 ans. Réimprimé de Human Parasitology, 4e éd. Droit d'auteur 2013, avec la permission d'Elsevier. (B) Image SEM d'un theragripper dans la configuration fermée. Comme l'ankylostome, les theragrippers sont équipés de micropointes acérées. Illustrations schématiques de (C) une seule et (D) de nombreuses pinces thérapeutiques attachées au tissu muqueux et libérant un médicament encapsulé (coloré en vert). Barres d'échelle, 100 µm (A à D). (E) Illustration conceptuelle de l'administration rectale de theragrippers chargés de médicaments à l'aide d'un contrôleur de débit microfluidique actionné par pression. Les images (C) à (E) ont été illustrées par L. Gregg. MFCS, système de contrôle de flux microfluidique. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abb4133
L'histoire de couverture en ligne de Avancées scientifiques cette semaine présente un microdispositif gastro-intestinal (GI) conceptuel, développé par une équipe de recherche pour la libération prolongée de médicaments. Les plates-formes d'administration de médicaments pour une libération prolongée de médicaments se sont avérées difficiles à développer en bio-ingénierie en raison des mouvements du tractus gastro-intestinal (GI) et de leur élimination résultante du corps. Dans un nouveau rapport, Arijit Ghosh et une équipe de chercheurs interdisciplinaires en génie chimique et biomoléculaire, gastro-entérologie et hépatologie, la science des matériaux, la découverte de médicaments et la neurologie à l'Université Johns Hopkins aux États-Unis ont signalé de nouveaux dispositifs chargés de médicaments bioinspirés par les mécanismes de préhension des vers ronds parasites connus sous le nom d'ankylostomes. Les parasites peuvent s'attarder dans l'intestin grêle pendant des périodes prolongées en se nourrissant du sang de leur hôte.
Ghosh et al. conçu et développé une construction de préhension qu'ils appelaient theragrippers pour enfoncer leurs griffes dans le tissu muqueux du tractus intestinal. Les dispositifs effectuaient une préhension en réponse à la chaleur corporelle ou à d'autres signaux biologiques et libéraient des médicaments dans la lumière gastro-intestinale. Comme preuve de concept, ils ont montré comment les dispositifs se sont accrochés au tractus gastro-intestinal de rats vivants pendant 24 heures et ont démontré une multiplication par six de la demi-vie d'élimination d'un médicament anti-inflammatoire non stéroïdien utilisé pour soulager la douleur modérée. Les travaux ont montré que l'appareil aidait le médicament à rester dans le corps pendant une période beaucoup plus longue. Le travail fournit des preuves de première classe sur les microdispositifs à verrouillage automatique pour améliorer efficacement l'administration prolongée et améliorée de médicaments.
Délivrance de médicaments dans le tractus gastro-intestinal
Dans ce travail, Ghosh et al. ont été inspirés par le biomécanisme des Ancylostoma duodenale (ankylostomes) qui résident dans l'intestin humain jusqu'à deux ans. Les travaux ont présenté les premières preuves précliniques d'outils de verrouillage à l'échelle submillimétrique pour une libération et une rétention améliorées du médicament in vivo. L'administration de médicaments par le tractus gastro-intestinal peut améliorer l'observance par rapport aux injectables, résultant en un meilleur traitement. Les médicaments administrés par le tractus gastro-intestinal permettent une absorption et une circulation systémique efficaces en raison de l'énorme surface intestinale et de la riche vascularisation de la muqueuse du tractus gastro-intestinal. Par exemple, les scientifiques avaient déjà développé des particules pénétrant le mucus (MPP) pour une meilleure rétention, bien que de tels dispositifs aient été retirés après une journée en raison de l'élimination de la couche de mucus sous-jacente. Il existe donc actuellement un besoin urgent de développer des systèmes d'administration de médicaments étendus.
Représentation schématique des microdispositifs inspirés des ankylostomes qui améliorent l'extension du médicamentReprésentation schématique des microdispositifs inspirés des ankylostomes qui améliorent l'administration prolongée du médicament chez le rat. Crédit d'image:Lydia Gregg 2020 JHU, Avancées scientifiques, doi :10.1126/sciadv.abb4133 livraison chez le rat. Crédit d'image:Lydia Gregg 2020 JHU, Avancées scientifiques, doi:10.1126/sciadv.abb4133
L'expérience :développer des agrippeurs
Pour réaliser un verrouillage automatisé dans la lumière gastro-intestinale, Ghosh et al. reposait sur le déclenchement thermique de l'appareil. Ils ont verrouillé un patch de charge de médicament sur les microactionneurs pour administrer du kétorolac (un analgésique) comme médicament modèle. Les theragrippers ont été retenus dans le côlon pendant 24 heures, permettant une exposition importante au médicament, entraînant une concentration plasmatique de kétorolac 10 fois plus élevée 12 heures après l'administration. Le travail de preuve de concept a validé l'actif, Theragrippers à changement de forme et à verrouillage automatique pour une libération prolongée du médicament dans le tractus gastro-intestinal. Les scientifiques ont utilisé plusieurs micropointes pointues pour concevoir les pinces à dents assurant un verrouillage sur la muqueuse gastro-intestinale un peu comme les ankylostomes. Ils ont coiffé l'épais, segments rigides et charnières bicouches des pinces avec une couche de cire thermosensible. La couche de paraffine ou de cire de surface du dispositif s'est ramollie à la température du corps après l'implantation pour déclencher de manière autonome les griffes à l'intérieur du tractus gastro-intestinal du modèle animal.
L'équipe a utilisé des matériaux hybrides contenant un polymère métallique fait d'or et de chrome et portant un patch polymère à élution médicamenteuse pour la libération contrôlée de médicaments. La force adhésive du polymère chargé de médicament à l'échafaudage métallique sous-jacent a empêché le délaminage (retrait) du patch médicamenteux pendant le péristaltisme gastro-intestinal. Les matériaux étaient biocompatibles sans toxicité potentielle pour l'administration de médicaments. L'équipe a sélectionné la voie rectale d'administration du dispositif la plus courante chez les patients pédiatriques et dans les interventions thérapeutiques pour la colite ulcéreuse.
La fluorescéine a permis la visualisation de la libération chimique des pinces. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abb4133 
Ghosh et al. a d'abord réglé la porosité du patch médicamenteux déposé par électrolyse sur l'appareil pour charger et libérer les médicaments pendant 24 heures. Ils ont utilisé du kétorolac, un produit approuvé par la Food and Drug Administration des États-Unis, non stéroïdien, anti-inflammatoire comme candidat modèle avec un profil de clairance élevé (demi-vie inférieure à 3 heures) pour des expériences in vivo dans un modèle rongeur. La taille des pores du polymère a facilité la libération de quantités substantielles de kétorolac à un taux acceptable, et l'équipe a utilisé des théragrippers de 250 µm pour l'administration de médicaments in vivo chez le rat. Les constructions étaient 32 fois plus petites que le diamètre typique du côlon chez les rats et pesaient environ 300 g. Ghosh et al. régler la pénétration du theragripper en faisant varier les paramètres de la construction, et a utilisé la méthode des éléments finis pour estimer la force générée par les griffes pliantes de l'appareil. L'équipe a appliqué une contrainte à la pointe du theragripper pour l'empêcher de se replier pendant les simulations et a calculé la pression approximative de chaque micropointe du theragripper sur le côlon, qui était comprise entre 0,4 et 0,6 MPa. Les résultats ont indiqué leur potentiel à exercer une pression suffisante pour briser la barrière muqueuse sans endommager le côlon.
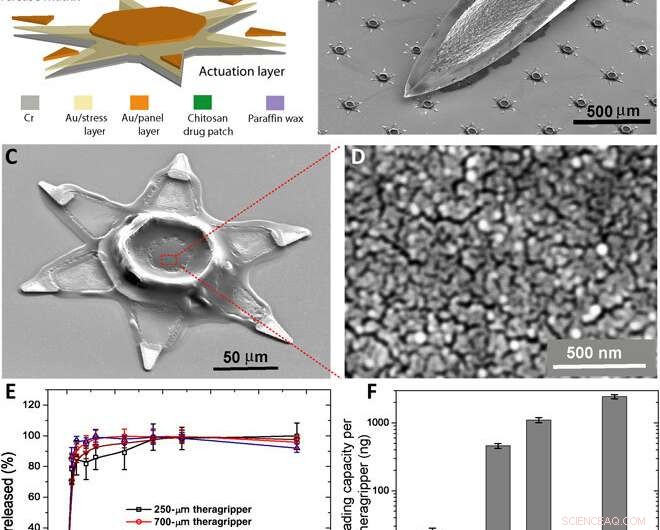
Fabrication parallèle des theragrippers et de leurs caractéristiques de chargement et de libération de médicament in vitro. (A) Schéma fonctionnel illustrant les étapes de microfabrication pour une gamme de theragrippers, montrant la couche d'actionnement, couche à élution médicamenteuse, et le déclencheur thermosensible. (B) Image SEM montrant des theragrippers à côté de la pointe d'une aiguille hypodermique de calibre 22. Les theragrippers sont suffisamment petits pour passer en toute sécurité dans le tractus gastro-intestinal sans provoquer d'obstruction gastrique. (C) Image SEM montrant un seul 250 um, comme le theragripper fabriqué avec le patch de chitosane encapsulé au centre et la couche de déclenchement de cire de paraffine sur les charnières. (D) High-resolution SEM image showing the surface morphology of the chitosan patch at the center of the theragripper. The patch has pores less than 100 nm in size. (E) Release characteristics of ketorolac (KT) from theragrippers of four different sizes. (F) Plot showing the relative scaling of the drug loading capacity of theragrippers of different sizes. The entire loaded drug gets released over a period of 24 hours. While the 250-μm theragrippers were used for our in vivo experiments in rats, larger 1.5-mm theragrippers can be loaded with about 100 times more drug, for use in larger animal models and humans. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abb4133
Ex vivo and in vivo attachment followed by systemic drug delivery
The team performed ex vivo (experiments on tissue conducted externally in a laboratory) theragripper attachment studies using rat colon tissue and visualized surface penetration using scanning electron microscopy (SEM). During in vivo experiments in rats, Ghosh et al. deployed thousands of grippers in a single shot by using a pneumatic microfluidic controller (PMC). The team delivered the drug deploying theragrippers intrarectally via a pneumatic delivery system to jugular vein cannulated rats. The rat colon appeared normal at the sites of attachment, indicating the absence of tissue damage or inflammation. The team also conducted similar experiments with a porcine (pig) model to understand theragrippers as a resident device in the upper GI tract. During these investigations, the device transited through the esophagus in less than a minute and remained attached to the colon for up to a day. All experiments demonstrated the safe elimination of the grippers from the body through natural mucosal turnover. Each theragripper contained approximately 23 nanograms of ketorolac for sustained drug concentrations and showed delayed clearance compared with pristine ketorolac.
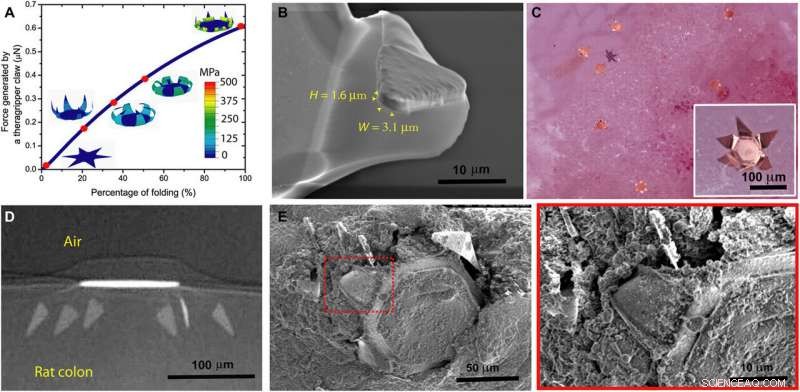
Theragrippers can apply sufficient force to penetrate the mucosa. (A) Plot of the force generated by a theragripper as a function of the percentage of folding, generated by FEM. Each claw of the theragripper can generate a maximum force of around 0.6 μN per hinge. Insets show the simulated configurations at different stages of the folding process marked by red dots. The colors in the legend indicate the magnitude of the von Mises stress in the gripper. (B) Close-up SEM image of the tip of a theragripper, showing the cross section of the tip having a width (W) of approximately 3.1 μm and a height (H) of 1.6 μm. To estimate the pressure exerted by this tip as the gripper actuates, we used the Hertz contact mechanics model and assumed the tip to be a sphere of diameter 1.6 to 3.1 μm. (C) Ex vivo experiment showing many theragrippers latching onto the colon of a rat. The inset shows the bright-field zoomed-in image of a single theragripper. (D) μ-CT image of the cross section of a theragripper penetrating into the colon ex vivo. (E) SEM image of a theragripper latching onto the colon mucosa ex vivo. (F) Zoomed-in image of the red outlined region in (E), showing the penetration of the claw into the colon tissue. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abb4133
De cette façon, Arijit Ghosh and colleagues developed a versatile platform of thermoresponsive theragrippers for drug dispersion in smaller conduits within the body. The team markedly improved the performance by altering the geometry, hydrogel matrix and drug formulation to observe drug release and the retention of grippers in the colon for 24 hours. Due to the thermoresponsive nature of theragrippers, the team will need to refrigerate the devices for immediate and long-term storage. They conducted proof-of-concept studies with the model drug ketorolac, which showed an increased half-life of almost 12 hours, the concept can be extended to other drugs. The new and versatile theragripper drug delivery system is based on self-latching in live animals and presents a new paradigm in drug administration.
© 2020 Réseau Science X