Crédit :Wiley
Comment éviter l'élimination des agents thérapeutiques de la circulation sanguine ou leur dégradation enzymatique précoce lors de l'administration systémique ? Des scientifiques chinois ont développé une nouvelle méthode pour lier un traitement anticancéreux établi, floxuridine, avec de l'albumine sérique naturelle pour son transport et son administration aux cellules cancéreuses cibles. Dans la revue Angewandte Chemie , les auteurs démontrent la synthèse automatisée d'un polymère de floxuridine conjugué, son transport et sa livraison réussis, et son efficacité dans l'arrêt de la croissance tumorale.
Comment faire parvenir un médicament à sa cible ? Malgré de nombreux progrès dans la recherche sur les nanotransporteurs, le problème persiste, notamment en cancérologie. Pendant le transport dans la circulation sanguine, les médicaments anticancéreux peuvent interférer avec les cellules saines, ou ils peuvent être dégradés par des enzymes ou éliminés du corps avant de pénétrer dans le tissu tumoral. Envisager un système de portage naturel et sûr, Weihong Tan et ses collègues de l'Université du Hunan, Chine, et l'Université de Floride, ETATS-UNIS, a choisi l'albumine sérique endogène comme nanotransporteur possible. Pour assurer la liaison de l'antimétabolite floxuridine à l'albumine, ils ont dû le modifier.
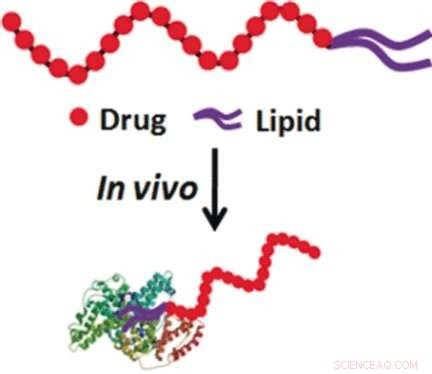
La floxuridine est un nucléoside pyrimidique fluoré et un antimétabolite, qui inhibe les enzymes de la synthèse de l'ADN. Son oligomère, un oligonucléotide de 10 unités, est encore plus efficace et est activement internalisé dans la cellule. Pour le rendre transportable par la sérumalbumine, Le professeur Tan et son groupe ont décidé de doter l'oligonucléotide de chaînes alkyles hydrophobes en tant que lieur. Cela était nécessaire car l'albumine transporte naturellement des molécules lipophiles telles que les lipides et le cholestérol, mais pas d'oligonucléotides chargés négativement.
La synthèse de l'oligonucléotide floxuridine conjugué à chaîne alkyle contenant 20 unités (LFU20) s'est déroulée sur un synthétiseur d'ADN. Les auteurs ont testé le composé pour son interaction avec l'albumine sérique, internalisation cellulaire, le transport dans la circulation sanguine chez les souris implantées dans une tumeur, et la prolifération tumorale. Ils ont observé que bien qu'une grande partie de la drogue quitte encore le corps, une proportion beaucoup plus élevée que dans le groupe témoin accumulée dans la tumeur. Là, le médicament a été internalisé dans les cellules. L'« effet de perméabilité et de rétention améliorés » a dirigé l'accumulation, un effet bien établi dans la recherche sur les tumeurs. Dans les cellules, les lysosomes absorbent le médicament, et les enzymes libèrent la structure antimétabolique de la floxuridine, notent les auteurs.
Les scientifiques ont rapporté que la prolifération tumorale a été stoppée par le composé lipidique conjugué, alors que le médicament FU20 libre sans ancre lipidique n'a pas pu arrêter la croissance tumorale. Cela signifie que LFU20 semble "faire de l'auto-stop" avec l'albumine pour trouver les cellules cibles et s'y accumuler. Les auteurs ont également souligné que le médicament est facilement préparé par synthèse automatisée, et la queue lipidique hydrophobe, qui assure l'affinité à l'albumine, peuvent être facilement incorporés à l'extrémité 5' de l'oligonucléotide. Faire de l'auto-stop avec un potentiel de meurtre est payant dans la livraison de drogue.