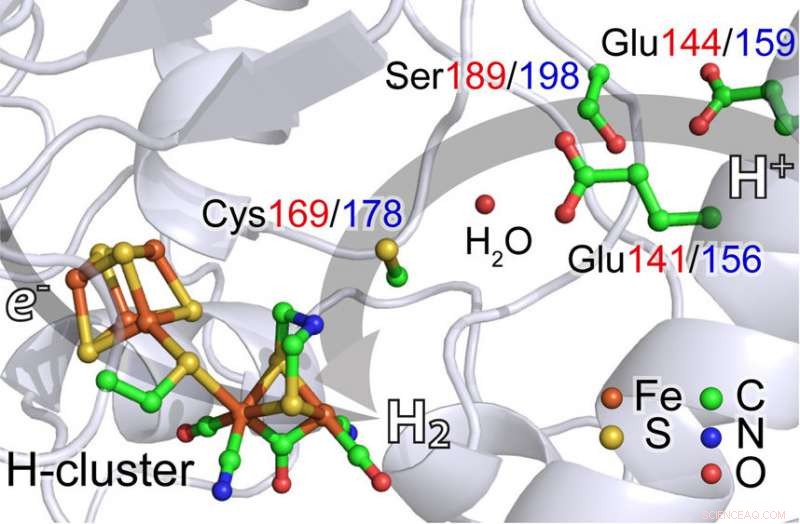
En utilisant une technique nouvellement développée et l'une des sources de rayons X les plus avancées au monde, chercheurs du Japon, L'Allemagne et les États-Unis étudient les enzymes qui peuvent produire de l'hydrogène gazeux. Comprendre ces réactions pourrait être important pour développer une économie de carburant propre alimentée par l'hydrogène. Crédit :Cramer Lab, UC Davis
En utilisant une technique nouvellement développée, chercheurs du Japon, L'Allemagne et les États-Unis ont identifié une étape clé dans la production d'hydrogène gazeux par une enzyme bactérienne. Comprendre ces réactions pourrait être important pour développer une économie de carburant propre alimentée par l'hydrogène.
L'équipe a étudié les hydrogénases - des enzymes qui catalysent la production d'hydrogène à partir de deux organismes largement répandus : Chlamydomonas reinhardtii , une algue unicellulaire et Desulfovibrio desulfuricans, une bactérie.
Dans les deux cas, leurs enzymes hydrogénases ont un site actif avec deux atomes de fer.
« Parmi les hydrogénases, L'hydrogénase [FeFe] a le taux de renouvellement le plus élevé (taux de production d'hydrogène moléculaire) et a donc un rôle potentiel dans la future économie de l'hydrogène, soit par une utilisation directe, soit par un complexe synthétique ayant un centre réactionnel similaire, " a déclaré le professeur Stephen P. Cramer du département de chimie de l'UC Davis et co-auteur de l'article avec les étudiants diplômés Cindy C. Pham (co-premier auteur) et Nakul Mishra et le scientifique du projet Hongxin Wang dans le même département.
Les chercheurs ont utilisé une technique appelée spectroscopie vibrationnelle par résonance nucléaire (NRVS) pour suivre les structures vibrationnelles et l'activité d'analyse des atomes de fer dans l'enzyme. Le NRVS nécessite un équipement spécial, et n'est actuellement disponible que sur quatre sites dans le monde :le synchrotron SPring-8 à Hyogo, Japon, où cette étude a été réalisée; la source avancée de photons du laboratoire national d'Argonne, Illinois; l'Installation Européenne de Rayonnement Synchrotron de Grenoble, La France; et Petra-III à Hambourg, Allemagne.
L'algue verte unicellulaire Chlamydomonas reinhardtii possède une enzyme à base de fer qui peut générer de l'hydrogène gazeux. Crédit :JGI
En utilisant le NRVS, l'équipe a pu montrer que les atomes de fer forment brièvement un hydrure (fer-hydrogène) avant de libérer de l'hydrogène moléculaire (H2). C'est la première expérience réussie de ce type sur les hydrogénases [FeFe] naturelles, a dit Wang.
"Le succès de cette recherche est dû à la large collaboration entre les biochimistes, spectroscopistes, physiciens expérimentateurs et théoriciens, ", a déclaré Wang. "Cela commence un voyage pour rechercher des informations spécifiques au fer pour tous les intermédiaires de l'hydrogénase [FeFe] à l'avenir."
Auteurs supplémentaires sur le papier, publié en ligne dans le Journal de l'American Chemical Society sont :Vladimir Pelmenschikov, Université technique de Berlin, Allemagne; James Birrell, Constance Sommer, Edward Reijerse et Wolfgang Lubitz, Institut Max Planck pour la conversion chimique de l'énergie, Mulheim an der Ruhr, Allemagne; Casseday Richers et Thomas Rauchfuss, Université de l'Illinois ; Kenji Tamasaku et Yoshitaka Yoda, PRINTEMPS-8, Hyogo, Japon. Le travail a été financé en partie par des subventions des National Institutes of Health et de la Max Planck Society.