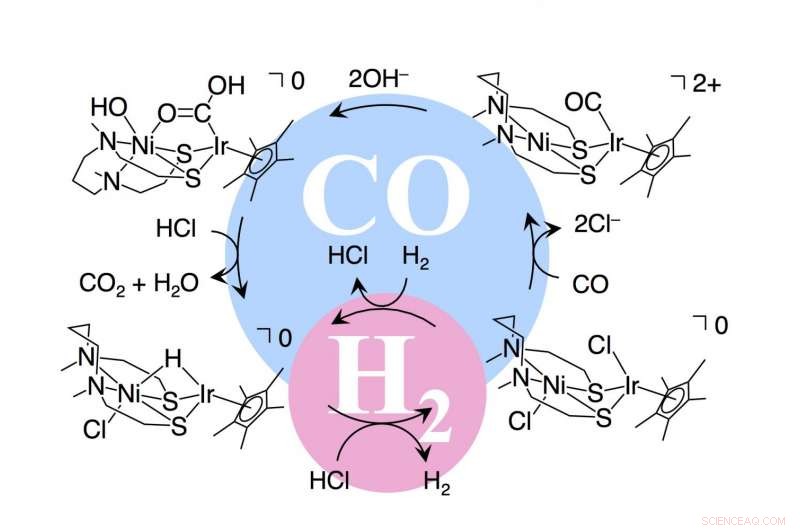
Mécanisme de réaction avec un catalyseur pour piles à combustible utilisant l'hydrogène et le monoxyde de carbone comme combustibles. Crédit :Université de Kyushu
La demande de sources de combustibles respectueux de l'environnement augmente à mesure que l'objectif de réduire la dépendance aux combustibles fossiles devient communément reconnu. L'hydrogène représente une source de carburant durable possible lorsqu'il est produit à partir d'eau et brûlé avec de l'oxygène, car seule de l'eau est libérée en tant que sous-produit. L'oxydation de l'hydrogène pour libérer de l'énergie et de l'eau à l'aide de piles à combustible contenant des catalyseurs fait l'objet de recherches intensives. Cependant, les catalyseurs utilisés dans l'oxydation de l'hydrogène souffrent généralement d'empoisonnement par le monoxyde de carbone, qui est présent en tant que contaminant dans l'hydrogène gazeux commercial. Ainsi, la capacité d'oxyder à la fois l'hydrogène et le monoxyde de carbone dans le même système de réaction est une perspective intéressante pour éviter l'empoisonnement du catalyseur et augmenter l'efficacité de la production d'énergie à partir de l'hydrogène.
Une collaboration dirigée par l'Université de Kyushu a récemment développé un catalyseur qui peut oxyder à la fois l'hydrogène et le monoxyde de carbone en fonction du pH du système de réaction. Le catalyseur imite le comportement de deux enzymes :l'hydrogénase en milieu acide (pH 4-7) et le monoxyde de carbone déshydrogénase en milieu basique (pH 7-10). Le catalyseur est un complexe soluble dans l'eau contenant des atomes métalliques de nickel et d'iridium avec une structure "papillon" unique. Les chercheurs ont étudié la capacité de leur catalyseur à oxyder l'hydrogène et le monoxyde de carbone dans un mélange 1:1. Surtout, ils ont pu isoler divers intermédiaires dans les processus d'oxydation pour confirmer les mécanismes d'oxydation de l'hydrogène et du monoxyde de carbone par le catalyseur.
"Nous avons découvert que le catalyseur réagissait avec l'hydrogène pour former un complexe d'hydrure dans des conditions acides, " dit le premier auteur, le professeur Seiji Ogo, Faculté d'ingénierie/Institut international de recherche sur l'énergie neutre en carbone (WPI-I2CNER), Université de Kyushu. "En outre, le catalyseur facilement coordonné avec le monoxyde de carbone, qui a été oxydé en dioxyde de carbone dans des conditions basiques."
L'équipe a ensuite étudié la résistance de leur catalyseur à l'empoisonnement par le monoxyde de carbone dans un prototype de pile à combustible utilisant des gaz d'alimentation d'hydrogène, monoxyde de carbone, et un mélange 1:1 des deux. La densité de puissance de la pile à combustible contenant le catalyseur dépendait du pH du système et de la composition du gaz d'alimentation. L'oxydation de l'hydrogène par le catalyseur était facilitée à pH bas (conditions acides) et l'oxydation du monoxyde de carbone était plus rapide à pH élevé (conditions basiques); ces tendances correspondent bien au comportement observé pour les enzymes apparentées.
"La capacité de notre catalyseur à utiliser à la fois l'hydrogène et le monoxyde de carbone comme sources d'énergie représente une avancée importante dans la technologie de l'hydrogène, " explique Ogo.
Il est prévu que les catalyseurs pour l'oxydation de l'hydrogène qui peuvent résister à l'empoisonnement au monoxyde de carbone permettront le développement de piles à combustible à hydrogène avec des performances améliorées, représentant une nouvelle étape sur la voie de l'objectif ultime d'une société durable.