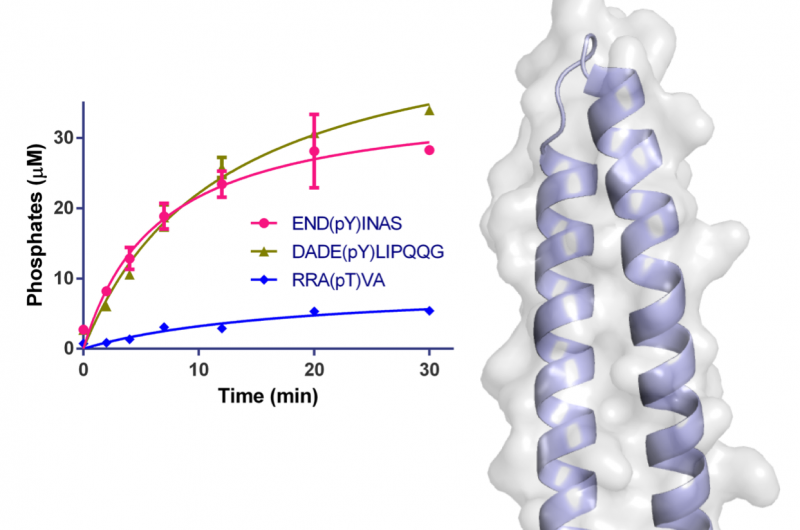
Figure 1 :Structure de WipA en dessin animé et représentation de surface semi-transparente. Le domaine phosphatase est représenté en rouge-vert et le coiled-coil attaché en bleu clair. Les résidus impliqués dans la catalyse sont représentés sous forme de bâtonnets autour des ions Mn2+ et phosphate. La surface est représentée en gris clair. Le graphique en médaillon affiche la déphosphorylation au cours du temps de peptides spécifiques en utilisant 20 nM de WipA. Crédit :Source de lumière diamant
Des scientifiques basés à Londres ont élucidé la structure d'un grand fragment d'une protéine bactérienne, connu sous le nom de WipA, qui est sécrétée par Legionella pneumophila. L'oeuvre, récemment publié dans le Journal de chimie biologique , ont montré que la protéine possédait des caractéristiques fascinantes qui donnaient des informations précieuses sur son mécanisme d'action.
La bactérie, L. pneumophila, provoque une forme grave de pneumonie connue sous le nom de maladie du légionnaire. La pathogénicité de cette bactérie dépend de la sécrétion de plus de 300 protéines effectrices dans l'hôte. Un tel effecteur, WipA, a attiré l'attention pour sa dépendance à un complexe chaperon (nécessaire pour assurer la fonctionnalité des protéines) pour sa sécrétion et son rôle inconnu dans la pathogénicité.
Deux des lignes de lumière de cristallographie macromoléculaire (MX) (I02 et I04) à Diamond Light Source ont été utilisées pour lancer l'étude et résoudre la structure cristalline d'un grand fragment de WipA. La structure a montré que la protéine possédait un pli sérine/thréonine phosphatase qui ciblait de manière surprenante les peptides tyrosine-phosphorylés. En outre, il a été émis l'hypothèse que WipA pourrait passer d'un état homo-dimérique à un état hétéro-dimérique pour interagir avec une cible hôte phosphorylée sur tyrosine. Les découvertes aideront à clarifier les mécanismes moléculaires qui sous-tendent la pathogénicité de Legionella et pourraient aider au développement d'inhibiteurs.
Vapeur infectée
La maladie du légionnaire peut être mortelle parmi les membres vulnérables d'une population, et est particulièrement dangereux lors des épidémies hospitalières. L'une des principales sources d'infection à Legionella est la vapeur d'eau dans les systèmes de climatisation, chaudières, bains et douches chaudes.
Une fois qu'un hôte respire la vapeur infectée, les bactéries pénètrent dans les poumons et recherchent les globules blancs, connu sous le nom de macrophages. Les bactéries sont englouties par les macrophages, mais au lieu d'être tué par eux, les bactéries utilisent intelligemment un système de sécrétion de type IVb pour sécréter une vaste gamme de protéines effectrices dans la cellule hôte afin de détourner la machinerie cellulaire de l'hôte et d'assurer la survie bactérienne.
Dépistage approfondi
Le fragment majeur de WipA a été cristallisé avec succès en supprimant les deux extrémités de la séquence qui prédisaient les régions non structurées. Les cristaux ont été initialement analysés sur les lignes de lumière I02 et I04 de Diamond, tandis que les travaux ont été achevés sur la ligne de lumière PetraIII P13 du Laboratoire européen de biologie moléculaire à Hambourg.
Au Diamant, la ligne de lumière Microfocus MX (I04) a été utilisée pour le criblage des cristaux et I02 a été utilisée pour collecter les données de diffraction. Le Dr Nikos Pinotsis est chercheur post-doctoral en biologie structurale et moléculaire dans le laboratoire du professeur Gabriel Waksman à l'Institut de biologie structurale et moléculaire de Birkbeck/UCL et co-investigateur de l'étude. Il a expliqué leur approche, "Même si la taille des cristaux WipA était suffisante pour les expériences de diffraction monocristalline, la plupart présentaient des réseaux multiples et/ou désordonnés, par conséquent, un dépistage approfondi était essentiel pour acquérir avec succès des données de haute résolution et de qualité. Nous avons optimisé nos stratégies de collecte de données à une taille de faisceau qui correspondait suffisamment à la plus courte des dimensions du cristal et optimisé le faisceau en maximisant le faisceau et le temps d'exposition tout en minimisant les dommages causés par les rayonnements."
Premier de sa catégorie
La structure du fragment WipA présentait un pli de phosphatase monté sur une épingle à cheveux hélicoïdale, qui était le premier de sa catégorie. Le noyau de cette structure ressemblait à une sérine/thréonine protéine phosphatase, mais des expériences biochimiques ont montré de manière inattendue qu'il avait une préférence pour les substrats tyrosine-phosphorylés. Cette observation surprenante n'avait été relevée qu'une seule fois parmi plusieurs centaines de phosphatases similaires.
Le Dr Pinotsis a expliqué la pertinence des résultats :« Une fois que la cible hôte pour la déphosphorylation par WipA est connue, des inhibiteurs pourraient être conçus pour inhiber cette interaction. Bien qu'il soit possible que ces découvertes conduisent à la conception d'antibactériens, ils contribuent principalement à une compréhension générale de la survie et de la pathogénicité d'une bactérie, ce qui est une première étape très importante pour établir des traitements durables contre les infections. »
L'équipe prévoit d'identifier la cible WipA dans les cellules hôtes et continuera d'explorer d'autres interactions protéine-protéine pour fournir une vue plus complète du mécanisme d'infection de Legionella.