Le noyau de chacune de vos cellules contient toute l’information génétique (le génome) nécessaire à la construction de chaque type de cellule et de protéine dans tout votre corps. Comme une bibliothèque complexe dans un espace minuscule 50 fois plus petit que la largeur d'un cheveu humain, les gènes sont organisés en régions précises en trois dimensions.
En plus du génome, le noyau contient des structures appelées corps nucléaires qui contiennent de fortes concentrations de protéines et d'acides nucléiques spécifiques. Le rôle des corps nucléaires reste cependant un mystère depuis près d’un siècle. Une nouvelle étude du laboratoire de Mitch Guttman, professeur de biologie de Caltech, montre que ces corps nucléaires peuvent agir comme des usines miniatures pour permettre une production efficace d'ARNm.
L’épissage de l’ARNm est une partie fondamentale du processus qui se produit lorsque les instructions codées de l’ADN sont transformées en une protéine fonctionnelle. Une fois qu'un gène est transcrit de l'ADN en ARN, les sections étrangères (appelées introns) doivent être supprimées, un processus facilité par les enzymes d'épissage.
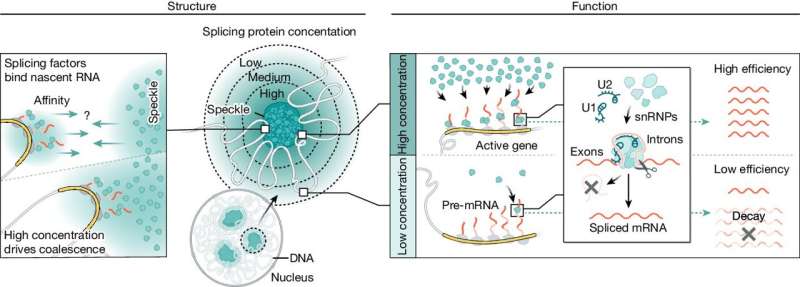
Dans la nouvelle étude, les chercheurs de Caltech ont examiné un type particulier de corps nucléaire, appelé tache nucléaire, qui contient de fortes concentrations d'enzymes d'épissage. L'équipe de Guttman a découvert que le génome se déplace physiquement de sorte que les gènes hautement transcrits se trouvent à proximité des taches, permettant un épissage plus efficace.
Les résultats ont des implications à la fois sur la compréhension scientifique fondamentale de la relation entre la structure nucléaire et la fonction cellulaire et, à terme, sur le développement futur de thérapies pour les maladies dans lesquelles l'épissage de l'ARNm est affecté, y compris pour les maladies neurodégénératives comme la SLA.
L'article décrivant les résultats a été publié dans la revue Nature. le 8 mai. Il est intitulé "L'organisation du génome autour des taches nucléaires stimule l'efficacité de l'épissage des ARNm."
Depuis une décennie, les chercheurs du laboratoire Guttman étudient l’organisation spatiale du noyau, autrement dit l’agencement de la bibliothèque. Les structures 3D dans lesquelles l'ADN est ordonné rendent certains gènes plus ou moins accessibles à la machinerie qui convertit l'ADN en ARNm, et la nouvelle étude montre que la structure physique du génome relie la transcription au processus d'épissage.
Une cellule musculaire, par exemple, déplacera son génome de sorte que les gènes hautement transcrits pour l'activité musculaire se trouvent à proximité physique des taches nucléaires, où des concentrations élevées d'enzymes d'épissage rendent l'épissage de l'ARN particulièrement efficace. Une cellule neuronale, quant à elle, réorientera son génome dans l'espace afin que les gènes nécessaires à la production de cellules spécialisées dans la fonction neurologique soient plus proches des taches.
"Nous savons que l'épissage dépend des enzymes, et toute mutation qui perturbe la concentration des enzymes a des effets dramatiques", explique Prashant Bhat, chercheur postdoctoral associé en biologie et en génie biologique et premier auteur de l'étude.
"Auparavant, nous avions tendance à considérer l'épissage comme une constante :vous créez un pré-ARNm, vous l'épissez. Nous savons maintenant que l'organisation physique du noyau fait une grande différence dans l'efficacité de l'épissage et, par extension, d'autres processus. ."
De nombreuses maladies, notamment les maladies neurodégénératives et le cancer, ont une caractéristique commune :un épissage dysfonctionnel de l’ARN. Bien qu'on ne sache pas si un épissage inapproprié est une cause principale de maladie ou un effet, le processus d'épissage est en fin de compte une cible thérapeutique prometteuse.
Par exemple, les maladies dans lesquelles un nombre insuffisant de protéines sont produites (appelées maladies d'haplo-insuffisance) pourraient être traitées en repositionnant la copie normale du gène de cette protéine près des taches nucléaires pour stimuler l'épissage et restaurer des niveaux de protéines sains.
Plus d'informations : Prashant Bhat et al, L'organisation du génome autour des taches nucléaires stimule l'efficacité de l'épissage de l'ARNm, Nature (2024). DOI :10.1038/s41586-024-07429-6
Informations sur le journal : Nature
Fourni par l'Institut de technologie de Californie