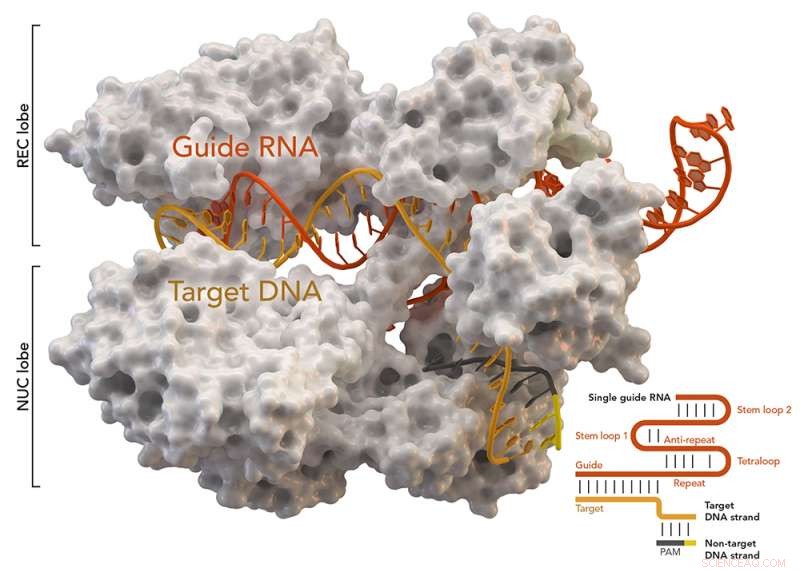
Protéine Cas9 associée à CRISPR (blanche) de Staphylococcus aureus basée sur la base de données de protéines ID 5AXW. Crédit :Thomas Splettstoesser (Wikipédia, CC BY-SA 4.0)
(Phys.org) - Une équipe de chercheurs de l'Université de Californie et de l'Université de Tokyo a trouvé un moyen d'utiliser la technique d'édition de gènes CRISPR qui ne repose pas sur un virus pour l'administration. Dans leur article publié dans la revue Nature Génie Biomédical , le groupe décrit la nouvelle technique, son bon fonctionnement et les améliorations qui doivent être apportées pour en faire un outil d'édition de gènes viable.
CRISPR-Cas9 a fait l'actualité ces derniers temps car il permet aux chercheurs de modifier directement les gènes, soit en désactivant les parties indésirables, soit en les remplaçant complètement. Mais malgré de nombreuses réussites, la technique souffre encore d'un important déficit qui l'empêche d'être utilisée comme un véritable outil médical :elle commet parfois des erreurs. Ces erreurs peuvent causer de petits ou de gros problèmes à un hôte en fonction de ce qui ne va pas. Des recherches antérieures ont suggéré que la majorité des erreurs sont dues à des problèmes de livraison, ce qui signifie qu'un remplacement de la partie virale de la technique est nécessaire. Dans ce nouvel effort, les chercheurs rapportent qu'ils ont découvert un tel remplacement, et cela a si bien fonctionné qu'il a pu réparer une mutation génétique dans un modèle murin de dystrophie musculaire de Duchenne. L'équipe a nommé la nouvelle technique CRISPR-Gold, parce qu'une nanoparticule d'or a été utilisée pour délivrer les molécules d'édition de gènes au lieu d'un virus.
Le nouveau package a été créé en modifiant un peu d'ADN pour le faire coller à une nanoparticule d'or, puis à une protéine Cas9 et également à un guide d'ARN. L'emballage était ensuite recouvert d'un polymère qui servait d'enveloppe de confinement, qui déclenchait également l'endocytose (une forme de transport cellulaire) et aidait les molécules à s'échapper des endosomes une fois à l'intérieur des cellules cibles. Les molécules se sont alors mises au travail :le Cas9 a coupé le brin d'ADN cible, l'ARN guide montrait ce qui devait être fait et un brin d'ADN était placé là où une mutation avait existé. Le résultat était un gène exempt d'une mutation qui cause la dystrophie musculaire de Duchenne.
Il y a encore un problème majeur à surmonter avec la technique, cependant, cela ne fonctionne que dans les applications localisées. Idéalement, une masse de paquets serait injectée dans la circulation sanguine permettant la réparation de tous les types cellulaires, tels que les muscles altérés par un gène mutant.
© 2017 Phys.org