Grâce à un éditorial du New York Times de 2013, nous connaissons tous la décision d'Angelina Jolie de subir une double mastectomie préventive pour réduire son risque de développer un futur cancer du sein. Ses commentaires francs ont révélé qu'elle avait à la fois de solides antécédents familiaux de la maladie et, sur la base des résultats des tests génétiques, une forme mutée du gène connu sous le nom de BRCA1, ce qui lui donne 87 pour cent de risque de cancer du sein et 50 pour cent de risque de cancer de l'ovaire [source :Jolie]. Face à cette réalité, qui peut être plus ou moins sévère selon les personnes, elle a choisi d'enlever les deux seins avant que les cellules constituant ses glandes productrices de lait ne se transforment en cellules cancéreuses voyous capables de croissance incontrôlée.
Si la procédure la protège de cette maladie, comme le suggère la probabilité, elle aura beaucoup de gens à remercier :les conseillers génétiques, les chirurgiens, et sa famille, bien sûr, pour n'en nommer que quelques-uns.
Mary-Claire King ne figure peut-être pas sur cette liste. Professeur de sciences du génome et de génétique médicale à l'Université de Washington, King a aidé à démêler la base génétique du cancer du sein héréditaire. Ses travaux ont d'abord conduit à la découverte de BRCA1 en 1994 puis, un an plus tard, au BRCA2. Femmes et hommes, trop, comme il s'avère) qui portent des formes mutées de ces gènes sont beaucoup plus susceptibles de développer un certain nombre de cancers, y compris la poitrine, cancer de l'ovaire et de la prostate.
King elle-même désigne souvent un autre VIP - Paul Broca, un pathologiste français qui a proposé pour la première fois dans les années 1860 que le cancer du sein pourrait être héréditaire. La femme de Broca souffrait d'un cancer du sein précoce, et quand il étudia son arbre généalogique, il a découvert que la maladie pouvait être retracée sur quatre générations. Lorsque King est allé nommer le gène qu'elle avait découvert, elle voulait l'appeler BROCA pour honorer le Français, mais elle n'avait droit qu'à quatre lettres. Le nom final -- BRCA -- abrège " Broca " en signifiant " fr est Californie ncer" et peut-être même Berkeley, Californie, où King a fait ses travaux de doctorat [source :Check].
Nomenclature à part, les gènes BRCA sont une réussite de la génétique moderne, prouver que les biomarqueurs peuvent prédire de manière fiable la prédisposition d'une personne à développer une maladie ou une affection. Il y a une dizaine d'années, porté par le succès du Projet Génome Humain, les avant-gardistes ont promis un temps où les molécules biologiques trouvées dans le corps serviraient d'indicateurs de phénomènes tels que la maladie, infection ou exposition environnementale. Ces signaleurs conduiraient à l'éradication du cancer et d'autres maladies pernicieuses. Mais une chose amusante s'est produite sur le chemin de l'utopie :les biomarqueurs se sont avérés difficiles à identifier. Et quand ils l'étaient, les chercheurs ne pouvaient pas développer des tests suffisamment sensibles ou suffisamment rentables pour en faire des outils de diagnostic précieux.
La communauté médicale a donc salué la découverte des gènes BRCA, et le développement de tests génétiques fiables pour les identifier chez les individus, avec les bras ouverts. Tout cela a conduit au prochain défi :faire en sorte que le public comprenne ce que sont ces gènes.
Contenu
Les seins sont des structures étonnantes. Ils sont si uniques dans le règne animal que leur présence définit un groupe entier d'organismes - le mot "mammifère" vient de "mammaire, " qui lui-même vient de " maman , " le mot latin pour sein, pis ou trayon. Les biologistes classeraient les seins comme glandes exocrines , ou des structures qui sécrètent leurs produits par des conduits vers l'environnement extérieur. Ce n'est pas la même chose que glandes endocrines , qui sécrètent leurs produits directement dans la circulation sanguine.
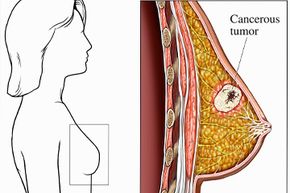
Le produit à base de seins, bien sûr, est le lait. Le lait arrive au monde extérieur par le mamelon, mais il commence sa vie plus profondément dans le sein, dans des amas de cellules appelés alvéoles. Ces amas forment des lobules, qui eux-mêmes créent des structures plus grandes appelées lobes. Comme les alvéoles produisent du lait, le fluide passe à travers des tubes minces - des canaux galactophores - qui mènent à des ouvertures dans le mamelon. Le tissu fibreux et la graisse remplissent les espaces entre les lobules et les canaux, et toute la structure repose sur les muscles pectoraux de la poitrine. Un réseau de vaisseaux lymphatiques et de ganglions entoure tout ce tissu et s'étend vers le haut dans l'aisselle.
Chez de nombreuses femmes, ce tissu fonctionne correctement et ne cause jamais de problèmes. Prochain, bien que, nous allons voir ce qui se passe quand c'est le cas.
Nommer le CancerLes médecins et les oncologues classent les cancers du sein en fonction de l'endroit où ils se développent. Certains cancers prennent naissance dans les cellules qui tapissent le canal mammaire. Ces soi-disant carcinomes canalaires sont le type de cancer du sein le plus courant, survenant chez 70 pour cent des femmes diagnostiquées avec la maladie [source :National Cancer Institute]. Les alvéoles constituant les lobules peuvent également abriter des excroissances cancéreuses. Carcinomes lobulaires sont beaucoup moins fréquents et ne représentent que 1 % des cas de cancer du sein [source :National Cancer Institute]. Certaines femmes ont même un mélange de types de cancer canalaire et lobulaire .
Parfois, les cellules constituant le tissu mammaire peuvent commencer à se développer sans contrôle, évinçant les cellules productrices de lait normales. Alors que ces brutes désinhibées poussent et se bousculent, ils forment une masse de tissu appelée masse ou tumeur. Si la masse reste contenue et n'envahit pas les lobules environnants ou d'autres parties du corps, c'est classé comme bénin. Si, cependant, il continue d'envahir le sein environnant et se propage aux ganglions lymphatiques, il est classé comme malin ou cancéreux.
Les scientifiques savent maintenant que le cancer est causé par des dommages à l'ADN - une mutation - dans les gènes qui régulent la croissance et la division des cellules. De nombreuses mutations surviennent lorsqu'une personne est exposée à certaines conditions environnementales, comme les radiations. Les cellules mammaires ne sont pas à l'abri de ces mutations acquises (par opposition aux mutations héréditaires). En réalité, deux types de cancer du sein surviennent lorsque l'ADN est endommagé par des agents cancérigènes ou des virus environnementaux.
Le premier type affecte la façon dont les hormones, comme les œstrogènes, interagir avec les cellules mammaires. Pendant le cycle menstruel d'une femme, les niveaux d'œstrogènes augmentent dans le sein pour préparer les tissus à produire du lait. Les molécules d'œstrogène se lient aux récepteurs des cellules mammaires, déclencher la prolifération des cellules. Si une femme ne tombe pas enceinte, toutes ces cellules productrices de lait supplémentaires se détériorent et meurent. Parfois, bien que, ce processus de prolifération peut se détraquer si certaines cellules mammaires contiennent de l'ADN endommagé. Lorsque ces cellules compromises reçoivent le signal de l'œstrogène, ils se multiplient comme il se doit, mais ils ne parviennent pas à s'arrêter et ne meurent pas à la fin d'un cycle.
Une autre mutation acquise affecte le gène codant pour une protéine connue sous le nom de récepteur 2 du facteur de croissance épidermique humain , abrégé HER2 . Normalement, Les protéines HER2 à la surface des cellules mammaires répondent aux facteurs de croissance - des substances chimiques qui indiquent à une cellule mammaire comment se développer correctement. Les protéines HER2 reçoivent ces facteurs, puis transférez les instructions à l'intérieur de la cellule. Si l'ADN du gène HER2 est endommagé, cependant, son activité peut atteindre des niveaux dangereux. Il peut produire trop de protéines HER2 et, par conséquent, provoquer une croissance incontrôlée des cellules mammaires.
Ni les cancers œstrogène-positifs ni HER2-positifs ne peuvent être transmis à d'autres membres de la famille car les mutations n'affectent que les cellules mammaires. Ce n'est pas le cas avec le cancer du sein héréditaire. Dans cette forme de maladie, une mutation est transportée dans les spermatozoïdes ou les ovules d'un parent et transmise, à la fécondation, à sa progéniture. Ces mutations apparaissent alors dans chaque cellule du corps et prédisposent la personne à développer un cancer. Les scientifiques ont découvert plusieurs gènes liés au cancer du sein héréditaire, y compris l'acronyme cauchemars p53, PTEN/MMAC1, CHEK2 et guichet automatique. Mais les gènes BRCA sont les plus connus et peut-être les plus étudiés. Dans la section suivante, nous allons examiner de plus près l'arbre généalogique des gènes BRCA.
Merci à Watson, Crick et des milliers d'autres, nous en savons beaucoup sur les bases chimiques de l'hérédité. Au cas où vous l'auriez oublié ou bloqué de votre mémoire, rappelons que le noyau d'une cellule humaine contient des chromosomes - les structures filiformes portant toute notre information génétique. Les cellules humaines ont 23 paires de chromosomes, pour un total de 46. Chaque chromosome est constitué d'une double hélice d'ADN portant une séquence linéaire de gènes, enroulé autour de protéines appelées histones. Un seul gène est une séquence distincte de nucléotides, les éléments constitutifs de l'ADN, qui code pour une protéine correspondante.
Alors que les scientifiques se penchaient sur le génome humain, ils ont remarqué que certains gènes partageaient certaines caractéristiques. Ils portaient soit une séquence similaire de nucléotides, ou il s'agissait de gènes dissemblables qui produisaient des protéines capables de participer au même processus cellulaire. Ils ont regroupé ces gènes en familles, puis ont utilisé le système de classification pour prédire la fonction des gènes nouvellement identifiés en fonction de leurs similitudes avec des gènes connus.
Il existe deux gènes BRCA - BRCA1 et BRCA2 - et chacun appartient à une famille différente. BRCA1 appartient à la famille de gènes RNF, qui codent pour des protéines connues sous le nom de protéines à doigt de zinc de type RING. Ces protéines sont ainsi nommées parce que la molécule de protéine a des régions qui se replient autour d'un ion zinc et parce que la forme résultante d'une telle région ressemble à un doigt. La forme unique des protéines à doigt de zinc de type RING leur permet de se lier facilement à d'autres molécules, en particulier les protéines et les acides nucléiques. Une fois qu'ils sont liés à une autre molécule, ils effectuent une action enzymatique qui aide une cellule à maintenir un environnement stable. Certaines de ces activités comprennent la croissance et la division cellulaires, transduction du signal, dégradation des protéines et, comme nous le verrons dans la section suivante, suppression tumorale.
Les gènes BRCA2 appartiennent à la famille des gènes FANC. Les gènes de ce groupe produisent un complexe de protéines qui participent à un processus connu sous le nom de voie de l'anémie de Fanconi (AF). Cette voie fonctionne principalement sur la localisation et la réparation des dommages à l'ADN. En particulier, les protéines ciblent des sections d'ADN où les brins opposés de la double hélice ne sont pas correctement liés. Quand ils trouvent une telle zone, les protéines FANC se lient à l'ADN et reconstruisent les liaisons croisées, permettant à l'ADN de se répliquer et de fonctionner normalement.
Clairement, les familles de gènes RNF et FANC jouent un rôle important pour nous garder en bonne santé. Si quelque chose interfère avec la fonction de ces gènes, il peut conduire à un certain nombre de maladies. Par exemple, la perturbation des gènes RNF peut conduire à une dystrophie myotonique, qui se caractérise par une fonte et une perte musculaires progressives. La perturbation des gènes FANC peut entraîner, tu l'as deviné, Anémie de Fanconi, qui peut provoquer une insuffisance médullaire, anomalies physiques et anomalies des organes. Et, bien sûr, les deux familles de gènes jouent un rôle dans certains cancers, y compris le cancer du sein.
Suivant, nous examinerons très spécifiquement BRCA1 et BRCA2 pour comprendre comment ils fonctionnent normalement et comment les mutations des gènes conduisent au cancer du sein.
Mary-Claire King a peut-être voulu honorer Paul Broca en donnant son nom à BRCA, mais les généticiens modernes connaissent les gènes par leurs noms officiels :« cancer du sein 1, début précoce" et "cancer du sein 2, début précoce." Vous pouvez également entendre "gènes de susceptibilité au cancer du sein 1 et 2" ou "cancer du sein héréditaire 1 et 2". vous pourriez penser que les deux gènes résident ensemble sur le même chromosome. Ce n'est pas le cas. L'emplacement exact de BRCA1 est 17q21; BRCA2 est 13q12.3. Voici la signification de ces chiffres :
Même si BRCA1 et BRCA2 appartiennent à des familles de gènes différentes, ils produisent tous deux de grosses protéines qui participent à la suppression tumorale lorsqu'ils fonctionnent normalement. La protéine BRCA1 est constituée de 1, 863 acides aminés et BRCA2 de 3, 418 acides aminés [source :van der Groep]. La protéine BRCA1 exerce ses effets de suppression tumorale en collaborant avec un certain nombre d'autres protéines pour réparer les ruptures de l'ADN. Ces complexes protéiques BRCA1 affectent probablement plusieurs processus de réparation de l'ADN, y compris la recombinaison homologue (échange d'une séquence de nucléotides avec un autre brin similaire d'ADN), réparation par excision de nucléotides (couper les bases d'ADN endommagées et en coller de nouvelles) et jonction d'extrémités non homologues (rassembler une cassure double brin). La protéine BRCA2 participe également au contrôle des dommages à l'ADN, mais semble beaucoup plus limité. Les scientifiques pensent que la protéine BRCA2 régule l'activité d'un plus petit nombre de protéines compagnes, y compris RAD51 et PALB2, pour diriger la recombinaison homologue de l'ADN endommagé.
Imaginez maintenant ce qui se passerait si vous supprimiez les gènes BRCA d'une cellule ou jetiez une clé à molette dans leur machinerie moléculaire. Sans leurs protéines associées, plusieurs processus de réparation de l'ADN cesseraient de fonctionner et, heures supplémentaires, car les cellules ont été exposées à des radiations ou à des agents chimiques, de plus en plus de défauts s'accumuleraient. Ces mutations finiraient par rendre les cellules instables et cancéreuses.
C'est exactement ce qui se passe lorsque les gènes BRCA sont compromis. Une mutation de l'un des gènes brouille son manuel d'instructions. Par conséquent, le gène n'a plus la capacité de construire des versions correctes de sa protéine apparentée. La protéine peut être anormalement courte ou ne pas avoir la séquence correcte d'acides aminés. Ces protéines défectueuses ne peuvent plus participer au processus de réparation de l'ADN, ce qui conduit finalement à la prolifération de cellules portant de l'ADN endommagé. Si ces cellules tapissent les canaux galactophores du tissu mammaire, une grosseur ou une tumeur, créé par une masse de cellules anormales, peut s'y développer. En plus du cancer du sein, Les mutations BRCA peuvent également conduire au cancer de l'ovaire, cancer des trompes de Fallope, cancer du pancréas et cancer de la prostate.
Malheureusement, la nature a trouvé de nombreuses façons de perturber les gènes BRCA. À ce jour, les scientifiques en ont identifié plus de 1, 000 mutations du gène BRCA1 et plus de 800 mutations du gène BRCA2 [sources :Genetics Home Reference, Référence à la maison de la génétique]. Et rappelez-vous, ces gènes défectueux peuvent être transmis d'une génération à l'autre, ce qui signifie que les personnes qui héritent de la mutation la portent avec elles toute leur vie. Il est assis dans leurs cellules, passer inaperçu jusqu'à ce qu'un cancer se développe ou jusqu'à ce que quelqu'un prenne des mesures pour empêcher que cela se produise. C'est là qu'interviennent les tests génétiques.
En savoir plus sur les mutations BRCA peut rendre n'importe qui anxieux. Il est facile de penser que vous pourriez être sensible au cancer parce que vous portez l'un des gènes défectueux. En réalité, seulement environ 5 à 10 pour cent de tous les cas de cancer du sein aux États-Unis sont dus à des mutations génétiques héréditaires [source :Susan G. Komen for the Cure]. Cela signifie que presque tous les cancers du sein se développent à la suite de mutations spontanées ou acquises sans rapport avec l'hérédité. La plupart des femmes, donc, ne bénéficieraient pas des tests génétiques.
Comment savez-vous? Les lignes directrices suivantes peuvent vous aider à décider de poursuivre ou non le dépistage des mutations du gène BRCA. Vous devriez envisager de tester si vous répondez à l'un des critères suivants, comme proposé par Susan G. Komen for the Cure, une organisation à but non lucratif dédiée à mettre fin au cancer du sein par la recherche, sensibilisation de la communauté et plaidoyer :
Un simple test peut révéler si la mutation existe ou non dans vos cellules. Dans la plupart des tests, un technicien prélèvera un échantillon de votre sang. Dans d'autres tests, vous utilisez un bain de bouche. Chaque méthode permet à l'installation de test d'obtenir des cellules - et du matériel génétique - de votre corps. Dans un laboratoire, les scientifiques analysent ce matériel pour rechercher des changements dans les gènes BRCA réels ou dans les protéines codées par ces gènes. Le test prend trois ou quatre semaines et peut coûter plusieurs centaines ou plusieurs milliers de dollars.
Si vous recevez un résultat de test positif, alors vous savez que vous avez hérité d'une mutation connue dans BRCA1 ou BRCA2. Et avoir une mutation BRCA augmente considérablement votre risque de cancer - jusqu'à 50 pour cent de développer un cancer du sein à 50 ans et jusqu'à 87 pour cent de développer un cancer du sein à 70 ans [source :Myriad Genetics]. Un conseiller en génétique peut vous aider à évaluer ce risque et à décider de la marche à suivre. Une option, bien sûr, est de maintenir la vigilance lors des mammographies de routine et des examens cliniques des seins, dans le but de détecter précocement un cancer, quand c'est le plus traitable. Une autre option consiste à prendre des médicaments, comme le tamoxifène, pour réduire le risque de développer un cancer. Et, finalement, vous pouvez prendre l'exemple d'Angelina Jolie et opter pour une chirurgie prophylactique - en enlevant autant de tissus sensibles au cancer que possible.
Il n'y a aucune garantie, toutefois. Même avec une double mastectomie préventive, le cancer du sein peut encore se développer si la chirurgie n'a pas réussi à retirer tous les tissus à risque. Et pourtant, cette ère moderne de la médecine génétique a conduit à une véritable révolution dans la détection et le traitement du cancer du sein, c'est pourquoi, depuis 1990, il y a eu une baisse de 33 pour cent de la mortalité par cancer du sein aux États-Unis [source :Susan G. Komen for the Cure].
Gènes BRCA chez les hommesLes hommes développent également un cancer du sein, bien qu'à des taux nettement inférieurs à ceux des femmes. Comme vous pouvez vous y attendre, les gènes BRCA jouent un rôle dans cette forme de la maladie. Les scientifiques pensent maintenant que le cancer du sein chez l'homme est plus fortement lié aux mutations du gène BRCA2. Le même gène défectueux peut également augmenter le risque de cancer de la prostate et du pancréas. Comme pour les femmes, les hommes qui détectent le cancer du sein et commencent le traitement tôt ont plus de chances de survivre à la maladie.
L'histoire du cancer du sein est étonnante à plusieurs niveaux :la science derrière la découverte des gènes BRCA, l'augmentation étonnante du taux de survie et la franchise avec laquelle nous parlons tous maintenant de la maladie. Mais ce qui m'étonne encore plus, c'est la complexité outrancière de notre machinerie cellulaire, avec la compression et la décompression de l'ADN et l'assemblage de complexes protéiques pour garder notre information génétique intacte et fonctionnelle.