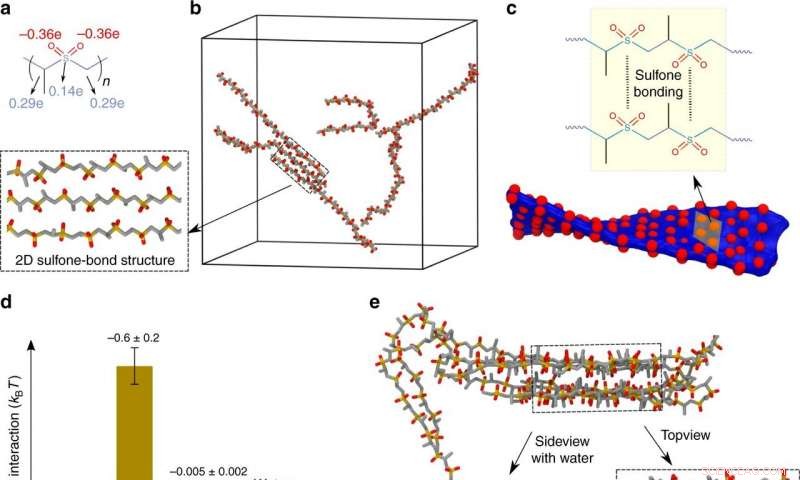
a Structure chimique du PPSU montrant le squelette polymère et les atomes d'oxygène qui portent des charges partielles atomiques positives/négatives (bleu/rouge), respectivement. b Instantané de simulation atomistique montrant un équilibre dissolution-complémentarité dans le DMSO pour six chaînes de PPSU20. L'encart est une superstructure formée par l'auto-complémentarité du PPSU. c Autocomplémentarité PPSU conduisant à une superstructure réversible 2D avec enrichissement en atomes d'oxygène en surface. La formation de superstructures 3D est inhibée dans le DMSO en raison de la forte répulsion entre les couches. d Énergies dipolaires moyennes par paire dipôle-dipôle de sulfone-sulfone et de sulfone-solvant. Les barres d'erreur représentent l'écart type de trois simulations parallèles. e Instantané de simulation atomistique montrant la formation d'une superstructure 3D grâce au regroupement de PPSU dans l'eau. Encart montrant la superstructure 3D avec ou sans molécules d'eau. Crédit: Communication Nature (2020). DOI :10.1038/s41467-020-18657-5
Des chercheurs de la Northwestern University jettent un filet pour les nanoparticules.
L'équipe a découvert une nouvelle, procédé rapide de fabrication de nanoparticules à partir d'un simple, polymère auto-assemblant. La nouvelle méthode offre de nouvelles possibilités pour diverses applications, y compris la purification de l'eau, des diagnostics et des formulations vaccinales à génération rapide, qui nécessitent généralement que de nombreux types de molécules différents soient capturés ou délivrés en même temps.
En utilisant un filet de polymère qui s'effondre en hydrogels nanométriques (ou nanogels), la méthode capture efficacement plus de 95% des protéines, Médicaments à base d'ADN ou de petites molécules, seuls ou en combinaison. Par comparaison, l'efficacité de chargement est généralement comprise entre 5% et 20% pour les autres systèmes de distribution de nanoparticules.
"Nous utilisons un polymère qui forme un large filet à travers une solution aqueuse, " a déclaré Evan A. Scott de Northwestern, qui a dirigé l'étude. « Ensuite, nous induisons l'effondrement du filet. Il recueille tout ce qui se trouve dans la solution, piégeant des agents thérapeutiques à l'intérieur de véhicules d'administration de nanogel avec une très grande efficacité. »
"Cela fonctionne comme un filet de pêche, qui s'étale d'abord en raison de la répulsion électrostatique, puis se rétrécit lors de l'hydratation pour piéger les «poissons, '" a ajouté Fanfan Du, un stagiaire postdoctoral dans le laboratoire de Scott.
L'article a été publié la semaine dernière (29 septembre) dans la revue Communication Nature .
Scott est professeur Kay Davis de génie biomédical à la McCormick School of Engineering de Northwestern. Les professeurs du nord-ouest Monica Olvera de la Cruz et Vinayak Dravid ont co-écrit l'article.
Molécules trouvées dans la nature, tels que l'ADN et les peptides, peuvent rapidement s'auto-assembler et s'organiser en diverses structures. Imitant ce processus en utilisant des systèmes polymères fabriqués par l'homme, cependant, est resté limité. Les processus précédemment développés pour les systèmes d'administration de médicaments à assemblage automatique prennent du temps, à forte intensité de main-d'œuvre et difficile à mettre à l'échelle. Les processus ont également tendance à être terriblement inefficaces, aboutissant à une petite fraction du médicament qui le rend réellement à l'intérieur du système d'administration.
« L'application clinique des nanoparticules auto-assemblées a été limitée par des difficultés d'évolutivité et de chargement de thérapies volumineuses ou multiples, surtout les protéines, ", a déclaré Scott. "Nous présentons un mécanisme hautement évolutif qui peut charger de manière stable presque n'importe quelle molécule thérapeutique avec une efficacité élevée."
L'équipe de Scott a réussi en utilisant un homopolymère de polypropylène sulfone (PPSU), qui est très soluble dans une solution de diméthylsulfoxyde (DMSO), mais forme des agrégats électrostatiques et hydrophiles dans l'eau. Les agrégats sont amphiphiles, ce qui les amène à s'assembler en réseaux et finalement à s'effondrer en gels.
"Ajouter plus d'eau provoque l'effondrement du réseau, conduisant à la formation de nanogels, " Du dit. " La manière dont l'eau est ajoutée affecte la formation de la chaîne PPSU, qui modifie la taille et la structure des nanogels."
Des simulations atomiques, réalisées par Baofu Qiao dans le groupe Olvera de la Cruz, ont confirmé que les nanostructures étaient stabilisées par une faible liaison sulfone-sulfone. À l'aide de simulations à gros grains réalisées par le boursier postdoctoral Northwestern Trung Dac Nguyen, les chercheurs ont observé les structures nanonet. Cela ouvre une nouvelle voie pour l'assemblage de matériaux mous au moyen d'une liaison sulfone-sulfone.
En plus des applications d'administration de médicaments, les chercheurs pensent également que la nouvelle méthode pourrait être utilisée pour la purification de l'eau. Le réseau pourrait s'effondrer pour collecter les contaminants dans l'eau, laissant de l'eau pure derrière.