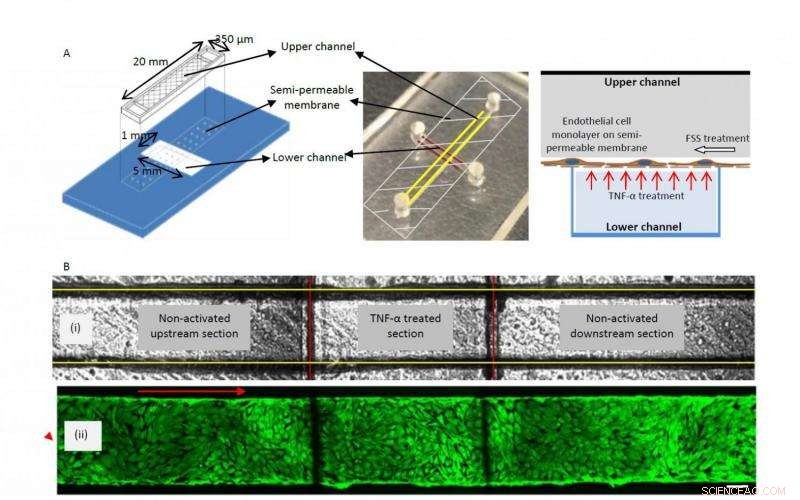
Un schéma graphique (à gauche) et une photographie (au centre) du dispositif bicouche montrant le canal supérieur (marqué de lignes jaunes) et inférieur (marqué de lignes rouges) séparés par une membrane semi-perméable. Le schéma de droite représente la culture d'une monocouche de cellules endothéliales sur la membrane semi-perméable et la manière dont le traitement au TNF-α est effectué à partir du canal inférieur. B, (i) Image en fond clair du canal supérieur (marqué de lignes jaunes) et inférieur (marqué de lignes rouges) définissant le canal amont, Sections activées par le TNF-α et en aval, (ii) Images du cytosquelette F-actine marqué par fluorescence (FITC phalloïdine) de la couche confluente BAOEC alignées pour s'écouler (12 dyne/cm2 FSS pendant 24 heures). Les cellules sont cultivées sur la membrane semi-perméable dans le canal supérieur du dispositif. La flèche indique la direction du flux (barre d'échelle :100 m) Crédit :Yaling Liu
La nanotechnologie a conduit à de meilleures techniques de diagnostic et à des traitements plus efficaces pour une variété de maladies. De minuscules appareils mesurant entre 1 et 100 micromètres (un micromètre équivaut à un millionième de mètre) permettent aux scientifiques d'observer l'activité cellulaire et d'administrer des médicaments à des cellules individuelles. Une percée qui est sur le point de révolutionner la médecine de précision pour le traitement de maladies telles que cancer.
Un obstacle à la réalisation de la promesse de la nanomédecine est l'incapacité d'observer les interactions de cellule à cellule à l'échelle nanométrique dans un environnement qui simule étroitement l'environnement dynamique à l'intérieur du corps. Un environnement micro-fluide qui imite le flux sanguin est essentiel pour apprendre comment les cellules sont endommagées par des maladies et comment elles pourraient récupérer en réponse au traitement.
Aujourd'hui, une équipe de chercheurs de l'Université Lehigh et de l'Université de Pennsylvanie a développé une technique pour observer l'interaction cellule à cellule à l'échelle nanométrique dans des conditions de micro-fluide. Ils ont appliqué avec succès la technique à l'étude de l'inflammation des vaisseaux sanguins, une condition qui ouvre la voie à une maladie cardiaque, la première cause de décès aux États-Unis et dans le monde. Leurs conclusions ont été publiées dans Biomicrofluidique .
"Nous avons montré que notre technique peut être appliquée avec succès à l'étude de l'inflammation et travaillons sur un moyen d'observer et d'intervenir de la même manière dans la réparation des cellules tumorales, " a déclaré Yaling Liu, Professeur agrégé de génie mécanique et de mécanique, Bioingénierie à Lehigh et co-auteur de l'étude.
Les tests de dépistage in vitro actuels sont coûteux, chronophage et relativement médiocre pour prédire les performances des médicaments in vivo. La technologie PharmaFlux est un service de test de micro-dispositifs pour les candidats-médicaments dans des micro-environnements pathologiques simulés. Crédit :Yaling Liu
Imiter le processus de transfert dynamique
Chronique, l'inflammation de bas grade est fortement associée à des cellules endothéliales dysfonctionnelles, qui forment la paroi interne des vaisseaux sanguins. L'apparition de la molécule d'adhésion intercellulaire-1 (ICAM-1) à la surface des cellules endothéliales, essentiel dans la régulation de l'interaction de cellule à cellule dans le cadre de la réponse du système immunitaire du corps, est un signe certain que l'inflammation et la maladie sont présentes. Par conséquent, l'observation de l'activation des cellules endothéliales dans des conditions pathologiques est essentielle pour comprendre comment se développe la maladie cardiaque et comment l'arrêter.
La meilleure façon d'observer ces changements est à l'intérieur du corps. Cependant, c'est très difficile à faire. L'observation de la maladie dans une culture cellulaire statique - en retirant et en cultivant des cellules dans un environnement artificiel tel qu'une boîte de Pétri - est limitée dans sa capacité à représenter avec précision les interactions dynamiques dans des conditions de flux sanguin.
En plus de Liu, l'équipe de Lehigh comprend Linda Lowe-Krentz, Professeur, Sciences Biologiques; H. Daniel Ou-Yang, Professeur, La physique; et Ph.D. étudiant Antoine Thomas. Ils ont collaboré avec Vladimir R. Muzykantov, Professeur de pharmacologie à Penn pour développer un vaisseau sanguin sur une puce afin d'étudier la dynamique d'ICAM-1 à la surface de cellules endothéliales activées dans des conditions pathologiques.
"Nous avons pu imiter et observer le processus de transfert dynamique - ce moment où la molécule d'adhésion intercellulaire-1 nanoparticules recouvertes d'anticorps se lie à la cellule signalant la régulation positive de l'inflammation par les cellules endothéliales - sur une puce. Nous avons également pu contrôler avec précision le flux de fluide, " a déclaré Liu. " Cette méthode fiable et relativement simple simule les conditions dans lesquelles les cellules endothéliales existent dans le corps, permettant d'observer la pathologie cellulaire en temps réel, et analyser les différences dans les réponses des cellules au traitement."
Un environnement idéal pour le dépistage des drogues
Parce que cette nouvelle technologie crée une plate-forme pour se concentrer sur une région malade particulière, Liu et ses collègues pensent qu'il est idéal pour tester de nouveaux traitements contre les maladies.
Les cellules saines existent sur la même puce que les cellules malades, ce qui permet un contrôle plus localisé pour tester un médicament particulier. Cette, combiné avec l'environnement de flux sanguin simulé, permet également aux chercheurs de rassembler un ensemble de données beaucoup plus robuste qu'ils ne le pourraient en utilisant une culture statique.
L'utilisation par l'équipe de nanoparticules recouvertes d'anticorps comme sondes d'imagerie pour évaluer les caractéristiques des cellules est un autre avantage clé de la nouvelle technologie. L'utilisation des sondes à nanoparticules élimine le besoin d'utiliser des anticorps ICAM-1 marqués par des radio-isotopes pour suivre les interactions cellulaires, une technique qui se heurte à des défis réglementaires et de sécurité. C'est aussi très cher.
"Notre système offre un environnement plus sûr, moyen moins coûteux de tester un nouveau médicament dans un environnement qui se rapproche étroitement de l'environnement d'une région malade, " dit Liu.
Un « pont » vers la médecine de précision
La plate-forme innovante de l'équipe fournit également un premier aperçu crucial de l'efficacité et de l'innocuité d'un nouveau médicament, une étape particulièrement importante compte tenu des risques et des dépenses associés aux essais cliniques chez l'homme.
Une étude de 2012 soumise au département américain de la Santé et des Services sociaux a détaillé les coûts des essais cliniques de médicaments. Les auteurs de « Examination of Clinical Trial Costs and Barriers for Drug Development » ont estimé que le coût de réalisation des essais cliniques pour un nouveau médicament se situe entre environ 50 millions de dollars et 115 millions de dollars selon le domaine thérapeutique—le système respiratoire et l'oncologie étant parmi les plus coûteux. .
L'étude a également identifié les coûts des essais cliniques comme une raison possible du ralentissement des demandes d'approbation de nouveaux médicaments. Entre 2003 et 2012, le nombre d'approbations par la FDA de nouveaux médicaments par an est passé de 30 à 25,7 en moyenne au cours de la décennie précédente. Le nombre annuel moyen de dépôts a également légèrement diminué au cours de la même période. Les auteurs déclarent :« Une réduction du pipeline de demandes de médicaments signifie moins de nouvelles thérapies dans les années à venir. »
La technologie développée par l'équipe Lehigh et UPenn offre aux sociétés pharmaceutiques la possibilité d'avoir un aperçu précoce du profil d'efficacité et d'innocuité d'un nouveau traitement avant de s'engager dans des essais cliniques, entraînant ainsi moins de risques et des coûts inférieurs. Selon Liu, ce premier aperçu pourrait servir de "pont" entre le développement d'un médicament et les essais sur l'homme. En fin de compte, et c'est le plus important, la mise en place de ce « pont » pourrait entraîner le développement de nouveaux traitements contre les maladies qui atteignent les consommateurs plus rapidement.
En cultivant directement les cellules des patients dans leur puce biomimétique et en les testant dans des conditions similaires observées in vivo, il peut fournir des informations pour la médecine de précision qui sont adaptées à un patient spécifique dans un environnement spécifique au patient.
Liu, avec le mentor de l'industrie Ira Weisberg (PDG d'Amherst Pharmaceuticals) et le chef d'entreprise Christopher Uhl (étudiant en doctorat en bio-ingénierie à Lehigh) ont reçu une subvention NSF Innovation Corp et ont travaillé avec le Bureau de transfert de technologie de l'Université de Lehigh pour commercialiser la technologie sous le nom de société PharmaFlux.
« Alors que nous continuons à développer la plate-forme au-delà de l'étude de l'inflammation, " Liu dit, « nous espérons apporter une contribution significative à l'accélération de l'administration ciblée de médicaments et aider à inaugurer une nouvelle ère d'une meilleure médecine. »