
Une nouvelle méthode de manipulation des environnements de type gel qui abritent les cellules souches pourrait aider les chercheurs à diriger la croissance de ces cellules polyvalentes dans l'os, tendon, tissu ou d'autres lignées spécifiques, dit un ingénieur biomédical de l'Université Texas A&M qui a développé l'approche.
Travailler avec des hydrogels à base de collagène, qui sont des gels biodégradables utilisés dans un certain nombre d'applications biomédicales en raison de leur compatibilité avec l'organisme et ses processus, Akhilesh Gaharwar a développé une méthode pour moduler leur rigidité sans affecter la chimie ou la structure - un résultat qui pourrait avoir des implications majeures pour la recherche sur les cellules souches. Gaharwar, professeur adjoint au département de génie biomédical de l'université, a publié ses découvertes dans la revue scientifique ACS Nano . L'article complet est accessible sur pubs.acs.org/doi/abs/10.1021/acsnano.5b03918.
Spécifiquement, Gaharwar a pu augmenter la rigidité d'un hydrogel de 10 fois et sa ténacité de 20 fois grâce à un processus dans lequel il ajoute une petite quantité de sphérique, nanoparticules magnétiques aux hydrogels à base de collagène. L'ensemble du processus est terminé en quelques secondes, et cela lui permet de personnaliser le gel selon divers degrés de rigidité et de ténacité, en fonction de la quantité de nanoparticules dans le matériau, dit Gaharwar.
Le processus, il ajoute, a un autre avantage distinct :il est compatible avec les cellules. Parce que Gaharwar utilise des concentrations extrêmement faibles de nanoparticules, son procédé ne modifie pas de manière significative la composition chimique de l'hydrogel.
Contrôler les propriétés physiques des hydrogels, Gaharwar explique, est essentiel car ces gels doivent être durables tout en respectant les propriétés des tissus qu'ils simulent lorsqu'ils sont déployés dans le corps - par exemple, en agissant comme des échafaudages qui aident à la guérison des blessures internes. Ce n'est qu'une des nombreuses applications biomédicales que l'hydrogel de Gaharwar pourrait avoir un impact. En plus des applications d'ingénierie tissulaire, L'hydrogel amélioré mécaniquement de Gaharwar pourrait faire progresser les approches d'administration de médicaments, biocapteurs et autres technologies, mais il pourrait jouer un rôle encore plus important en tant qu'outil d'apprentissage sur les cellules souches, il dit. Le système, il explique, pourrait permettre aux chercheurs de mieux comprendre le comportement des cellules souches et même de contrôler la façon dont elles se différencient en types de cellules spécifiques.
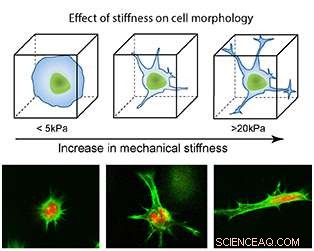
Connu pour leur capacité à se développer en différents types de cellules - comme un muscle, cellules sanguines ou cérébrales – les cellules souches ont le potentiel de servir de système de réparation interne, reconstituer d'autres cellules. Clé de cette transformation, note Gaharwar, est le microenvironnement entourant les cellules souches. Selon l'endroit où ces cellules souches sont situées dans le corps, ces cellules vont se transformer en différents types de cellules, il explique. Par exemple, les cellules souches qui sont étirées dans des environnements plus rigides pourraient finalement se transformer en cellules osseuses, tandis que les cellules souches qui restent rondes dans des environnements plus mous pourraient se développer en cartilage. Pensez-y comme une sorte d'effet domino :le microenvironnement de la cellule souche influence sa forme, et la forme de la cellule souche influence son développement en un type de cellule spécifique. Compte tenu de ce fait, Gaharwar pense que le contrôle de la rigidité de l'environnement de la cellule (dans ce cas, un hydrogel qui englobe les cellules souches) pourrait entraîner un contrôle accru de la différenciation des cellules souches.

Contrôler cet environnement, Gaharwar dit, est obtenu par un processus connu sous le nom de réticulation. La réticulation, il explique, implique de joindre les chaînes polymères qui composent un hydrogel afin qu'elles forment un réseau interconnecté qui sert essentiellement de squelette pour le gel et, par conséquent, augmente sa rigidité. Rejoindre ces chaînes nécessite les nanoparticules de Gaharwar, qui servent en quelque sorte de mortier en liant ces chaînes au niveau moléculaire. Ces sphériques, nanoparticules d'oxyde de fer, dont les surfaces ont été modifiées par Gaharwar et son équipe, ont de multiples points de conjugaison auxquels les chaînes polymériques se fixent en formant des liaisons chimiques fortes, il dit. Lorsque cela se produit, un réseau de chaînes est formé et l'hydrogel est renforcé, il dit.
D'autres technologies standard qui utilisent différentes nanoparticules n'entraînent pas le même niveau de rigidité mécanique car les nanoparticules n'interagissent pas chimiquement avec les chaînes polymères du gel; ils sont juste piégés, Gaharwar explique. Quoi de plus, les approches qui atteignent une certaine rigidité produisent souvent un environnement non convivial pour la cellule qui entraîne la mort cellulaire en raison de concentrations élevées de l'agent de renforcement, il dit. L'approche de Gaharwar surmonte ce défi en utilisant un 10, 000 fois moins de concentration de nanoparticules.
"En ajoutant une concentration infime de nanoparticules, nous pouvons obtenir une augmentation ou une diminution drastique des propriétés physiques de l'hydrogel, " dit Gaharwar. " En changeant la taille et la concentration des nanoparticules, nous pouvons obtenir des hydrogels allant d'un kilopascal à 200 kilopascals."
Fort des premiers résultats prometteurs que lui et son équipe ont obtenus, Gaharwar prévoit de continuer à travailler avec l'hydrogel amélioré pour déterminer s'il peut effectivement déclencher une différenciation dans les cellules souches. Ces cellules, il explique, besoin de faire l'expérience d'un environnement dynamique (comme ils le feraient dans le corps) où divers degrés de force sont appliqués à travers l'hydrogel et ressentis par les cellules qui s'y trouvent. Dans la phase suivante de la recherche, l'équipe, il dit, espère introduire ces stimuli externes avec un bioréacteur afin que des études plus approfondies puissent être menées.