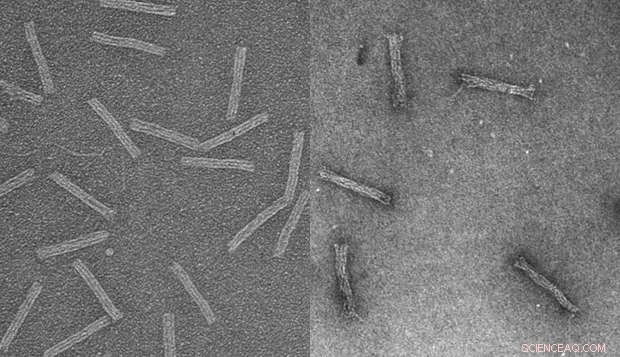
Des chercheurs de l'Ohio State University travaillent au développement de nanostructures d'ADN qui délivrent des médicaments aux cellules cancéreuses résistantes aux médicaments. Ces images au microscope électronique montrent les structures vides (à gauche) et chargées du médicament anticancéreux daunorubicine (à droite). Les chercheurs ont démontré pour la première fois que de telles structures en « origami d'ADN » peuvent être utilisées pour traiter les cellules leucémiques résistantes aux médicaments. Crédit :Randy Patton, L'Université d'État de l'Ohio.
Des chercheurs de l'Ohio State University travaillent sur une nouvelle façon de traiter le cancer résistant aux médicaments que les anciens Grecs approuveraient - seulement ce n'est pas un cheval de Troie, mais l'ADN qui cache la force d'invasion.
Dans ce cas, la force d'invasion est un médicament anticancéreux courant.
Dans les tests de laboratoire, les cellules leucémiques devenues résistantes au médicament l'ont absorbé et sont mortes lorsque le médicament a été caché dans une capsule faite d'ADN replié.
Précédemment, d'autres groupes de recherche ont utilisé la même technique d'emballage, connu sous le nom "Origami ADN, " pour déjouer la résistance aux médicaments dans les tumeurs solides. C'est la première fois que des chercheurs montrent que la même technique fonctionne sur des cellules leucémiques résistantes aux médicaments.
Les chercheurs ont depuis commencé à tester la capsule sur des souris, et espère passer aux essais sur le cancer chez l'homme d'ici quelques années. Leurs premiers résultats paraissent dans la revue Petit .
L'étude portait sur un modèle préclinique de leucémie myéloïde aiguë (LAM) qui a développé une résistance contre le médicament daunorubicine. Spécifiquement, lorsque des molécules de daunorubicine pénètrent dans une cellule AML, la cellule les reconnaît et les refoule à travers les ouvertures de la paroi cellulaire. C'est un mécanisme de résistance qui étudie le co-auteur John Byrd du centre médical Wexner de l'Ohio State University par rapport aux pompes de puisard qui tirent l'eau d'un sous-sol.
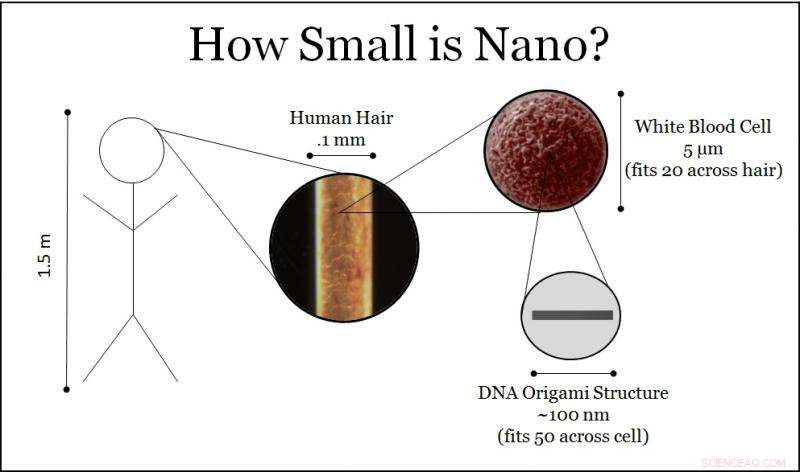
Un guide pratique sur l'échelle de taille de l'origami ADN. Crédit :Patrick Halley, L'université d'État de l'Ohio
Lui et Carlos Castro, professeur assistant en génie mécanique, diriger une collaboration axée sur la dissimulation de la daunorubicine à l'intérieur d'une sorte de cheval de Troie moléculaire qui peut contourner les pompes afin qu'elles ne puissent pas éjecter le médicament de la cellule.
"Les cellules cancéreuses ont de nouvelles façons de résister aux médicaments, comme ces pompes, et la partie excitante de l'emballage du médicament de cette façon est que nous pouvons contourner ces défenses afin que le médicament s'accumule dans la cellule cancéreuse et provoque sa mort, " dit Byrd, professeur de médecine interne et directeur de la division d'hématologie. "Potentiellement, nous pouvons également adapter ces structures pour qu'elles délivrent des médicaments de manière sélective aux cellules cancéreuses et non à d'autres parties du corps où elles peuvent provoquer des effets secondaires. »
"Les nanostructures d'origami d'ADN ont beaucoup de potentiel pour l'administration de médicaments, pas seulement pour fabriquer des véhicules d'administration de médicaments efficaces, mais permettant de nouvelles façons d'étudier l'administration de médicaments. Par exemple, on peut faire varier très précisément la forme ou la rigidité mécanique d'une structure et voir comment cela affecte l'entrée dans les alvéoles, " dit Castro, directeur du Laboratoire de nano-ingénierie et de biodesign.
Dans les essais, les chercheurs ont découvert que les cellules AML, qui avait précédemment montré une résistance à la daunorubicine, efficacement absorbé les molécules médicamenteuses lorsqu'elles étaient cachées à l'intérieur de minuscules capsules en forme de bâtonnets faites d'ADN. Sous le microscope, les chercheurs ont suivi les capsules à l'intérieur des cellules avec des étiquettes fluorescentes.
Chaque capsule mesure environ 15 nanomètres de large et 100 nanomètres de long, soit environ 100 fois plus petite que les cellules cancéreuses qu'elle est conçue pour infiltrer. Avec quatre creux, compartiments intérieurs ouverts, cela ressemble moins à une pilule qu'un humain avalerait et plus à un parpaing allongé.
Le chercheur postdoctoral Christopher Lucas a déclaré que la conception maximise la surface disponible pour transporter le médicament. « La façon dont la daunorubicine agit est qu'elle pénètre dans l'ADN de la cellule cancéreuse et l'empêche de se répliquer. Nous avons donc conçu une structure de capsule qui aurait beaucoup de paires de bases d'ADN accessibles pour qu'elle puisse se glisser. Lorsque la capsule se décompose, les molécules de médicament sont libérées pour inonder la cellule."
L'équipe de Castro a conçu les capsules pour qu'elles soient solides et stables, afin qu'ils ne se désintègrent pas complètement et ne libèrent pas la majeure partie de la drogue avant qu'il ne soit trop tard pour que la cellule les recrache.
Et c'est ce qu'ils ont vu avec un microscope à fluorescence :les cellules ont attiré les capsules dans les organites qui les digéreraient normalement, s'ils étaient de la nourriture. Lorsque les capsules se sont brisées, les médicaments ont inondé les cellules et les ont fait se désintégrer. La plupart des cellules sont mortes dans les 15 heures suivant la consommation des capsules.
Ce travail est le premier effort des ingénieurs du laboratoire de Castro pour développer une application médicale pour les structures d'origami ADN qu'ils ont construites.
Bien que l'ADN soit stéréotypé appelé « les éléments constitutifs de la vie, " Les ingénieurs utilisent aujourd'hui l'ADN naturel et synthétique comme blocs de construction littéraux pour les dispositifs mécaniques. Auparavant, les ingénieurs de l'État de l'Ohio ont créé de minuscules charnières et pistons d'ADN.
Comme Castro l'a souligné, L'ADN est un polymère, bien que naturel, et lui et ses collègues le façonnent en de minuscules dispositifs, des outils ou des contenants en exploitant les interactions physiques des bases qui composent la chaîne polymère. Ils construisent des chaînes à partir de séquences d'ADN qui vont naturellement s'attirer et se lier les unes aux autres d'une certaine manière, de sorte que longtemps les longs polymères se replient automatiquement, ou "auto-assembler, " en formes utiles.
Dans le cas de ce cheval de Troie ADN, les chercheurs ont utilisé le génome d'un bactériophage commun, un virus qui infecte les bactéries, et des brins synthétiques conçus pour replier l'ADN du bactériophage. Bien que la forme repliée remplisse une fonction, l'ADN lui-même ne le fait pas, a expliqué Patrick Halley, un étudiant diplômé en génie qui fait ce travail pour obtenir sa maîtrise.
"L'une des choses les plus difficiles à faire passer lorsque vous présentez cette technologie aux gens est que la capsule d'ADN ne fait rien d'autre que de maintenir une forme. C'est juste un statique, structure rigide qui porte des choses. Il ne code aucune protéine et ne fait rien d'autre que ce que nous pensons normalement faire de l'ADN, " a déclaré Halley.
En accord avec l'idée de fabrication d'origami ADN, Castro a déclaré qu'il espère créer un processus rationalisé et économiquement viable pour la construction des capsules - et d'autres formes également - dans le cadre d'un système modulaire d'administration de médicaments.
Byrd a déclaré que la technique devrait potentiellement fonctionner sur la plupart des formes de cancer résistant aux médicaments si d'autres travaux montrent qu'elle peut être efficacement traduite dans des modèles animaux, bien qu'il se soit arrêté avant de suggérer que cela fonctionnerait contre les agents pathogènes tels que les bactéries, où les mécanismes de résistance aux médicaments peuvent être différents.