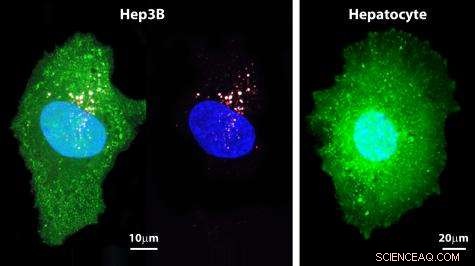
La figure de gauche (Hep3B) montre une cellule hépatique cancéreuse à fluorescence verte pénétrée par des protocellules. Les petits points rouges sont des enveloppes lipidiques bicouches. Leur cargaison - des nanoparticules remplies de médicament, leurs pores ici remplis de colorants fluorescents blancs à des fins d'imagerie - pénètrent dans la cellule cancéreuse. (La pénétration est plus clairement visible sur la deuxième image.) La cellule normale à droite (hépatocyte) ne montre aucune pénétration. (Images avec l'aimable autorisation de Carlee Ashley)
(PhysOrg.com) -- Fusion de la nanotechnologie et de la recherche médicale, Laboratoires nationaux Sandia, l'Université du Nouveau-Mexique, et le Centre de recherche et de traitement du cancer de l'UNM ont élaboré une stratégie efficace qui utilise des nanoparticules pour faire exploser les cellules cancéreuses avec un mélange de médicaments tueurs.
Dans l'article de couverture du numéro de mai de Matériaux naturels , disponible en ligne le 17 avril , les chercheurs décrivent des nanoparticules de silice d'environ 150 nanomètres de diamètre comme alvéolées avec des cavités qui peuvent stocker de grandes quantités et variétés de médicaments.
"L'énorme capacité du noyau nanoporeux, avec sa grande surface, combiné avec le ciblage amélioré d'une bicouche lipidique encapsulante [appelée liposome], permettre à une seule «protocellule» chargée d'un cocktail de médicaments de tuer une cellule cancéreuse résistante aux médicaments, " dit le chercheur de Sandia et professeur à l'UNM Jeff Brinker, le chercheur principal. "C'est un million de fois plus efficace que des méthodes comparables utilisant des liposomes seuls - sans nanoparticules - comme vecteurs de médicaments."
Les nanoparticules et les membranes cellulaires environnantes formées à partir de liposomes forment ensemble la combinaison appelée protocellule :la membrane scelle la cargaison mortelle et est modifiée avec des molécules (peptides) qui se lient spécifiquement aux récepteurs surexprimés à la surface de la cellule cancéreuse. (Trop de récepteurs est un signal que la cellule est cancéreuse.) Les nanoparticules assurent la stabilité de la membrane supportée et contiennent et libèrent la cargaison thérapeutique à l'intérieur de la cellule.
Une stratégie actuelle de livraison de nanoparticules approuvée par la Food and Drug Administration consiste à utiliser les liposomes eux-mêmes pour contenir et livrer la cargaison. Dans une comparaison directe de liposomes et de protocellules ciblés avec des compositions membranaires et peptidiques identiques, Brinker et ses collègues signalent que la plus grande capacité de chargement, la stabilité et l'efficacité de ciblage des protocellules conduisent à une cytotoxicité [destruction] plusieurs fois plus importante dirigée spécifiquement vers les cellules cancéreuses du foie humain.
Un autre avantage des protocellules par rapport aux liposomes seuls, dit l'auteur principal Carlee Ashley, un post-doctorant Harry S. Truman sur le site californien de Sandia à Livermore, est que les liposomes utilisés comme supports nécessitent des stratégies de chargement spécialisées qui rendent le processus plus difficile. "Nous avons démontré que nous pouvons simplement tremper les nanoparticules pour les charger avec des combinaisons de médicaments uniques nécessaires à la médecine personnalisée. Ils encapsulent efficacement les toxines ainsi que les siARN [acide ribonucléique] qui réduisent au silence les expressions des protéines."
ARN, le messager biologique qui indique aux cellules quelles protéines fabriquer, dans ce cas est utilisé pour faire taire l'usine cellulaire, un moyen de provoquer l'apoptose ou la mort cellulaire. "Si" est l'abréviation de "silence".
Les lipides servent également de bouclier qui empêche les médicaments de chimiothérapie toxiques de s'échapper de la nanoparticule jusqu'à ce que la protocellule se lie à la cellule cancéreuse et s'y installe. Cela signifie que peu de poisons s'infiltrent dans le système de l'hôte humain, si les protocellules ne trouvent pas de cellules cancéreuses. Ce voile atténue les effets secondaires toxiques attendus de la chimiothérapie conventionnelle.
Au lieu, les particules - suffisamment petites pour flotter sous le radar du foie et d'autres organes de nettoyage - peuvent circuler sans danger pendant des jours ou des semaines, en fonction de leur taille d'ingénierie, à la recherche de leur proie.
Une bibliothèque de phages - des virus qui attaquent les bactéries - a été créée au centre de cancérologie accrédité au niveau national de l'UNM par le collaborateur David Peabody. Cela a permis aux chercheurs d'exposer les phages à un groupe de cellules cancéreuses et de cellules normales, permettant l'identification de peptides qui se lient spécifiquement aux cellules cancéreuses mais pas aux cellules normales.
"Les protéines modifiées avec un peptide de ciblage qui se lie à un carcinome particulier présentent un 10, affinité mille fois plus grande pour ce cancer que pour d'autres cellules non apparentées, " a déclaré Ashley.
Brinker ajoute, "Une caractéristique clé de notre protocellule est que sa bicouche fluide permet une liaison de haute affinité avec seulement quelques-uns de ces peptides dans l'ensemble. Cela réduit la liaison non spécifique et la réponse immunitaire."
La méthode est testée sur des cellules cancéreuses humaines in vivo, et sera prochainement testé sur des tumeurs de souris au centre de cancérologie de l'UNM.
Les chercheurs continuent d'optimiser la taille de la particule de silice poreuse, qui est formé en aérosolisant une solution de précurseur. Le processus de fabrication de nanoparticules poreuses - appelé auto-assemblage induit par évaporation, et pionnier dans le laboratoire Brinker — produit des particules de 50 nm à plusieurs microns de diamètre. Les tailles de particules comprises entre 50 et 150 nanomètres de diamètre sont idéales pour maximiser la circulation et l'absorption dans les cellules cancéreuses, ainsi les particules sont présélectionnées par taille avant leur formation en protocellules.
"Leurs dimensions globales déterminent à quel point ils seront distribués dans la circulation sanguine, " a déclaré Brinker. "Nous modifions notre synthèse pour favoriser les plus petites tailles."
La charge électrique et l'hydrophobie [évitement de l'eau] sont également importantes pour le temps de circulation de la particule, ce qui peut améliorer ou diminuer sa capacité à rester exempt d'enchevêtrements moléculaires ou énergétiques indésirables.
La méthode peut être disponible dans le commerce dans cinq ans, les chercheurs estiment.