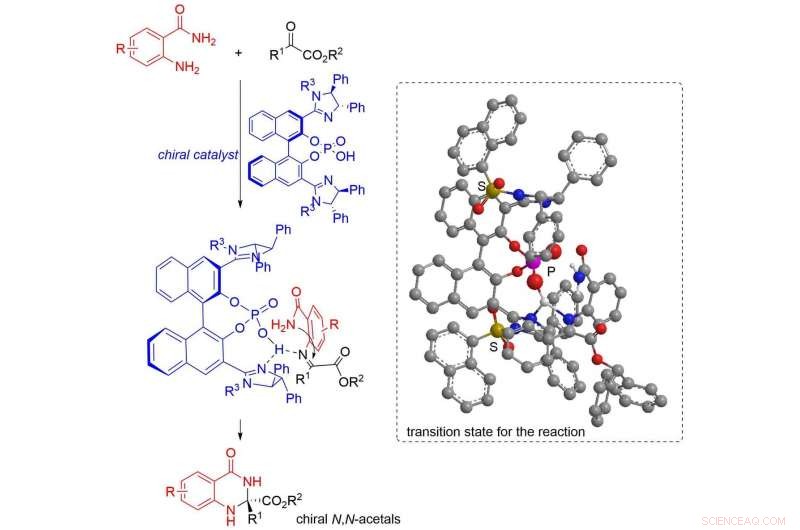
Crédit :Institut de technologie de Nagoya
Beaucoup de nos médicaments et autres médicaments bioactifs sont basés sur des structures chimiques appelées énantiomères, des molécules qui sont des images miroir les unes des autres et qui ne sont pas superposables. Parmi eux, le chiral N, N-acétals contenus dans les médicaments diurétiques comme le bendrofluméthiazide et le thiabutazide, utilisé pour traiter l'hypertension artérielle et l'œdème. Parce qu'un énantiomère et sa version miroir ont souvent des activités biologiques différentes, avec un seul d'entre eux ayant une utilité pharmacologique, une synthèse énantiosélective ou asymétrique produisant l'énantiomère souhaité en plus grandes quantités est hautement souhaitable.
Dans le cas de N, N-acétals, plusieurs études ont démontré leur préparation énantiosélective à partir d'aldéhydes, aldimines, ou énamines. Cependant, dans tous ces cas, leur partenaire de réaction a été limité à l'aldéhyde ou aux imines. Alors que les cétones ont été utilisées, avec des exemples de N énantiosélectif réussi, synthèse de N-acétal, leur utilisation - en général - n'est pas considérée comme efficace.
Dans une étude récente publiée dans Synthèse et catalyse avancées , des scientifiques du Nagoya Institute of Technology (NITech) et de l'Université d'Osaka au Japon ont exploré cette situation avec une synthèse énantiosélective de N chiral, N-acétals de composés -dicarbonylés - composés avec deux groupes carbonyle (cétone) sur le -carbone - en présence de catalyseurs chiraux d'acide phosphorique imidazoline, et obtenu des rendements aussi élevés que 99% avec une énantiopure maximale de 96%.
"Notre étude présente la première formation hautement stéréosélective de N chiral, N-acétals de -cétoesters utilisant un catalyseur original qui peut également être utilisé pour d'autres réactions de synthèse stéréosélectives, " déclare le professeur Shuichi Nakamura de NITech, qui a dirigé l'étude.
Les scientifiques ont commencé par examiner la réaction du 2-aminobenzamide avec divers α-cétoesters en présence de différents catalyseurs. Les -cétoesters différaient les uns des autres par la nature du groupe fonctionnel attaché au -carbone, tandis que les catalyseurs choisis étaient l'acide bis(imidazoline)-phosphorique avec différents substituants attachés à l'azote dans le cycle imidazoline, acide mono-imidazoline-phosphorique, et deux acides phosphoriques chiraux commerciaux. Parmi ces différentes combinaisons, les scientifiques ont trouvé le meilleur rendement (99%) et l'énantiopure (92%) dans le cas du -cétoester avec un groupe benzhydryle et d'un catalyseur acide bis(imidazoline)-phosphorique avec un groupe 1-naphtalènesulfonyle.
Les scientifiques ont ensuite examiné la réaction de divers aminobenzamides (portant soit un groupe méthyle donneur d'électrons, soit un fluoro attracteur d'électrons, chloro, et des groupes bromo) avec différents α-cétoesters (contenant le même groupe benzhydryle mais des groupes fonctionnels différents à la place d'un groupe phényle antérieur) conservant le même catalyseur acide bis(imidazoline)-phosphorique avec un groupe 1-naphtalènesulfonyle. Toutes les combinaisons ont montré un bon rendement (77-95%) ainsi qu'une énantiosélectivité élevée (82-96%).
En outre, l'équipe a étudié la synthèse énantiosélective de N, N-acétals via la réaction de la N-benzyl isatine (un -cétoamide cyclique), benzile (une dicétone acyclique), et le benzaldéhyde avec le 2-aminobenzamide pour le même catalyseur. Les trois réactions ont donné des produits avec une énantiopure élevée (91-93%).
L'équipe a également proposé un mécanisme possible pour le N, Réaction de formation de N-acétal correspondant au meilleur rendement (99%), impliquant un intermédiaire cétimine avec un groupe amide qui permet d'éviter la répulsion stérique entre le groupe phényle sur l'imidazoline, permettant la formation d'un isomère (R) à haute énantiopure.
Bien que le mécanisme soit encore spéculatif et nécessite une enquête plus approfondie, les scientifiques sont enthousiasmés par les implications potentielles des résultats expérimentaux. « Notre nouvelle méthode permettra la synthèse de candidats médicaments actuellement difficiles à synthétiser, et peut même potentiellement aider à créer et à fournir aux gens de nouveaux et meilleurs médicaments à l'avenir, " conclut le Pr Nakamura.
Maintenant, ce sont des conséquences prometteuses à espérer!