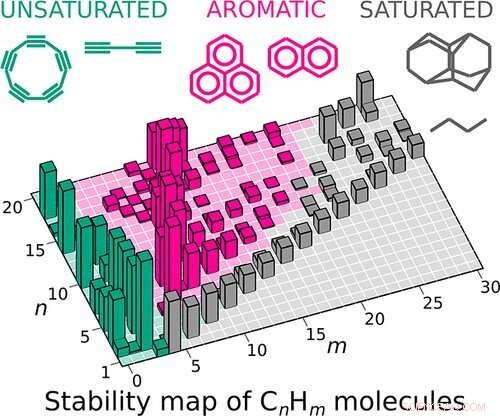
Carte de stabilité des hydrocarbures de 1 à 20 atomes de carbone (n) et de 0 à 30 atomes d'hydrogène (m). La hauteur de la colonne représente le degré de « magie » de la molécule. Crédit :Sergey V. Lepeshkin et al, The Journal of Physical Chemistry Letters (2022). DOI :10.1021/acs.jpclett.2c02098
Une équipe de recherche de Skoltech dirigée par le professeur Artem R. Oganov a découvert pourquoi certains hydrocarbures sont abondants dans la nature et faciles à synthétiser, alors que d'autres ne le sont pas. Ils ont utilisé la "magicité" comme mesure pour évaluer la stabilité des molécules par rapport à des molécules de compositions légèrement différentes. Cette approche a permis de construire une carte de stabilité qui est en bon accord avec les expériences et prédit de nouvelles molécules potentiellement synthétisables. L'article décrivant les résultats de cette étude est paru dans The Journal of Physical Chemistry Letters .
Les hydrocarbures sont des composés de carbone et d'hydrogène avec une formule générale, CnHm, où n et m sont respectivement le nombre d'atomes de carbone et d'hydrogène. Les hydrocarbures sont une classe majeure de molécules organiques et sont étonnamment nombreux. Pourtant, certains sont plus courants et plus faciles à synthétiser expérimentalement, tandis que d'autres ne peuvent être obtenus que par des astuces chimiques ingénieuses. Il n'était pas tout à fait clair pourquoi il en est ainsi.
"Le manuel de chimie organique avec sa multitude aléatoire de molécules différentes semble effrayant. Personne n'a la moindre idée de la raison pour laquelle certaines molécules existent et d'autres non. Vous pouvez en apprendre beaucoup sur chaque molécule spécifique si vous dessinez sa structure chimique à l'aide de ' sticks" pour représenter les liens entre les atomes, mais en réalité, de nombreux concepts liés à cela restent encore un sujet de débat et ne répondent pas à la question "Pourquoi ?". Les "sticks" ne sont rien de plus qu'un outil abstrait pratique, tandis que les le critère de stabilité rigoureux pour les composés est l'énergie », explique l'auteur principal de l'étude, Sergey Lepeshkin.
Dans leur nouvelle étude, les chercheurs ont examiné la chimie des hydrocarbures d'un point de vue théorique, en utilisant les valeurs énergétiques de divers composés comme référence. La stabilité dépend beaucoup moins de l'énergie absolue de la molécule que de son énergie relative à la moyenne des énergies de ses composés voisins avec un atome (de chaque type) en plus et un atome en moins. Les auteurs ont utilisé le concept de "magicité" précédemment proposé pour les nanoparticules pour identifier les composés les plus stables. Une molécule est "magique" si elle est plus stable qu'un ensemble de ses voisines dans l'espace chimique.
Les chercheurs ont effectué des calculs et effectué un test de "magicité" sur une large gamme de composés, la molécule comprenant jusqu'à 20 atomes de carbone et 42 atomes d'hydrogène. Pour cela, ils ont utilisé l'algorithme USPEX (Universal Structure Predictor :Evolutionary Xtallography) précédemment développé par Oganov et son équipe. Cet algorithme prédit simultanément des structures avec un minimum d'énergie pour chaque composition, permettant à différentes molécules de se concurrencer et d'échanger des informations structurelles entre elles. Une fois que l'outil avait obtenu les énergies pour toutes les compositions, il identifiait automatiquement les molécules "magiques", produisant une carte de stabilité pour tous les hydrocarbures dans la plage de compositions spécifiée.
"Nous avons maintenant toute la chimie des hydrocarbures sur une seule carte. Remarquablement, les "crêtes de stabilité" représentent la série homologue de nos manuels scolaires, qui sont essentiellement des séries de composés avec des changements réguliers de composition, de structure et de propriétés. La carte montre clairement quelles molécules sont faciles à synthétiser et qui peuvent se former spontanément et s'accumuler en grandes concentrations. Par exemple, la carte explique pourquoi certains des composés existent dans les atmosphères planétaires et l'espace interstellaire, dans les flammes et dans les gisements de pétrole. Enfin, la carte peut prévoir les composés qui restent à trouver. D'un grand intérêt sont ceux qui existent déjà mais qui ne sont pas « magiques ». Les exemples les plus frappants incluent le cyclopropane que les chimistes considèrent comme instable en raison de liaisons tendues avec des angles non optimaux, le butadiène qui est connu pour être très actif et sa propension à la polymérisation est utilisé dans la production industrielle de caoutchouc, et une molécule emblématique, le cyclobutadiène , qu'il a fallu 30 bonnes années pour synthétiser", conclut Oganov.
Ainsi, les chercheurs ont montré qu'un critère énergétique permet de décider si une molécule est stable ou non et offre une perspective sur l'étonnante diversité des hydrocarbures et de la chimie organique dans son ensemble. Ils ont mis au point une méthode universelle qui peut être utilisée pour l'analyse de stabilité de toute autre classe de molécules. Des chimistes réalisent l'exploit d'"édition moléculaire"