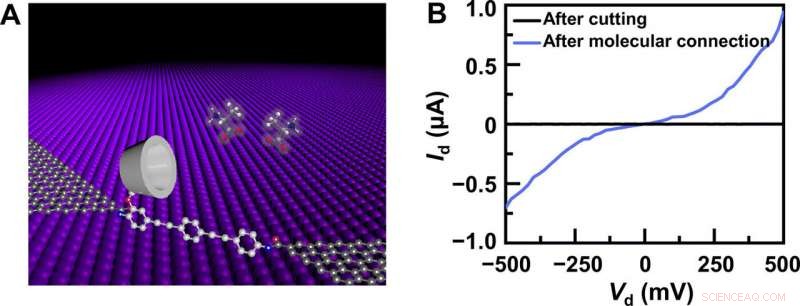
Structure de l'appareil et caractérisation électrique. (A) Représentation schématique d'un GMG-SMJ basé sur PM-β-CD. La machine moléculaire dotée d'un PM-β-CD était connectée de manière covalente avec des contacts ponctuels de graphène par des liaisons amide. (B) Courbes I-V de GMG-SMJ après coupage au plasma d'oxygène et après une nouvelle connexion moléculaire. Crédit: Avancées scientifiques , doi:10.1126/sciadv.abe4365
La chimie analytique vise à discriminer efficacement entre deux acides aminés. Dans un nouveau rapport en Avancées scientifiques , Zihao Liu et une équipe de recherche en Chimie, La physique, et la science des matériaux en Chine et au Japon, ont utilisé une méthode électrique monomoléculaire basée sur des nanocircuits moléculaires pour former des jonctions monomoléculaires stables graphène-molécule-graphène. L'équipe a développé ces jonctions moléculaires en liant de manière covalente une machine moléculaire. Ensuite, ils ont utilisé le pH pour faire varier le type et la charge des acides aminés afin de trouver des fluctuations de courant multimodales distinctes provenant de diverses interactions hôtes hôtes par rapport aux calculs théoriques. Les données de conductance ont produit des temps de nivellement et des vitesses de navette caractéristiques pour chaque acide aminé afin de permettre des mesures in situ précises et en temps réel. Les scientifiques ont testé quatre acides aminés et leurs énantiomères (molécules chirales qui sont des images miroir les unes des autres) pour montrer la capacité de les distinguer en quelques microsecondes pour fournir une méthode simple et précise pour l'identification des acides aminés ainsi que la protéine à molécule unique. séquençage.
Éléments constitutifs des protéines
Les acides aminés forment les éléments constitutifs des protéines, molécules avec des fonctions physiologiques spéciales et des éléments structurels clés dans les produits pharmaceutiques avec des applications dans les sciences de la vie. Les chercheurs peuvent reconnaître les énantiomères des acides aminés pour fournir des informations importantes relatives à la reconnaissance chirale et aux fonctions physiologiques dans les systèmes biologiques. Détecter la structure, la pureté énantiomérique et le comportement dynamique des acides aminés peuvent favoriser la production de nouvelles techniques pour le séquençage des protéines et les investigations pharmaceutiques. La détection et l'identification d'acides aminés avec différentes structures et chiralité sont d'une importance cruciale pour la protéomique, pharmaceutiques et nanobiotechnologies. Cependant, les machines moléculaires existantes ne fonctionnent qu'en comparant les paramètres thermodynamiques de l'ensemble, ce qui est insuffisant. Il est donc important de développer une technique moléculaire générale pour révolutionner les méthodes existantes et reconnaître les molécules cibles avec une grande précision. Dans ce travail, Liu et al. a démontré une technique à molécule unique pour identifier directement différents acides aminés protéinogènes et leurs énantiomères via des mesures dynamiques précises des interactions hôte-invité basées sur une technique à molécule unique connue sous le nom de jonctions monomoléculaires graphène-molécule-graphene abrégées en GMG-SMJ de manière covalente incorporer des systèmes moléculaires individuels se comportant comme un canal conducteur dans un nanocircuit électrique.
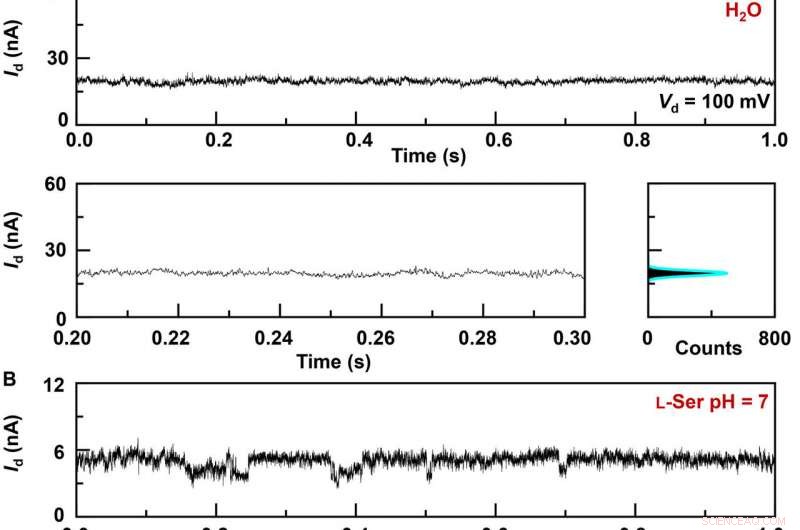
Enregistrements actuels en temps réel de la dynamique d'interaction hôte-invité dans les GMG-SMJ. courbes I-t de différents GMG-SMJ (en haut), les parties agrandies (en bas à gauche), et leurs histogrammes correspondants (en bas à droite) :(A) Un appareil fonctionnant dans une eau pure, (B) le même dispositif dans une solution aqueuse de L-Ser 100 nM, et (C) un autre dispositif dans une solution aqueuse de L-Ala 100 nM. Les encarts dans les histogrammes sont les parties agrandies des petits pics. pH =7, T =298 K, et la tension de polarisation =0,1 V. Crédit :Science Advances, doi:10.1126/sciadv.abe4365
La nouvelle approche a fourni une plate-forme robuste pour former une électronique à molécule unique afin de créer des dispositifs optoélectroniques moléculaires. Pour développer les constructions, Liu et al. pris en sandwich de manière covalente une machine moléculaire entre une paire de contacts ponctuels de graphène nano-écartés pour la détection des acides aminés et la reconnaissance de la chiralité. Les résultats ouvriront de nouvelles voies pour développer la nanotechnologie du séquençage précis des protéines à molécule unique pour des applications pratiques.
Développement d'appareils, caractérisation électrique et mesures en temps réel
L'équipe de recherche a synthétisé du graphène monocouche à l'aide d'un dépôt chimique en phase vapeur sur des feuilles de cuivre et l'a transféré sur des plaquettes de dioxyde de silicium/silicium et a modelé les électrodes métalliques par photolithographie. Pour développer les électrodes de contact ponctuelles en graphène à nano-écartement, ils ont utilisé une méthode lithographique en tirets. Ils ont ensuite construit des GMG-SMJ (jonctions de molécule unique de graphène-molécule-graphene) en connectant de manière covalente une seule machine moléculaire avec des électrodes de graphène via des liaisons amide. L'équipe a mesuré les courbes courant-tension des appareils à diverses étapes pour identifier la formation de GMG-SMJ. Le transport de charge à travers la jonction résultait de connexions à une seule molécule. Ils ont ensuite effectué des caractérisations électriques en fonction du temps pour surveiller la conductance des jonctions moléculaires uniques (SMJ) de la perméthylée-β-cyclodextrine (PM-β-CD) en temps réel. Ils ont d'abord mesuré les constructions dans l'eau, puis dans diverses solutions de différents acides aminés. Les trajectoires représentatives à l'heure actuelle ont révélé des distributions à pics multiples pour différents acides aminés en solution tels que la L-sérine et la L-alanine. Les multiples états distincts de chaque acide aminé proviennent uniquement du processus d'association/dissociation entre le centre fonctionnel PM-β-CD et les acides aminés environnants.
Analyses informatiques des SMJ L-Ala@PM-β-CD. (A) Diagramme schématique des orbitales moléculaires frontières calculées de la machine moléculaire. (B à D) Configurations moléculaires typiques lors de l'association avec des acides aminés différemment chargés :(B) cation, (C) zwitterion, et (D) anion. (E) Spectres de transmission correspondants à une tension de polarisation nulle. Le rouge, jaune, et les courbes vertes montrent la transmission lorsque l'anion, zwitterion, et les formes cationiques étaient dans la cavité, respectivement. La courbe bleue montre la cavité du vide. Les spectres complets sont fournis dans la fig. S4. (F à H) Représentation schématique des acides aminés en cation, zwitterion, et les formes anioniques. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abe4365 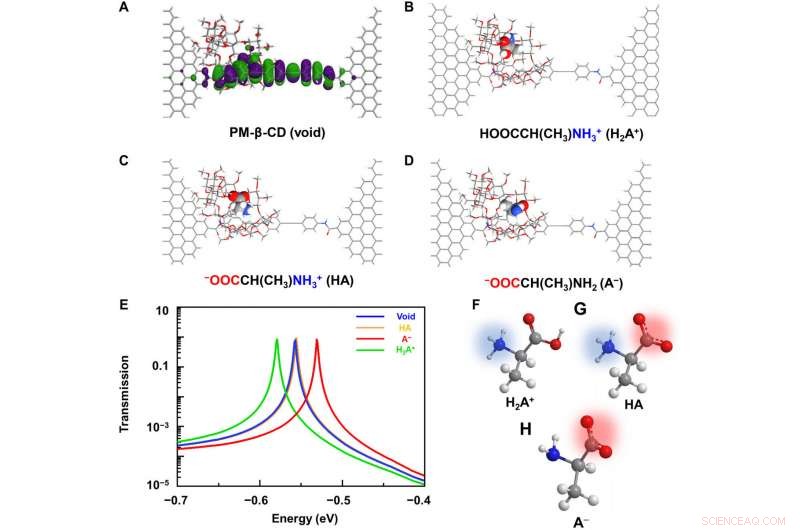
Pour mieux comprendre la corrélation entre les interactions hôte-invité dans les jonctions moléculaires uniques PM-β-CD à base de L-alanine, Liu et al. ont calculé les spectres de transmission de l'hôte PM-β-CD avec des invités L-Alanine différemment chargés. Pour y parvenir, ils ont utilisé une technique de fonction de Green hors d'équilibre basée sur la théorie de la fonctionnelle de la densité, comme le suggère le package Atomistix Toolkit. They noted the conductance contribution from the perturbed highest occupied molecular orbital (p-HOMO) to be dominant at low bias voltages as reflected with transmission spectra. The transmission spectra of the configurations were significantly different near the Fermi level of electrodes to afford different conductance stages. The researchers then analyzed the transitions between each level during amino acid recognition. They used L-alanine as an example to observe reversible transitions from the dissociation to form cations, zwitterions, and anion forms. The dissociation level dominated the device conductance, and the team collected the information using a four-state model, which described the transitions to understand the capacity to detect different structures of amino acids when interacting with PM-β-CD. The amino acids had at least two association processes for the carboxylic group and the other amino group. The greater the number of states recorded, the more accurate the recognition of results were.
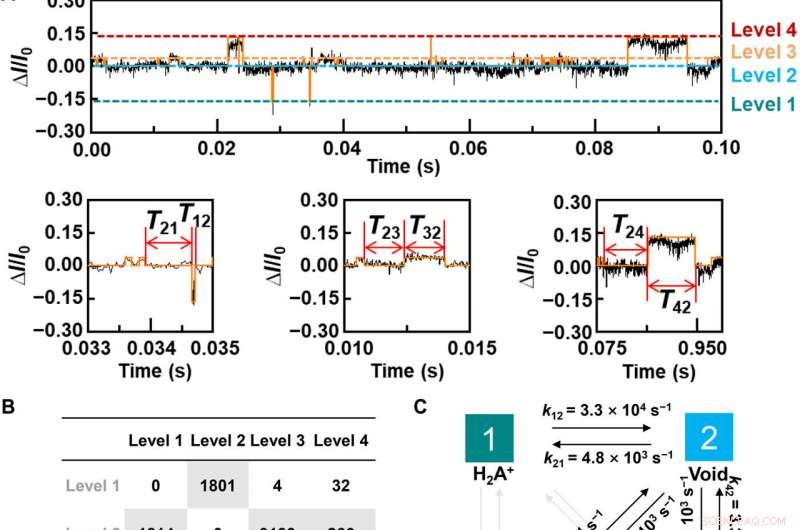
Dynamic analysis for L-Alanine detection. (A) Plot of ΔI/I0 as a function of time during the host-guest interaction. The red curve is the idealized fit by using a QuB software. pH =7, T =298 K, and the bias voltage =0.1 V. (B) Transition statistics between each state. The horizontal columns mean the initial state. (C) Kinetic model for the L-Ala recognition process. (D to I), Plots of time intervals of (D) level 1 to level 2, (E) level 2 to level 1, (F) level 2 to level 3, (G) level 3 to level 2, (H) level 2 to level 4, and (I) level 4 to level 2 at 298 K. Credit:Science Advances, doi:10.1126/sciadv.abe4365
Enantiomer recognition and outlook
Due to the similarity between enantiomers, it was more challenging to differentiate the structures compared to species identification. The associated energy differences were small and close to computational errors. To overcome these complexities, the team established a distinct "fingerprint database" for each amino acid to compare the conductance and kinetic data of different enantiomers. The team then achieved the current change and relaxation time data and compared them with the fingerprint database. Due to this universality, the method can also recognize chiral functional drug molecules to establish a broad approach for biomolecular detection at the single molecule-level.
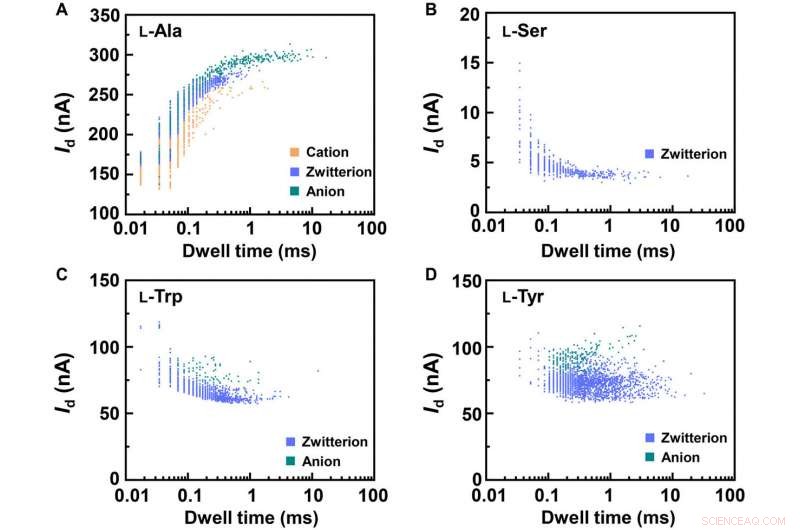
Statistical analyses of the translocation events for different amino acids. Translocation events (current as a function of the dwell time) were analyzed for (A) L-Ala, (B) L-Ser, (C) L-Trp, and (D) L-Tyr, respectivement. The two-dimensional (2D) contour plots are composed of all the events in 10-s recording at pH =7, showing the capability of detecting the different structures of amino acids when interacting with PM-β-CD. Crédit :Avancées scientifiques, doi:10.1126/sciadv.abe4365
De cette façon, Zihao Liu and colleagues presented a practical single-molecule approach for real-time electrical recognition of amino acids with different structures and chirality within microseconds. The host-guest dynamic processes could be observed for diverse amino acids at the level of the anion, zwitterion and cation shuttling. Using the permethylated-β-cyclodextrin (PM-β-CD) complex, the team recognized differently charged states of amino acids based on current fluctuation range and thermodynamic/kinetic parameters. The technique can revolutionize existing methods to accurately sequence single-molecule gene/protein sequencing toward universal applications. The method can also offer a universal tool to recognize many important molecules in environmental or biological systems to understand the basis of life at the molecular level.
© 2021 Réseau Science X