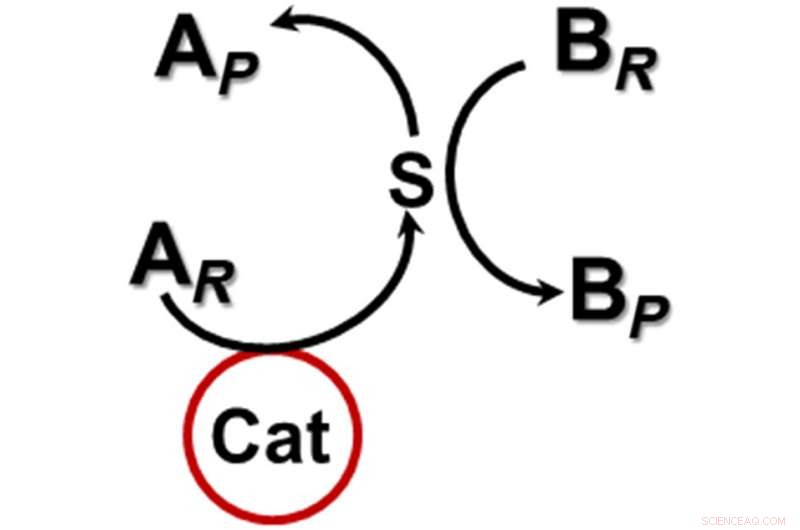
Un système catalytique sans contact. Crédit: Avancées scientifiques (2020). DOI :10.1126/sciadv.aax6637
Une équipe de recherche de la Northwestern University a révélé une nouvelle approche pour conduire des réactions chimiques, une approche qui ne nécessite pas de contact direct avec un catalyseur.
Dans les réactions catalytiques typiques, le catalyseur - la substance qui augmente la vitesse d'une réaction chimique - et les réactifs substrats doivent être présents dans le même milieu et en contact direct les uns avec les autres pour produire une réaction. Le nouveau système de l'équipe de recherche démontre une réaction chimique produite par un intermédiaire créé par une réaction chimique distincte. Les résultats pourraient avoir des applications dans l'assainissement de l'environnement et la production de carburant.
"Améliorer notre compréhension de la relation catalyseur-intermédiaire-réaction pourrait considérablement élargir les possibilités de réactions catalytiques, " dit Harold Kung, Walter P. Murphy Professeur de génie chimique et biologique à la McCormick School of Engineering, qui a dirigé la recherche. "En apprenant qu'une réaction chimique peut se dérouler sans contact direct avec un catalyseur, nous ouvrons la porte à l'utilisation de catalyseurs à partir d'éléments abondants dans la terre pour effectuer des réactions qu'ils ne catalyseraient normalement pas. »
L'étude, intitulé "Noncontact Catalysis:Initiation of Selective Ethylbenzene Oxidation by Au Cluster-Facilitated Cyclooctene Epoxidation, " a été publié le 31 janvier dans la revue Avancées scientifiques . Mayfair Kung, professeur agrégé de recherche en génie chimique et biologique, était un auteur co-correspondant sur le papier. Linda Broadbelt, Sarah Rebecca Roland Professeur de génie chimique et biologique et doyenne associée à la recherche, également contribué à l'étude.
La recherche s'appuie sur des travaux antérieurs dans lesquels l'équipe a étudié l'oxydation sélective du cyclooctène, un type d'hydrocarbure, en utilisant de l'or (Au) comme catalyseur. L'étude a révélé que la réaction était catalysée par des nanoclusters d'or dissous. Surpris, les chercheurs ont entrepris d'étudier dans quelle mesure les grappes d'or pourraient catalyser l'oxydation sélective d'autres hydrocarbures.
En utilisant une plate-forme qu'ils ont développée appelée Système de catalyse sans contact (NCCS), les chercheurs ont testé l'efficacité d'un catalyseur à l'or contre l'éthylbenzène, un composé organique répandu dans la production de nombreux plastiques. Alors que l'éthylbenzène n'a subi aucune réaction en présence des amas d'or, l'équipe a découvert que lorsque les amas d'or réagissaient avec le cyclooctène, la molécule résultante a fourni l'intermédiaire nécessaire pour produire l'oxydation de l'éthylbenzène.
"Les deux réactions sont totalement indépendantes l'une de l'autre, " a déclaré Kung. "Nous avons vu que les nanoclusters d'or et le cyclooctène étaient inefficaces pour oxyder l'éthylbenzène à eux seuls. Le contact direct n'a pas provoqué la réaction. Ainsi, la réaction intermédiaire était nécessaire.
En démontrant comment des catalyseurs normalement inefficaces peuvent être rendus efficaces dans une réaction par un intermédiaire, les chercheurs pensent qu'il est possible de concevoir des systèmes utilisant des catalyseurs physiquement séparés d'un milieu réactionnel qui, autrement, endommagerait le catalyseur. Cette nouvelle approche pourrait fournir une solution de contournement efficace en matière d'assainissement de l'environnement, comme le nettoyage d'une rivière contaminée, où certains composants de l'eau peuvent être toxiques pour le catalyseur.
"Vous pouvez utiliser une membrane pour séparer le catalyseur du milieu, utiliser ensuite le catalyseur pour générer un intermédiaire pouvant traverser la membrane et dégrader le contaminant de manière plus sûre, " dit Kung.
Le travail ouvre également la porte à une plus grande liberté dans la production chimique industrielle. Une capacité à conduire des réactions couplées en parallèle sans les contraintes de la stoechiométrie traditionnelle - les relations strictes basées sur la quantité entre les produits de réaction - pourrait rendre les processus industriels de co-oxydation des hydrocarbures plus polyvalents, efficace, et rentable. Ces processus sont essentiels à la production d'essence et à la conversion du gaz naturel en carburant liquide et autres produits chimiques.
La prochaine étape de l'équipe de recherche consiste à déterminer la réactivité de l'or contre d'autres hydrocarbures de différentes forces de liaison. Ils espèrent également savoir si un phénomène similaire peut être appliqué à d'autres métaux, comme l'argent ou le cuivre.
"Nous n'en sommes pas encore là, mais une fois que nous comprenons la relation entre la réactivité des clusters d'or envers les hydrocarbures et les forces de liaison, nous pourrons prédire et concevoir d'autres systèmes de réactions chimiques, " dit Kung.