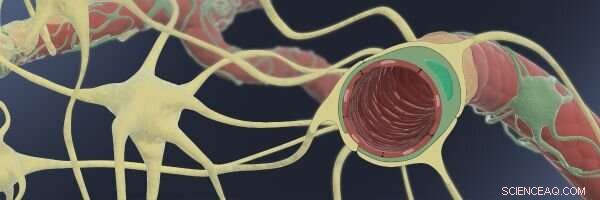
Cette illustration montre comment dans la barrière hémato-encéphalique (BBB), de fins capillaires endothéliaux (rouge) sont enveloppés de péricytes de support (vert) et d'astrocytes (jaune), leur permettant de générer une barrière étanche avec des fonctions de transport hautement sélectives pour les molécules entrant dans le liquide cérébral à partir de la circulation sanguine. Crédit :Institut Wyss de l'Université Harvard
Comme les barrières de sécurité aéroportuaires qui dégagent les voyageurs autorisés ou empêchent les voyageurs non autorisés et leurs bagages d'accéder aux zones d'opérations centrales, la barrière hémato-encéphalique (BHE) contrôle étroitement le transport des nutriments essentiels et des métabolites énergétiques dans le cerveau et évite les substances indésirables circulant dans la circulation sanguine. Surtout, sa structure hautement organisée de vaisseaux sanguins minces et de cellules de soutien est également le principal obstacle empêchant les médicaments vitaux d'atteindre le cerveau afin de traiter efficacement le cancer, neurodégénérescence, et d'autres maladies du système nerveux central. Dans un certain nombre de maladies du cerveau, le BBB peut également se décomposer localement, provoquant des substances neurotoxiques, les cellules sanguines et les agents pathogènes s'infiltrent dans le cerveau et causent des ravages irréparables.
Pour étudier la BHE et le transport de drogue à travers elle, les chercheurs se sont principalement appuyés sur des modèles animaux tels que les souris. Cependant, les fonctions précises de constitution et de transport des BHE dans ces modèles peuvent différer considérablement de celles des patients humains, ce qui les rend peu fiables pour la prédiction de l'administration de médicaments et de l'efficacité thérapeutique. De plus, les modèles in vitro tentant de recréer la BHE humaine à l'aide de cellules primaires dérivées de tissus cérébraux n'ont jusqu'à présent pas été en mesure d'imiter la barrière physique de la BHE, fonctions de transport, et les activités de navette de médicaments et d'anticorps suffisamment proches pour être utiles en tant qu'outils de développement thérapeutique.
Maintenant, une équipe dirigée par Donald Ingber, MARYLAND., doctorat au Wyss Institute for Biologically Inspired Engineering de Harvard a surmonté ces limitations en exploitant sa technologie d'organes sur puces microfluidiques (puces d'organes) en combinaison avec une approche imitant l'hypoxie inspirée du développement pour différencier les cellules souches pluripotentes humaines (iPS) en cellules endothéliales microvasculaires cérébrales cellules (BMVEC). La « puce BBB améliorée par l'hypoxie » qui en résulte récapitule l'organisation cellulaire, fonctions de barrière étroite et capacités de transport de la BHE humaine; et il permet le transport de médicaments et d'anticorps thérapeutiques d'une manière qui imite plus étroitement le transport à travers la BHE in vivo que les systèmes in vitro existants. Leur étude est rapportée dans Communication Nature .
"Notre approche de la modélisation de la navette des médicaments et des anticorps à travers la BHE humaine in vitro avec une fidélité aussi élevée et sans précédent présente une avancée significative par rapport aux capacités existantes dans ce domaine de recherche extrêmement difficile, " a déclaré Ingber, directeur fondateur du Wyss Institute. " Il répond à un besoin critique dans les programmes de développement de médicaments dans le monde pharmaceutique et biotechnologique que nous visons maintenant à surmonter avec un « programme de transport de la barrière hémato-encéphalique » dédié au Wyss Institute en utilisant notre talent unique et des ressources. » Ingber est également le professeur Judah Folkman de biologie vasculaire au HMS et le programme de biologie vasculaire du Boston Children's Hospital, ainsi que professeur de bio-ingénierie à SEAS.
La BHE est constituée de minces vaisseaux sanguins capillaires formés par les BMVEC, des cellules multifonctionnelles appelées péricytes qui s'enroulent autour de l'extérieur des vaisseaux, et les astrocytes en forme d'étoile, qui sont des cellules cérébrales non neuronales qui entrent également en contact avec les vaisseaux sanguins avec des processus semblables à ceux du pied. En présence de péricytes et d'astrocytes, les cellules endothéliales peuvent générer la barrière de paroi vasculaire hermétiquement scellée typique de la BHE humaine.
L'équipe d'Ingber a d'abord différencié les cellules iPS humaines en cellules endothéliales cérébrales dans la boîte de culture en utilisant une méthode qui avait été précédemment développée par le co-auteur Eric Shusta, Doctorat., Professeur de génie chimique et biologique à l'Université du Wisconsin-Madison, mais avec la puissance supplémentaire de la bioinspiration. "Parce que dans l'embryon, la BHE se forme dans des conditions de faible teneur en oxygène (hypoxie), nous avons différencié les cellules iPS pendant une période prolongée dans une atmosphère avec seulement 5% au lieu de la concentration normale en oxygène de 20%, " a déclaré le co-premier auteur Tae-Eun Park, doctorat "Par conséquent, les cellules iPS ont initié un programme de développement très similaire à celui de l'embryon, produisant des BMVEC qui présentaient une fonctionnalité plus élevée que les BMVEC générés dans des conditions normales d'oxygène.

Dans la puce BBB humaine améliorée, des cellules endothéliales dérivées de cellules souches pluripotentes humaines induites dans un processus inspiré du développement, former un microvaisseau dans le bas de deux canaux microfluidiques parallèles (images du bas), tandis que les péricytes et les astrocytes qui peuplent le canal supérieur se connectent au microvaisseau à travers une membrane poreuse en division. Crédit :Institut Wyss de l'Université Harvard
S'appuyant sur un modèle BBB humain précédent, les chercheurs ont ensuite transféré les BMVEC humaines induites par l'hypoxie dans l'un des deux canaux parallèles d'un dispositif microfluidique Organ-on-Chip qui sont divisés par une membrane poreuse et perfusés en continu avec du milieu. L'autre canal était peuplé d'un mélange de péricytes et d'astrocytes primaires du cerveau humain. Après une journée supplémentaire de traitement d'hypoxie, la puce BBB humaine pourrait être maintenue de manière stable pendant au moins 14 jours à des concentrations d'oxygène normales, ce qui est beaucoup plus long que les précédents modèles de BBB humains in vitro tentés dans le passé.
Sous la contrainte de cisaillement des fluides perfusant la puce BBB, les BMVEC forment ensuite un vaisseau sanguin, et développer une interface dense avec les péricytes s'alignant avec eux de l'autre côté de la membrane poreuse, ainsi qu'avec les astrocytes étendant les processus vers eux à travers de petites ouvertures dans la membrane. "La morphologie distincte de la BHE modifiée est parallèle à la formation d'une barrière plus étanche contenant un nombre élevé de systèmes de transport sélectif et de navette de médicament par rapport aux BBB de contrôle que nous avons générées sans hypoxie ni contrainte de cisaillement fluide, ou avec un endothélium dérivé de cerveau adulte au lieu de cellules iPS, " dit Nur Mustafaoglu, Doctorat., co-premier auteur de l'étude et chercheur postdoctoral travaillant dans l'équipe d'Ingber. "De plus, nous pourrions émuler les effets des stratégies de traitement chez les patients en clinique. Par exemple, nous avons ouvert la BHE de manière réversible pendant une courte période en augmentant la concentration d'un soluté de mannitol [osmolarité] pour permettre le passage de gros médicaments comme l'anticorps anticancéreux Cetuximab."
Pour fournir une preuve supplémentaire que la puce BBB humaine améliorée par l'hypoxie peut être utilisée comme un outil efficace pour étudier l'administration de médicaments au cerveau, l'équipe a étudié une série de mécanismes de transport qui empêchent les médicaments d'atteindre leurs cibles dans le cerveau en les refoulant dans la circulation sanguine (efflux), ou ça, en revanche, permettent le transport sélectif de nutriments et de médicaments à travers la BHE (transcytose).
"Lorsque nous avons spécifiquement bloqué la fonction de P-gp, une pompe à efflux endothéliale clé, nous pourrions augmenter considérablement le transport de la doxorubicine, un médicament anticancéreux, du canal vasculaire vers le canal cérébral, très similaire à ce qui a été observé chez les patients humains, " dit Park. " Ainsi, notre système in vitro pourrait être utilisé pour identifier de nouvelles approches pour réduire l'efflux et ainsi faciliter le transport des médicaments dans le cerveau à l'avenir. »
Sur un autre site, les développeurs de médicaments tentent d'exploiter la «transcytose médiée par les récepteurs» comme véhicule pour la navette des nanoparticules chargées de médicament, médicaments chimiques et protéiques plus gros, ainsi que des anticorps thérapeutiques à travers la BHE. "La puce BBB humaine améliorée par l'hypoxie récapitule la fonction des voies critiques de transcytose, tels que ceux utilisés par le LRP-1 et les récepteurs de la transferrine responsables de l'absorption des lipoprotéines vitales et du fer du sang circulant et de leur libération dans le cerveau de l'autre côté de la BHE. En exploitant ces récepteurs à l'aide de différentes stratégies précliniques, nous pouvons imiter fidèlement la navette précédemment démontrée d'anticorps thérapeutiques ciblant les récepteurs de la transferrine in vivo, tout en maintenant l'intégrité de la BHE in vitro, " dit Mustafaoglu.
Sur la base de ces constatations, le Wyss Institute a lancé un « programme de transport de la barrière hémato-encéphalique ». "Initialement, le programme BBB Transport vise à découvrir de nouvelles cibles navettes enrichies sur la surface vasculaire du BMVEC, en utilisant une nouvelle transcriptomique, protéomique, et les approches cellulaires iPS. En parallèle, nous développons des navettes d'anticorps entièrement humains dirigées contre des cibles de navettes connues avec des capacités améliorées de ciblage du cerveau, " dit James Gorman, MARYLAND., Doctorat., le chef du personnel du programme de transport BBB en collaboration avec Ingber. "Nous visons à collaborer avec de multiples partenaires biopharmaceutiques dans une relation pré-concurrentielle pour développer des navettes offrant une efficacité et une flexibilité d'ingénierie exceptionnelles pour l'incorporation dans des médicaments à base d'anticorps et de protéines, parce que c'est tellement nécessaire par les patients et l'ensemble du domaine".
Les auteurs pensent qu'en plus des études de développement de médicaments, la puce BBB humaine améliorée par l'hypoxie peut également être utilisée pour modéliser des aspects des maladies du cerveau qui affectent la BHE telles que la maladie d'Alzheimer et la maladie de Parkinson, et aux approches avancées de médecine personnalisée en utilisant des cellules iPS dérivées de patients.