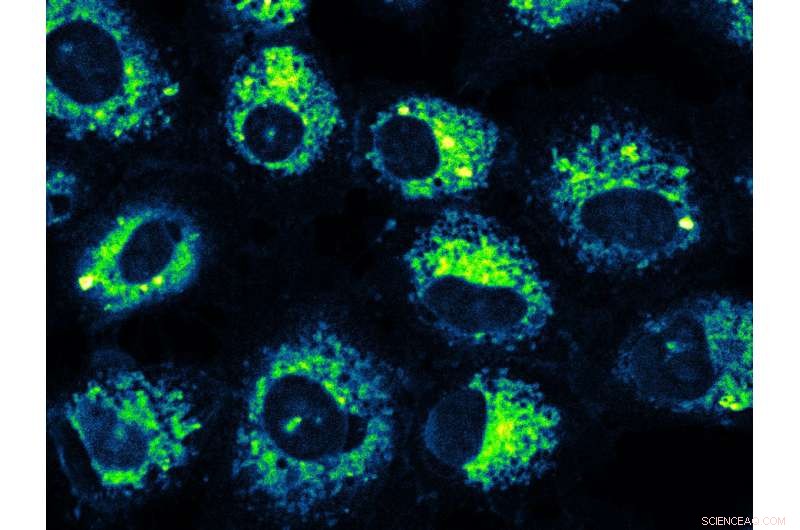
Une image microscopique de cellules cancéreuses pulmonaires humaines, dans lequel la molécule développée par l'Utah State University transportant du monoxyde de carbone cible les mitochondries, comme le révèle la couleur jaune-vert brillant. Crédit :Université d'État de l'Utah
Il y a environ quatre ans, La chimiste de l'Utah State University, Lisa Berreau, a posé une question à la collègue et toxicologue de l'USU, Abby Benninghoff.
"Mes étudiants et moi avions développé une nouvelle molécule de flavonoïde qui pourrait libérer du monoxyde de carbone, " se souvient Berreau. " Et nous cherchions une réponse à la question, « Est-ce que cela pourrait tuer les cellules cancéreuses ? » »
La réponse courte de Benninghoff ? Oui. Mais comme dans de nombreuses activités scientifiques, la question a soulevé plus de questions et a lancé un effort interdisciplinaire pour explorer les nuances de la libération contrôlée de monoxyde de carbone dans les cellules.
Berreau et Benninghoff, avec leurs élèves Marina Popova, Tatiana Soboleva, Hector Esquer et Stacey Anderson, ainsi que son collègue Suliman Ayad de la Florida State University, attirent l'attention internationale avec leurs conclusions. L'équipe a récemment publié les résultats de ses études dans la revue American Chemical Society Biologie chimique et dans le Journal de l'American Chemical Society .
La recherche de l'équipe est soutenue par les National Institutes of Health, la Station d'expérimentation agricole de l'Utah et le Bureau de la recherche et des études supérieures de l'USU.
Libération de monoxyde de carbone, également connu sous le nom de CO, semble probablement un peu effrayant. Après tout, nous équipons nos maisons de détecteurs de monoxyde de carbone pour éviter les accidents tragiques. Nous veillons à ne pas faire tourner les voitures au ralenti dans des espaces clos. Encore, le gaz redoutable est produit par notre propre corps, bien qu'en petites quantités, et peut être un antidote clé à des maladies modernes comme le cancer, inflammation et hypertension.
Comme de nombreuses substances, y compris les exemples moins menaçants de l'eau et de l'oxygène, trop de monoxyde de carbone est une mauvaise chose. Mais un peu pourrait être une bouée de sauvetage.
"Cette ecchymose sur votre peau - c'est la preuve d'une voie biochimique, où le CO est libéré, " dit Berreau, vice-président associé pour la recherche à l'Utah State et professeur au département de chimie et de biochimie de l'USU.
Les molécules spécifiques des scientifiques de l'USU pour la libération de CO sont uniques, dans les tentatives précédentes de développer des molécules libérant du monoxyde de carbone, connu sous le nom de « CORM », " ont utilisé des structures contenant du métal.
De gauche, Abby Benninghoff, scientifiques de l'Université d'État de l'Utah, Tatiana Soboleva, Marina Popova et Lisa Berreau développent des molécules pour fournir des quantités contrôlées de monoxyde de carbone à des cibles dans le corps humain. Crédit :Mary-Ann Muffoletto
« L'utilisation de métaux suscite des inquiétudes en raison d'une possible toxicité, " dit Berreau.
La molécule développée par USU est dérivée de pigments organiques appelés flavonoïdes, qui se produisent naturellement dans des aliments tels que les baies et le cacao.
Parmi les défis liés au développement des molécules et à l'exploitation du pouvoir de guérison du CO, figure la manière de fournir le gaz potentiellement bénéfique en toute sécurité, quantités souhaitées vers des sites spécifiquement ciblés dans le corps.
"Une caractéristique de nos molécules est qu'elles ne libèrent de monoxyde de carbone que lorsqu'elles sont déclenchées par la lumière visible, " dit Berreau.
C'est une partie "unique et excitante" des efforts de l'USU, dit Benninghoff, professeur agrégé au Département des animaux de l'USU, Sciences laitières et vétérinaires et École de médecine vétérinaire. "Notre base de flavonoïdes, les photoCORM organiques sont traçables, ciblables et déclenchables."
Les doctorants Popova et Soboleva se penchent sur ce qui se passe aux niveaux cellulaire et moléculaire, que le CO est libéré et diffuse dans les cellules.
En utilisant la microscopie à fluorescence, Popova, auteur principal de la JACS papier, fait la démonstration d'une livraison ciblée de CO par des photoCORM aux cellules cancéreuses, ainsi que la capacité des photoCORMs à produire des effets anti-inflammatoires significatifs.
"Nous affinons notre structure moléculaire pour permettre un meilleur contrôle de la libération de CO pour produire des effets biologiques plus ciblés et précis, " elle dit.
Soboleva, un USU Presidential Graduate Research Fellow et auteur principal du ACS Biologie Chimique papier, étudie le comportement du photoCORM au niveau mitochondrial. Elle a récemment reçu une bourse compétitive de l'American Health Association, ce qui lui permettra d'explorer davantage l'utilisation des photoCORM pour lutter contre l'inflammation, un fléau de santé publique d'aujourd'hui lié à un large éventail de maladies chroniques, comprennent les maladies cardiaques et le diabète.
"Notre collaboration interdisciplinaire nous a permis d'accomplir bien plus que ce que nous aurions pu faire dans notre propre laboratoire, " dit Berreau, qui détient le brevet sur le photoCORM développé par USU. "C'est pourquoi la collaboration est importante. Nous apportons une expertise complémentaire dans le développement de molécules libérant du CO pour des applications thérapeutiques potentielles."