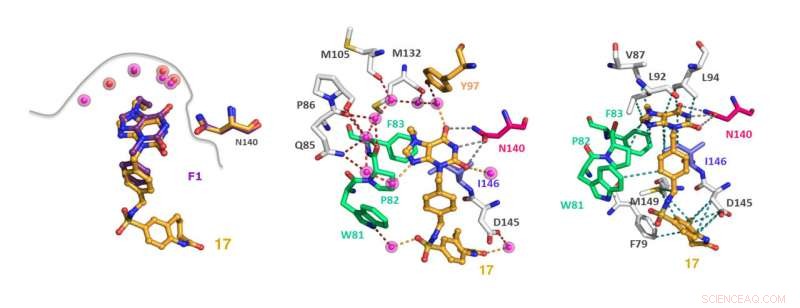
Comparaison du mode de liaison de la F1 et du composé 17. Crédit :Université Lobatchevsky
La recherche de nouvelles molécules médicinales aux propriétés prédéterminées est un complexe, processus coûteux et chronophage, surtout en oncologie. La science moderne nous permet d'accélérer cette recherche grâce à l'utilisation de la technologie informatique et à l'introduction de processus automatisés. Dans le développement de molécules biologiquement actives, il existe deux concepts de base :une molécule médicinale et une cible thérapeutique.
La molécule se lie à la cible, le plus souvent une protéine, affectant ainsi certaines fonctions cellulaires. Si la cible thérapeutique est connue, Ensuite, la première étape de la conception d'un nouveau médicament consiste à rechercher de petites molécules pouvant interagir avec la cible. Les molécules sont sélectionnées dans d'immenses bibliothèques chimiques virtuelles, qui comprennent des millions de composés.
Au cours de la dernière décennie, le processus de sélection de molécules médicinales potentielles a été grandement simplifié par l'introduction du criblage robotisé à haut débit, qui permet de tester des milliers de composés en peu de temps.
Prototypes composés qui ont été criblés lors du criblage à haut débit, bien que capable d'interagir avec la protéine d'intérêt, sont encore loin d'être le médicament final et ne peuvent pas être utilisés immédiatement dans les essais précliniques et cliniques.
Pour commencer les études précliniques, les molécules biologiquement actives doivent répondre à un certain nombre de critères, comme une activité élevée par rapport à la protéine cible, l'absence d'effet sur d'autres cibles, et une bonne pharmacocinétique, c'est-à-dire la capacité de la molécule à pénétrer dans le corps, y être distribué, être éliminé du corps et n'avoir aucun effet toxique sur celui-ci. A la recherche d'une molécule répondant à tous les critères nécessaires, les composés prototypes subissent une phase d'optimisation, ce qui est également assez coûteux et prend du temps.
Selon Alexeï Fedorov, Chef du département de chimie organique de l'Université Lobatchevsky, le groupe de recherche international a développé une stratégie pour accélérer et automatiser considérablement le processus d'optimisation des prototypes de molécules. De telles molécules deviennent alors des candidats pour des essais précliniques ultérieurs.
« Dans cette approche, nous avons combiné la conception d'une chimiothèque focalisée sur la cible thérapeutique d'intérêt, criblage virtuel (informatique) de la bibliothèque obtenue, ainsi que la synthèse automatisée et l'étude de l'activité biologique des molécules résultantes in vitro, " note Alexeï Fedorov
A la première étape de cette démarche, le modèle d'interaction de la molécule prototype choisie avec la cible est déterminé par analyse par diffraction des rayons X. Puis, sur la base des données obtenues, une nouvelle chimiothèque virtuelle est conçue. Dans ce cas, la molécule prototype est le bloc de construction principal, auxquels sont ajoutés de nouveaux composants correspondant à la structure de la protéine cible.
Intégrer des briques élémentaires dans de nouvelles molécules, Des réactions chimiques soigneusement sélectionnées sont utilisées qui répondent aux exigences de la chimie médicale. La sélection des réactions chimiques garantit que les composés d'une nouvelle chimiothèque peuvent être facilement obtenus par des méthodes de chimie organique en une ou deux étapes avec des rendements élevés et sans sous-produits.
L'étape suivante consiste en un criblage informatique de la banque virtuelle obtenue afin de sélectionner les molécules capables d'une interaction optimale avec la cible et possédant les propriétés nécessaires, comme la solubilité, biodisponibilité, toxicité, etc. Tout cela augmente considérablement les chances de trouver un candidat potentiel pour le rôle de molécule médicinale.
Finalement, les composés sélectionnés au cours du criblage informatique sont synthétisés, et leurs propriétés biologiques sont testées in vitro. Ces deux processus peuvent désormais être entièrement automatisés et peuvent être exécutés par des robots, ce qui réduit considérablement le temps de développement de nouveaux composés médicamenteux.
L'efficacité de la stratégie proposée a été démontrée en optimisant les substances antitumorales, inhibiteurs des protéines contenant du bromodomaine. Cette classe de protéines est impliquée dans la régulation d'un certain nombre de gènes qui jouent un rôle clé dans le développement du cancer.
"Plus tôt, notre groupe a identifié une molécule prototype capable d'interagir efficacement avec cette cible thérapeutique. L'optimisation du prototype à l'aide de la technique décrite a permis d'obtenir plusieurs molécules candidates qui se lient 60 fois mieux à la cible. Ils ont également montré une meilleure sélectivité, solubilité dans l'eau, et l'efficacité des tests en cellule. Actuellement, les molécules sont en préparation pour des essais précliniques pour traiter différents types de tumeurs, " conclut le professeur Fedorov.
Maintenant, la conception ciblée de nouvelles molécules médicinales est devenue une partie importante de la pharmacologie. Le passage d'une méthode d'essais et d'erreurs à une conception vraiment rationnelle des médicaments, obtenu grâce à l'introduction d'approches informatiques et robotiques en chimie médicale, ouvre la voie à une production plus efficace et plus rapide de nouvelles molécules médicinales possédant les propriétés physico-chimiques et l'action biologique souhaitées.