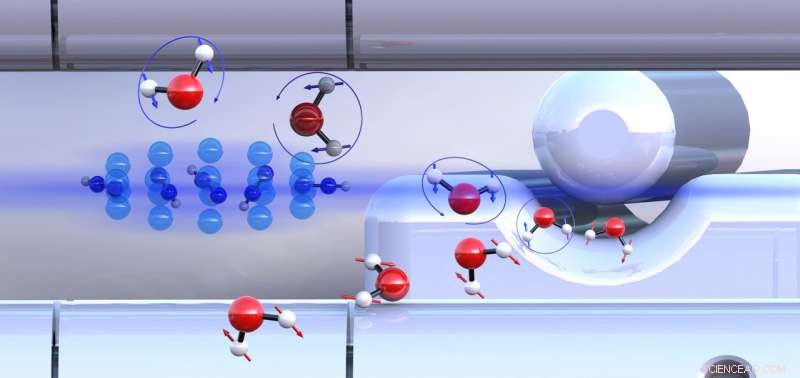
Les molécules d'ortho-eau et de para-eau pré-triées avec des spins nucléaires orientés différemment (flèches bleues ou rouges) réagissent avec les ions diazénylium (centre gauche) à des vitesses différentes. Crédit :Université de Bâle
Les molécules d'eau existent sous deux formes différentes avec des propriétés physiques presque identiques. Pour la première fois, des chercheurs ont réussi à séparer les deux formes pour montrer qu'elles peuvent présenter des réactivités chimiques différentes. Ces résultats ont été rapportés par des chercheurs de l'Université de Bâle et leurs collègues de Hambourg dans la revue scientifique Communication Nature .
D'un point de vue chimique, l'eau est une molécule dans laquelle un seul atome d'oxygène est lié à deux atomes d'hydrogène. Il est moins connu que l'eau existe sous deux formes différentes (isomères) au niveau moléculaire. La différence réside dans l'orientation relative des spins nucléaires des deux atomes d'hydrogène. Selon que les rotations sont alignées dans le même sens ou dans le sens opposé, on se réfère à l'ortho- ou para-eau.
Expériences avec des molécules d'eau triées
Le groupe de recherche dirigé par le professeur Stefan Willitsch du département de chimie de l'Université de Bâle a étudié comment les deux formes d'eau diffèrent en termes de réactivité chimique - leur capacité à subir une réaction chimique. Les deux isomères ont des propriétés physiques presque identiques, ce qui rend leur séparation particulièrement difficile.
Cette séparation a été rendue possible par une méthode basée sur les champs électriques développée par le professeur Jochen Küpper du Centre de Hambourg pour la science des lasers à électrons libres. En utilisant cette approche, les chercheurs ont pu initier des réactions contrôlées entre les isomères d'eau "pré-triés" et les ions diazénylium ultrafroids ("azote protoné") retenus dans un piège. Au cours de ce processus, un ion diazénylium transfère son proton à une molécule d'eau. Cette réaction est également observée dans la chimie de l'espace interstellaire.
Réactivité accrue
Il a été démontré que la para-eau réagit environ 25 pour cent plus rapidement que l'ortho-eau. Cet effet peut être expliqué en termes de spin nucléaire influençant également la rotation des molécules d'eau. Par conséquent, différentes forces d'attraction agissent entre les partenaires de réaction. L'eau para est capable d'attirer son partenaire de réaction plus fortement que la forme ortho, ce qui entraîne une augmentation de la réactivité chimique. Des simulations informatiques ont confirmé ces résultats expérimentaux.
Dans leurs expériences, les chercheurs ont travaillé avec des molécules à des températures très basses proches du zéro absolu (environ -273°C). Ce sont des conditions idéales pour préparer avec précision les états quantiques individuels et définir le contenu énergétique des molécules, et de provoquer une réaction contrôlée entre eux. Willitsch explique la démarche expérimentale :« Mieux on maîtrise les états des molécules impliquées dans une réaction chimique, mieux les mécanismes sous-jacents et la dynamique d'une réaction peuvent être étudiés et compris."