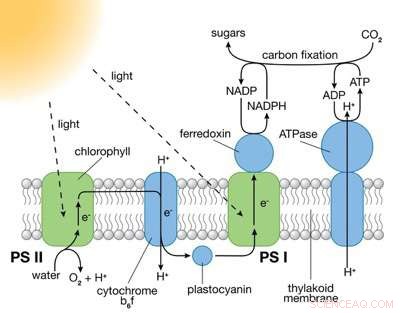
Les photosystèmes (PS) I et II sont de grands complexes protéiques qui contiennent des molécules de pigment absorbant la lumière nécessaires à la photosynthèse. PS II capte l'énergie de la lumière du soleil pour extraire les électrons des molécules d'eau, fractionnement de l'eau en ions oxygène et hydrogène (H+) et production d'énergie chimique sous forme d'ATP. PS I utilise ces électrons et H+ pour réduire le NADP+ (une molécule porteuse d'électrons) en NADPH. L'énergie chimique contenue dans l'ATP et le NADPH est ensuite utilisée dans la réaction indépendante de la lumière de la photosynthèse pour convertir le dioxyde de carbone en sucres. Crédit :Laboratoire national de Brookhaven
La photosynthèse des plantes vertes convertit l'énergie solaire en énergie chimique stockée en transformant le dioxyde de carbone atmosphérique et l'eau en molécules de sucre qui alimentent la croissance des plantes. Les scientifiques ont essayé de reproduire artificiellement ce processus de conversion d'énergie, dans le but de produire des carburants respectueux de l'environnement et durables, comme l'hydrogène et le méthanol. Mais imitant les fonctions clés du centre photosynthétique, où des biomolécules spécialisées effectuent la photosynthèse, s'est avéré difficile. La photosynthèse artificielle nécessite de concevoir un système moléculaire capable d'absorber la lumière, transport et charge électrique séparée, et catalyser les réactions productrices de carburant, tous des processus complexes qui doivent fonctionner de manière synchrone pour atteindre une efficacité de conversion d'énergie élevée.
Maintenant, des chimistes du Brookhaven National Laboratory du Département de l'énergie des États-Unis (DOE) et de Virginia Tech ont conçu deux photocatalyseurs (matériaux qui accélèrent les réactions chimiques lors de l'absorption de la lumière) qui incorporent des composants individuels spécialisés pour l'absorption de la lumière, séparation des charges, ou catalyse en une seule "supramolécule". Dans les deux systèmes moléculaires, plusieurs centres de collecte de lumière constitués d'ions métalliques ruthénium (Ru) sont connectés à un seul centre catalytique constitué d'ions métalliques rhodium (Rh) par l'intermédiaire d'une molécule de pontage qui favorise le transfert d'électrons des centres Ru vers le catalyseur Rh, où l'hydrogène est produit.
Ils ont comparé les performances de production d'hydrogène et analysé les propriétés physiques des supramolécules, comme décrit dans un article publié dans l'édition en ligne du 1er juin de Journal de l'American Chemical Society , comprendre pourquoi le photocatalyseur avec six absorbeurs de lumière Ru produit plus d'hydrogène et reste stable plus longtemps.
« Le développement de systèmes moléculaires efficaces pour la production d'hydrogène est difficile car les processus se déroulent à des rythmes différents, " a déclaré l'auteur principal Gerald Manbeck, un chimiste dans le groupe de photosynthèse artificielle au Brookhaven Lab. « L'achèvement du renouvellement catalytique de l'hydrogène avant que les charges séparées – l'électron excité par la lumière et chargé négativement et le « trou » positif » laissés après que la molécule excitée ait absorbé l'énergie lumineuse – aient une chance de se recombiner et de produire inutilement de la chaleur est l'un des principaux défis. "
Une autre complication est que deux électrons sont nécessaires pour produire chaque molécule d'hydrogène. Pour que la catalyse se produise, le système doit être capable de retenir le premier électron assez longtemps pour que le second apparaisse. "En construisant des supramolécules avec de multiples absorbeurs de lumière qui peuvent fonctionner indépendamment, nous augmentons la probabilité d'utiliser chaque électron de manière productive et améliorons la capacité des molécules à fonctionner dans des conditions de faible luminosité, " dit Manbeck.
Manbeck a commencé à fabriquer les supramolécules à Virginia Tech en 2012 avec feu Karen Brewer, co-auteur et son conseiller postdoctoral. Il a découvert que le système à quatre métaux (tétramétallique) avec trois centres absorbant la lumière Ru et un centre catalytique Rh ne produisait que 40 molécules d'hydrogène pour chaque molécule de catalyseur et cessait de fonctionner après environ quatre heures. En comparaison, le système à sept métaux (heptamétallique) avec six centres Ru et un centre Rh était plus de sept fois plus efficace, cycle 300 fois pour produire de l'hydrogène pendant 10 heures. Cette grande disparité d'efficacité et de stabilité était déroutante car les supramolécules contiennent des composants très similaires.
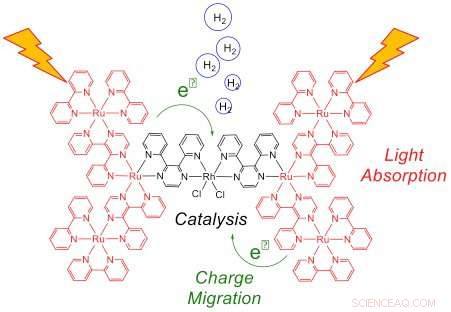
Cette représentation du système heptamétallique lors de l'exposition à la lumière montre la récolte de lumière par les six centres Ru (rouge) et le transfert d'électrons vers le catalyseur Rh (noir), où l'hydrogène est produit. Un transfert d'électrons efficace vers Rh est essentiel pour obtenir des performances catalytiques élevées. Crédit :Laboratoire national de Brookhaven
Manbeck a rejoint Brookhaven en 2013 et a depuis réalisé une série d'expériences avec le co-auteur Etsuko Fujita, leader du groupe photosynthèse artificielle, comprendre les causes fondamentales de la différence de performance.
"La capacité à former l'état à charges séparées est un indicateur partiel de la capacité d'une supramolécule à être un bon photocatalyseur, mais réaliser une séparation de charge efficace nécessite un réglage fin de l'énergétique de chaque composant, " a déclaré Fujita. " Pour promouvoir la catalyse, le catalyseur Rh doit être suffisamment faible en énergie pour accepter les électrons des absorbeurs de lumière Ru lorsque les absorbeurs sont exposés à la lumière."
Par voltamétrie cyclique, une technique électrochimique qui montre les niveaux d'énergie dans une molécule, les scientifiques ont découvert que le catalyseur Rh du système heptamétallique est légèrement plus pauvre en électrons et donc plus réceptif à recevoir des électrons que son homologue du système tétramétallique. Ce résultat suggère que le transfert de charge est favorable dans le système heptamétallique mais pas dans le système tétramétallique.
Ils ont vérifié leur hypothèse avec une technique résolue en temps appelée spectroscopie d'absorption transitoire nanoseconde, dans lequel une molécule est promue à un état excité par une impulsion laser intense et la décroissance de l'état excité est mesurée au fil du temps. Les spectres résultants ont révélé la présence d'un transfert de charge Ru-à-Rh dans le système heptamétallique uniquement.
"Les données ont non seulement confirmé notre hypothèse, mais ont également révélé que la séparation des charges à l'état excité se produit beaucoup plus rapidement que nous ne l'avions imaginé, " dit Manbeck. " En fait, la migration de charge se produit plus rapidement que la résolution temporelle de notre instrument, et implique probablement de courte durée, états excités à haute énergie. » Les chercheurs prévoient de rechercher un collaborateur avec une instrumentation plus rapide qui peut mesurer le taux exact de séparation des charges pour aider à clarifier le mécanisme.
Dans une expérience de suivi, les scientifiques ont effectué la mesure d'absorption transitoire dans des conditions opératoires photocatalytiques, with a reagent used as the ultimate source of electrons to produce hydrogen (a scalable artificial photosynthesis of hydrogen fuel from water would require replacing the reagent with electrons released during water oxidation). The excited state generated by the laser pulse rapidly accepted an electron from the reagent. They discovered that the added electron resides on Rh in the heptametallic system only, further supporting the charge migration to Rh predicted by cyclic voltammetry.
"The high photocatalytic turnover of the heptametallic system and the principles governing charge separation that were uncovered in this work encourage further studies using multiple light-harvesting units linked to single catalytic sites, " said Manbeck.