Les médicaments antibiotiques sont devenus un traitement populaire contre les infections bactériennes au début du XXe siècle et sont apparus comme un outil de transformation de la santé humaine. Au milieu du siècle, de nouveaux antibiotiques ont été régulièrement développés pendant l'âge d'or du médicament.
Mais ensuite les bactéries ont évolué. Ils ont trouvé de nouveaux moyens d’échapper aux traitements antibiotiques, rendant nombre d’entre eux inutiles. À mesure que les nouvelles sources d'antibiotiques se tarissaient, les infections bactériennes se sont transformées en la crise sanitaire mondiale actuelle de résistance aux antibiotiques.
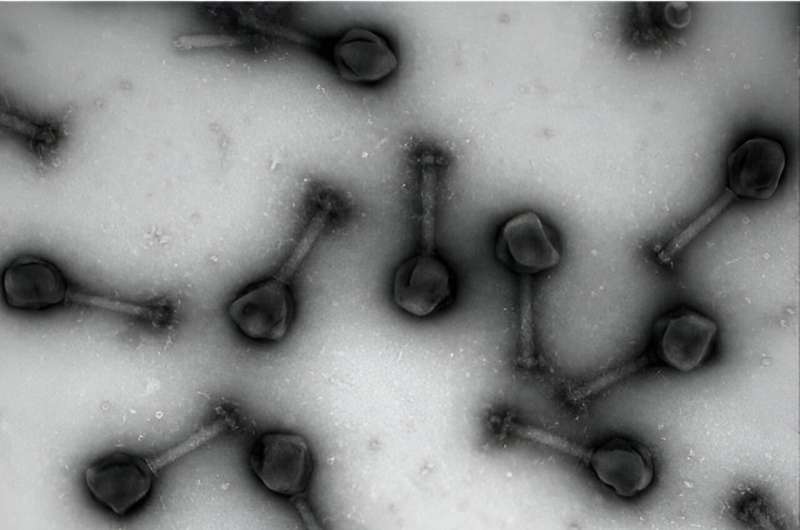
Les scientifiques se tournent désormais vers un allié inhabituel, les virus, pour les aider à contrer cette menace croissante. Récemment, les chercheurs se sont concentrés sur les virus appelés bactériophages comme nouvel outil pour traiter et désarmer les bactéries résistantes aux antibiotiques. Une attention particulière a été accordée aux phages « géants » (des virus récemment découverts dotés de génomes extrêmement volumineux) qui pourraient être exploités comme agents d'administration spéciaux capables non seulement de tuer les bactéries, mais également conçus pour délivrer des antibiotiques directement à la source de l'infection. P>
Mais afin de proposer de nouvelles thérapies grâce aux phages, les scientifiques doivent d'abord comprendre la composition biologique extraordinaire et les mécanismes à l'intérieur de ces mystérieux virus.
Les chercheurs de l'École des sciences biologiques de l'Université de Californie à San Diego et leurs collègues de l'Innovative Genomics Institute de l'UC Berkeley et de l'Université Chulalongkorn de Bangkok ont fait un pas en avant substantiel dans le déchiffrement de plusieurs fonctions clés des phages géants.
"Ces phages géants ont de grands génomes qui pourraient en théorie être manipulés pour transporter des charges utiles qui tuent plus efficacement les bactéries", a déclaré Joe Pogliano, professeur à l'École des sciences biologiques de l'UC San Diego et auteur principal d'un nouvel article publié dans le Actes de l'Académie nationale des sciences . "Le problème est que leur génome est enfermé, donc il n'est pas facile d'y accéder. Mais maintenant nous avons découvert certains de ses éléments clés."
Comme décrit dans l'article, la recherche menée par Chase Morgan, étudiant diplômé de l'École des sciences biologiques, s'est concentrée sur les phages géants des Chimalliviridae qui se répliquent à l'intérieur des bactéries en formant un compartiment qui ressemble au noyau à l'intérieur des cellules des humains et d'autres organismes vivants. Le compartiment semblable au noyau des Chimalliviridae sépare et importe sélectivement certaines protéines qui lui permettent de se répliquer à l'intérieur de la bactérie hôte. Mais la façon dont ce processus se déroule était une partie déroutante du processus.
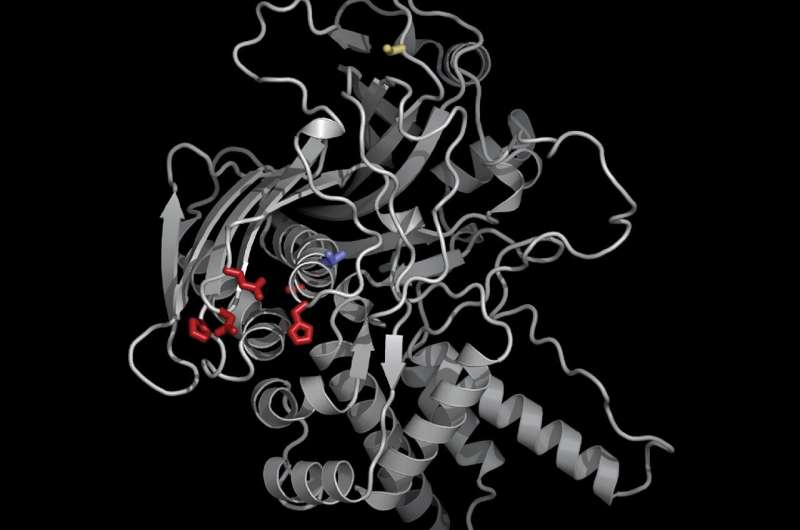
À l'aide de nouveaux outils génétiques et de biologie cellulaire, Morgan et ses collègues ont identifié une protéine clé, qu'ils ont nommée « importateur de protéines des chimallivirus A », ou PicA, qui agit comme une sorte de videur de boîte de nuit, transportant sélectivement les protéines en permettant l'entrée à l'intérieur du noyau pour certains mais en refusant l’accès à d’autres. PicA, ont-ils découvert, coordonne le trafic de protéines cargo à travers la coque protectrice du noyau du phage.
"Le simple fait que ce virus soit capable de mettre en place cette structure et ce système de transport incroyablement complexes est vraiment incroyable et nous n'en avons jamais vu auparavant", a déclaré Morgan. "Ce que nous considérons comme une biologie complexe est généralement réservé aux formes de vie supérieures avec des humains et nos dizaines de milliers de gènes, mais nous observons ici des processus fonctionnellement analogues dans un génome viral relativement petit de seulement environ 300 gènes. C'est probablement le système sélectif le plus simple. système de transport que nous connaissons."
Grâce à CRISPRi-ART, un outil d'ARN programmable pour étudier les génomes, les chercheurs ont pu démontrer que PicA est un composant essentiel du processus de développement et de réplication du noyau des Chimalliviridae.
"Sans la simplicité et la polyvalence des technologies CRISPR ciblant l'ARN, il serait presque impossible de poser directement ces questions et d'y répondre. Nous sommes vraiment ravis de voir comment ces outils dévoilent les mystères codés par les génomes des phages", a déclaré le co-auteur Ben Adler, chercheur postdoctoral travaillant sous la direction de Jennifer Doudna, pionnière du CRISPR, lauréate du prix Nobel.
Les bactéries et les virus se sont engagés dans une sorte de course aux armements depuis des milliards d’années, chacun évoluant pour contrer les adaptations des autres. Les chercheurs affirment que le système de transport sophistiqué PicA est le résultat de cette concurrence évolutive intense et continue. Le système a évolué pour être à la fois très flexible et hautement sélectif, n’autorisant que les éléments bénéfiques clés à l’intérieur du noyau. Sans le système PicA, les protéines défensives de la bactérie pénétreraient à l'intérieur et saboteraient le processus de réplication du virus.
Ces informations sont vitales alors que les scientifiques de l'Emerging Pathogens Initiative et du Center for Innovative Phage Applications and Therapeutics de l'UC San Diego s'efforcent de jeter les bases d'une éventuelle programmation génétique des phages pour traiter une variété de maladies mortelles.
"Nous ne comprenions vraiment pas comment fonctionnait le système d'importation de protéines ni quelles protéines étaient impliquées auparavant. Cette recherche est donc la première étape dans la compréhension d'un processus clé qui est essentiel à la réplication réussie de ces phages", a déclaré l'École des sciences biologiques. Emily Armbruster, étudiante diplômée, co-auteure de l'article. "Plus nous comprendrons ces systèmes essentiels, mieux nous serons en mesure de concevoir des phages à des fins thérapeutiques."
Les futures cibles de ces virus génétiquement programmés comprennent la bactérie Pseudomonas aeruginosa, connue pour provoquer des infections potentiellement mortelles et présenter des risques pour les patients hospitalisés. D'autres cibles prometteuses incluent E. coli et Klebsiella, qui peuvent provoquer des infections chroniques et récurrentes et, dans certains cas, pénétrer dans la circulation sanguine, ce qui peut mettre la vie en danger.
Plus d'informations : Chase J. Morgan et al, Une voie d'importation de protéines essentielle et hautement sélective codée par un phage formateur de noyau, Actes de l'Académie nationale des sciences (2024). DOI :10.1073/pnas.2321190121
Informations sur le journal : Actes de l'Académie nationale des sciences
Fourni par l'Université de Californie - San Diego