Les scientifiques de Northwestern Medicine ont développé un moyen plus efficace de créer des vaccins et des médicaments nanothérapeutiques, selon une nouvelle étude publiée dans ACS Nano .
"Au cours de la dernière décennie, la technologie de l'acide nucléique sphérique, ou SNA, est devenue une vaste plateforme thérapeutique pour une grande variété de maladies, notamment le cancer et d'autres maladies", a déclaré Chad Mirkin, Ph.D., professeur de médecine à la Division. d'hématologie et d'oncologie, professeur de chimie George B. Rathmann au Weinberg College of Arts and Sciences de Northwestern et directeur de l'Institut international de nanotechnologie, qui était l'auteur principal de l'étude.
Dans le laboratoire Mirkin, les chercheurs ont exploité cette technologie SNA dans leurs travaux pour concevoir des nanomédicaments de précision destinés à être utilisés dans la régulation des gènes et dans l'immunothérapie du cancer avec des effets secondaires indésirables limités grâce à un processus de développement systématique connu sous le nom de vaccinologie rationnelle.
"Dans le développement de vaccins, historiquement, très peu d'attention a été accordée à la structure des vaccins", a déclaré Mirkin, qui est également membre du Robert H. Lurie Comprehensive Cancer Center de l'Université Northwestern. "Tout l'accent a été mis sur les composants. Le principe de la vaccinologie rationnelle est que, même si les composants sont essentiels, la structure est tout aussi importante. La façon dont vous présentez les composants du vaccin dans une architecture modulaire à l'échelle nanométrique peut avoir un impact considérable sur l'efficacité du vaccin, qu'il s'agisse de traiter une maladie infectieuse ou un cancer."
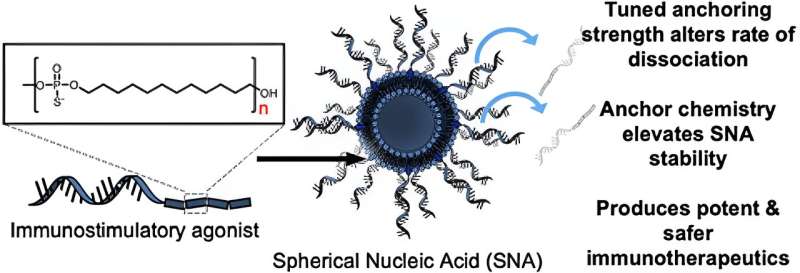
Dans l'étude, les chercheurs ont d'abord testé les effets de l'utilisation de différents groupes d'ancrage chimiques pour attacher les oligonucléotides (courts brins d'ADN ou d'ARN) à la surface des liposomes afin de préparer les SNA. Ils ont constaté que lorsque des groupes d’ancrage à base de dodécane de plus en plus hydrophobes étaient utilisés, la stabilité de la nanostructure était considérablement améliorée. Lorsqu'elles ont été introduites dans des cellules dendritiques de souris dérivées de la moelle osseuse, ces constructions de SNA plus stables ont présenté une absorption cellulaire améliorée par rapport aux autres versions de SNA préparées à l'aide d'autres types de groupes d'ancrage, avec des compositions chimiques différentes.
"Nous avons découvert un moyen d'ancrer les oligonucléotides à la surface de la particule, ce qui modifie la stabilité globale de la construction SNA, ce qui est essentiel", a déclaré Jasper Dittmar, titulaire d'un doctorat. étudiant au laboratoire Mirkin et co-auteur de l’étude. "La beauté de l'architecture SNA est qu'elle est reconnue par presque tous les types de cellules, y compris les cellules immunitaires, et rapidement internalisée. Vous faites pénétrer le vaccin dans les cellules importantes à la stœchiométrie souhaitée, avec le nombre souhaité d'antigènes et molécules adjuvantes."
Les scientifiques du laboratoire Mirkin ont ensuite chargé le vaccin SNA avec OVA1 (un peptide modèle dérivé de la protéine d'œuf souvent utilisé dans le développement de vaccins) et l'ont administré à des souris atteintes de lymphome. Les souris traitées avec OVA1 SNA présentaient non seulement un plus grand nombre de lymphocytes T polyfonctionnels (qui sont considérés comme puissants contre les infections chroniques et les tumeurs), mais elles présentaient également une réduction de 21 fois du volume des tumeurs par rapport aux souris traitées avec une solution saline, selon l'étude. étudier.
Pour évaluer les effets secondaires inflammatoires du vaccin, les enquêteurs ont ensuite étudié le SNA pour voir s’il activait des réponses immunitaires excessives chez la souris. Les souris ayant reçu le traitement n'ont pas produit de tempête de cytokines, un effet secondaire parfois mortel des immunothérapies.
Étant donné que les tempêtes de cytokines sont associées à des cas graves de COVID-19, Mirkin et son équipe de recherche ont également créé un vaccin SNA dans lequel le peptide OVA1 a été remplacé par un peptide du virus responsable du COVID-19 (peptide CoV) et administré à l'homme. cellules et finalement des souris. Les enquêteurs ont découvert que le vaccin améliorait les réponses immunitaires anti-COVID spécifiques à l'antigène avec un minimum d'effets secondaires indésirables.
"Pris ensemble, les résultats de cette étude jettent les bases d'une nouvelle façon de développer et de fournir des vaccins et d'autres traitements de précision, quelle que soit la maladie cible", a déclaré Michael Evangelopoulos, titulaire d'un doctorat. étudiant du laboratoire Mirkin et co-auteur de l'étude.
Les résultats soulignent également l'importance de la construction de vaccins, a déclaré Mirkin.
"La structure compte", a déclaré Mirkin. "Dans un domaine où nous avons consacré très peu de temps à la structure des vaccins, nous avons peut-être manqué la forêt derrière les arbres. C'est une compréhension combinée des composants et de la présentation structurelle qui conduit à un médicament efficace ou non. ."
À l'avenir, le groupe Mirkin continuera à concevoir différentes configurations de vaccins SNA pour évaluer lesquels sont les plus efficaces, a-t-il déclaré.
"Nous passons beaucoup de temps à utiliser la plateforme SNA pour identifier les structures les plus efficaces, puis à essayer de comprendre pourquoi, ce qui fonctionne et pourquoi cela fonctionne", a déclaré Mirkin. "Nous pensons qu'en faisant cela, nous serons en mesure de créer une toute nouvelle génération de médicaments basés sur ce concept de vaccinologie rationnelle."
Plus d'informations : Jasper W. Dittmar et al, Réglage de la dissociation de l'ADN à partir d'acides nucléiques sphériques pour une immunostimulation améliorée, ACS Nano (2023). DOI :10.1021/acsnano.3c04333
Informations sur le journal : ACS Nano
Fourni par l'Université Northwestern