Pour les patients atteints de certains types de cancer, la thérapie cellulaire CAR T a tout simplement changé la vie. Développée en partie par Carl June, professeur Richard W. Vague à la Perelman School of Medicine, et approuvée par la Food and Drug Administration (FDA) en 2017, la thérapie cellulaire CAR T mobilise le système immunitaire des patients pour lutter contre le lymphome et la leucémie, entre autres. d'autres cancers.
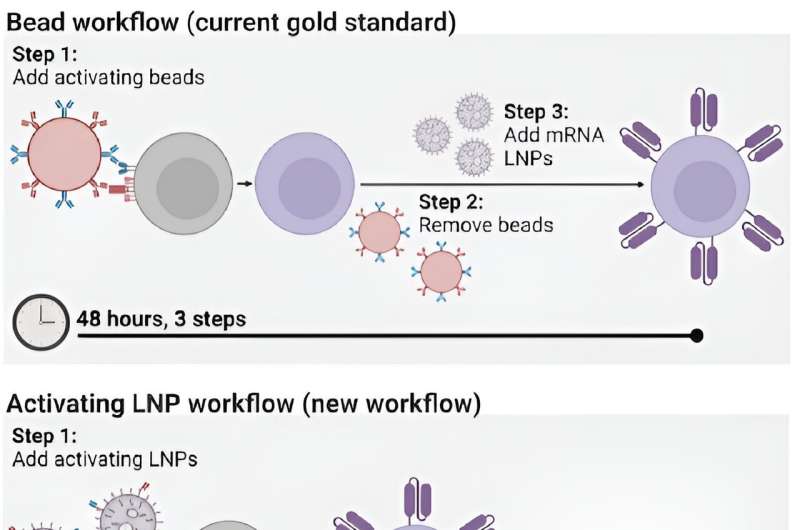
Cependant, le processus de fabrication des cellules CAR T elles-mêmes prend du temps et est coûteux, nécessitant plusieurs étapes sur plusieurs jours. Le processus consiste à extraire les cellules T des patients, puis à les activer avec de minuscules billes magnétiques, avant de donner aux cellules T des instructions génétiques pour fabriquer des récepteurs d'antigènes chimériques (CAR), les récepteurs spécialisés qui aident les cellules T à éliminer les cellules cancéreuses.
Aujourd'hui, les ingénieurs de Penn ont développé une nouvelle méthode de fabrication de cellules CAR T, qui ne prend que 24 heures et ne nécessite qu'une seule étape, grâce à l'utilisation de nanoparticules lipidiques (LNP), de puissants véhicules de distribution qui ont joué un rôle essentiel dans le développement de Moderna. et les vaccins Pfizer-BioNTech contre la COVID-19.
Dans un nouvel article publié dans Advanced Materials, Michael J. Mitchell, professeur agrégé en bio-ingénierie, décrit la création de « nanoparticules lipidiques activatrices » (aLNP), qui peuvent activer les lymphocytes T et fournir les instructions génétiques pour les CAR en une seule étape, grandement simplifiant le processus de fabrication des cellules CAR T.
"Nous voulions combiner ces deux domaines de recherche extrêmement prometteurs", explique Ann Metzloff, doctorante et chercheuse diplômée au laboratoire Mitchell et auteur principal de l'article. "Comment pourrions-nous appliquer des nanoparticules lipidiques à la thérapie cellulaire CAR T ?"
D’une certaine manière, les lymphocytes T fonctionnent comme une unité de réserve militaire :en période de santé, ils restent inactifs, mais lorsqu’ils détectent des agents pathogènes, ils se mobilisent, augmentant rapidement leur nombre avant de se tourner vers la menace. Le cancer pose un défi unique à cette stratégie de défense. Étant donné que les cellules cancéreuses appartiennent au corps, les cellules T ne traitent pas automatiquement le cancer comme dangereux, d'où la nécessité d'« activer » d'abord les cellules T et de délivrer des CAR détectant le cancer dans le cadre de la thérapie cellulaire CAR T.
Jusqu'à présent, le moyen le plus efficace d'activer les lymphocytes T consistait à les extraire du sang d'un patient, puis à mélanger ces cellules avec des billes magnétiques attachées à des anticorps spécifiques, des molécules qui provoquent une réponse immunitaire. "Les perles coûtent cher", explique Metzloff. "Ils doivent également être retirés avec un aimant avant de pouvoir administrer cliniquement les lymphocytes T. Cependant, ce faisant, vous perdez également une grande partie des lymphocytes T."
Fabriquées principalement à partir de lipides, les mêmes molécules hydrofuges qui constituent les graisses de cuisine domestiques comme le beurre et l'huile d'olive, les nanoparticules lipidiques se sont révélées extrêmement efficaces pour délivrer des charges moléculaires délicates. Leur forme en forme de capsule peut enfermer et protéger l’ARNm, qui fournit aux cellules les instructions nécessaires pour fabriquer des protéines. En raison de l'utilisation généralisée des vaccins contre la COVID-19, explique Metzloff, "l'innocuité et l'efficacité des nanoparticules lipidiques ont été démontrées chez des milliards de personnes à travers le monde."
Pour incorporer les LNP dans la production de cellules CAR T, Metzloff et Mitchell se sont demandés s'il serait possible de fixer les anticorps activateurs utilisés sur les billes magnétiques directement à la surface des LNP. Selon eux, l’utilisation des LNP de cette manière pourrait permettre d’éliminer complètement le besoin d’activer les billes dans le processus de production. "C'est nouveau", explique Metzloff, "car nous utilisons des nanoparticules lipidiques non seulement pour délivrer des CAR codant pour l'ARNm, mais également pour initier un état d'activation avantageux."
Au cours de deux années, Metzloff a soigneusement optimisé la conception des aLNP. L’un des principaux défis consistait à trouver le bon rapport entre un anticorps et un autre. "Il y avait beaucoup de choix à faire", se souvient Metzloff, "car cela n'avait jamais été fait auparavant."
En attachant les anticorps directement aux LNP, les chercheurs ont pu réduire de trois à une le nombre d’étapes impliquées dans le processus de fabrication des cellules CAR T et réduire de moitié le temps nécessaire, de 48 heures à seulement 24 heures. "Nous espérons que cela aura un effet transformateur sur le processus de fabrication des cellules CAR T", explique Mitchell. "Il faut actuellement beaucoup de temps pour les fabriquer et ils ne sont donc pas accessibles à de nombreux patients dans le monde qui en ont besoin."
Les cellules CAR T fabriquées à l'aide d'aLNP n'ont pas encore été testées chez l'homme, mais dans des modèles murins, les cellules CAR T créées à l'aide du processus décrit dans l'article ont eu un effet significatif sur la leucémie, réduisant la taille des tumeurs, démontrant ainsi la faisabilité de la technologie. .
Metzloff voit également un potentiel supplémentaire pour les aLNP. "Je pense que les aLNP pourraient être explorées plus largement en tant que plate-forme permettant de livrer d'autres cargaisons aux cellules T", dit-elle. "Nous avons démontré dans cet article une application clinique spécifique, mais les nanoparticules lipidiques peuvent être utilisées pour encapsuler de nombreuses choses différentes :des protéines, différents types d'ARNm. Les aLNP ont une large utilité potentielle pour le traitement du cancer par cellules T dans son ensemble, au-delà de cet ARNm. Application des cellules CAR T que nous avons montrée ici."
Plus d'informations : Ann E. Metzloff et al, Nanoparticules lipidiques mimétiques cellulaires présentant un antigène pour l'immunothérapie rapide du cancer par cellules CAR T à ARNm, Matériaux avancés (2024). DOI : 10.1002/adma.202313226
Informations sur le journal : Matériaux avancés
Fourni par l'Université de Pennsylvanie