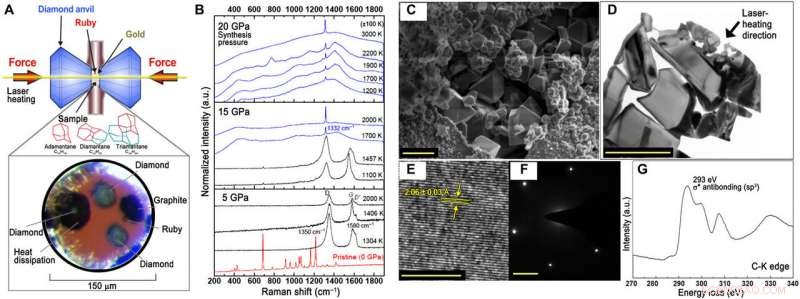
Identification et caractérisation du diamant brut de synthèse des diamantoïdes inférieurs. (A) En haut :Illustration schématique du CNA chauffé au laser et de l'échantillon. En bas :Image optique en lumière transmise d'un échantillon (à l'intérieur d'un DAC) après chauffage laser. (B) Spectres Raman représentatifs du diamantane à pression trempée à ambiante (C14H20) en fonction de l'augmentation de la température de synthèse à des pressions de 5, 15, et 20 GPa. Chaque spectre Raman est collecté à partir d'un point laser individuel avec une valeur P-T spécifique. a.u., unités arbitraires. (C) Image au microscope électronique à balayage (MEB) du diamant formé à partir de triamantane à 20 GPa et ~ 2000 K. Des grains de diamant bien formés sont intégrés dans des grains de diamant cristallins plus petits. (D) Image TEM de diamant formé à partir de triamantane orienté parallèlement à la direction du faisceau de chauffage laser. Barres d'échelle, 1 µm [(C) et (D)]. (E) Image HRTEM montrant l'espacement d du plan du diamant (111) correspondant à 2,06 ± 0,03 Å. Barre d'échelle, 5 nm. (F) Modèle de diffraction électronique correspondant à zone sélectionnée avec la barre d'échelle de 2 1/nm. (G) EELS à partir d'un grain de diamant représentant l'hybridation sp3 presque complète du diamant formé à partir de triamantane (voir fig. S3 pour SEM et EELS de flocon de graphite et fig. S4 pour le spectre de rayons X à dispersion d'énergie des motifs de diamant et XRD et SEM images de nanoparticules d'or). Crédit: Avancées scientifiques , doi:10.1126/sciadv.aay9405
Dans un nouveau rapport publié dans Avancées scientifiques , Sulgiye Park et une équipe de recherche en sciences géologiques, sciences des matériaux et de l'énergie, recherche avancée et sources de rayonnement avancées aux États-Unis et à Pékin, Chine, développé un nanomatériau à base de carbone aux propriétés exceptionnelles. Ils ont utilisé de nouveaux « diamondoïdes » comme précurseurs prometteurs pour développer des diamants haute pression et haute température. Les conditions de pression et de température les plus basses pour produire des diamants dans l'étude étaient de 12 GPa à environ 2000 K et 900 K à une pression de 20 GPa, respectivement. Les travaux ont montré une barrière de transformation considérablement réduite par rapport à la synthèse du diamant utilisant des allotropes d'hydrocarbures conventionnels. Parc et al. crédité les observations aux similitudes structurelles et la pleine sp 3 hybridation des diamantoïdes et du diamant en vrac.
La conversion diamant en diamant dans le travail s'est produite rapidement en 19 µs à 20 GPa. À l'aide de simulations de dynamique moléculaire, ils ont montré que la déshydrogénation permettait aux cages de carbone diamantoïdes restantes de se reconstruire en structures semblables à des diamants à haute pression et température ( P-T ). L'étude a cartographié avec succès les conditions P-T et le début de la conversion diamantoïde en diamant pour expliquer clairement les facteurs chimiques et physiques facilitant la synthèse du diamant.
Le diamant a de nombreuses propriétés excellentes et est l'un des matériaux les plus importants techniquement et commercialement. Depuis les premières tentatives de synthèse de diamants au 19 e siècle, les scientifiques des matériaux ont développé des efforts concertés pour concevoir des approches et des précurseurs écoénergétiques afin de générer des diamants de haute qualité. En raison de la barrière énergétique élevée pour la transformation directe des précurseurs de carbone en phase diamant, un réactif est généralement requis. Pour comprendre les mécanismes sous-jacents de la technologie de synthèse du diamant, la conception d'un nouveau système précurseur pour une synthèse de diamant facile avec une barrière énergétique et temporelle réduite est une avancée critique.

Diagrammes de synthèse P-T des diamantoïdes inférieurs. (A) Plage P-T dans laquelle le diamant se forme à partir de diamantoïdes inférieurs par rapport aux matériaux carbonés conventionnels en utilisant diverses techniques de synthèse (6). HP-HT dans le graphique représente la haute pression, synthèse de diamant à haute température à partir d'un chauffage laser à haute pression ou d'un appareil multi-enclumes. Le catalyseur HP-HT fait référence au diamant formé à l'aide de réactifs/catalyseurs. Les lignes pointillées noires représentent les régions de synthèse du diamant à partir de diamantoïdes sur la base de ce travail. (B à D) Diagrammes de synthèse P-T de la formation du diamant par rapport au graphite à partir de l'adamantane, diamantane, et triamantane. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aay9405
Les diamantoïdes sont la plus petite forme de cages en carbone à terminaison hydrogène pouvant être superposées sur le réseau de diamants. Les matériaux sont entièrement faits de sp 3 -des liaisons hybridées et comportent d'autres propriétés exceptionnelles dont la rigidité, stabilité thermique et uniformité au niveau atomique, par rapport au diamant en vrac. Alors que les études précédentes valident l'utilisation des diamantoïdes comme précurseurs prometteurs du diamant, les scientifiques cherchent à comprendre les voies mécanistiques de la transformation diamantoïde en diamant via des enquêtes systématiques sur la phase pression-température (P-T). Pour y parvenir, Parc et al. utilisé des cellules à enclume de diamant chauffées au laser (DAC) pour explorer la synthèse de diamant à partir d'une série de diamantoïdes inférieurs tels que l'adamantane, diamantane et triamantane sans utiliser de réactif supplémentaire. L'équipe de recherche a observé la transformation des diamantoïdes inférieurs en diamants à une barrière énergétique et temporelle considérablement réduite, par rapport à d'autres matériaux (hydro) carbonés à la limite P-T la plus basse. Les résultats clarifient les propriétés de base et les mécanismes régissant la conversion des hydrocarbures en diamant pour une synthèse de diamant économe en énergie et en temps.
Lors du chauffage laser des diamantoïdes à haute pression, Parc et al. observé deux phases distinctes contribuant à la formation de graphite et de diamant cubique. A 20 GPa et ~1200 à 2200 K, le diamant s'est formé comme produit dominant sans traces de graphite. Les résultats ont montré que si l'équipe ne surmontait pas la barrière cinétique de transition de phase grâce à une durée accrue de chauffage au laser ou à une température plus élevée, du carbone amorphe de type diamant hydrogéné formé à côté du diamant. Lorsque l'équipe a optimisé les conditions, la transition de phase diamantoïde à diamant s'est produite directement sans formation de graphite. Parc et al. utilisé des images de microscopie électronique à transmission (MET) pour vérifier la formation de diamant à partir de triamantane à 20 GPa et 2000 K.
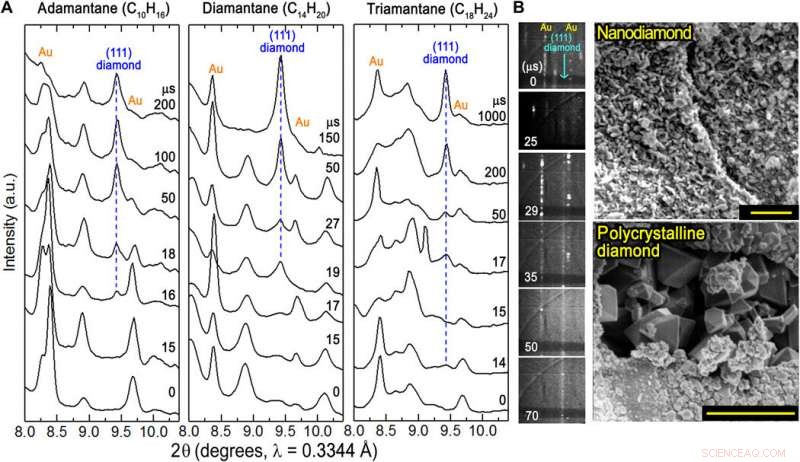
Moment du début de la formation du diamant à partir des diamantoïdes inférieurs. (A) Modèles XRD in situ de trois diamantoïdes en fonction de l'augmentation de la durée de chauffage au laser. Les pics non marqués appartiennent à l'échantillon. (B) Intégration de gâteau d'images de diffraction bidimensionnelle mettant en évidence la texture de la croissance du diamant en fonction de l'augmentation du temps de chauffage au laser. Images SEM représentatives de nanodiamant et de diamant polycristallin. Barres d'échelle, 2 µm. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aay9405
Lorsque les scientifiques ont comparé les diagrammes de synthèse P-T pour les trois diamantoïdes inférieurs avec des matériaux conventionnels tels que le graphite, ils ont observé un seuil de température beaucoup plus bas pour la formation du diamant. Des trois diamantoïdes étudiés, le triamantane nécessitait la température la plus basse pour former le diamant à une pression donnée. L'équipe a également étudié le début de la formation du diamant en contrôlant la durée du chauffage au laser pour l'adamantane, diamantane et triamantane. Ils ont effectué une analyse qualitative de la taille des particules de diamant en utilisant la diffraction de puissance des rayons X (XRD) bidimensionnelle pour montrer une taille de grain de diamant accrue avec un chauffage laser accru. La transformation a été caractérisée par une transition progressive d'une ligne de diffraction faible et large typique d'un diamant de taille nanométrique pour former des lignes étroites et tachetées à des temps plus longs caractéristiques de la croissance des grains dans le diamant polycristallin.
L'équipe a également utilisé des simulations de dynamique moléculaire ad initio (AIMD) pour étayer les résultats expérimentaux et a confirmé la voie de transformation diamantoïde en diamant. La fonction de distribution radiale de la longueur de la liaison carbone-carbone et la fonction de distribution angulaire de l'angle C-C-C ont accompagné la transformation structurelle. Les scientifiques ont noté une coordination C-C multipliée par trois et une coordination réduite par deux, loin des caractéristiques de type graphite. À une pression élevée de 40 GPa, 80 pour cent des atomes de carbone ont montré une coordination quadruple pour indiquer un changement vers une structure semblable au diamant. Toutes les observations par la suite concordaient avec la formation de diamants.
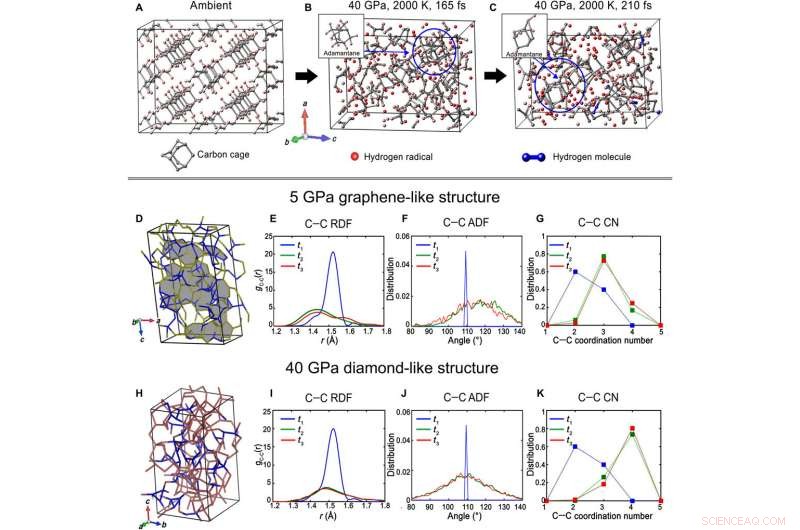
Simulations AIMD pour élucider les transformations adamantane-diamant. (A) Cellule unitaire d'adamantane vierge. (B) Déshydrogénation de l'adamantane après 165 fs à 40 GPa et 2000 K. Il y a 28 % de formation de radicaux H. L'encart représente une cage d'adamantane vierge qui n'a pas encore été rompue. (C) Déshydrogénation de l'adamantane après 215 fs à 40 GPa et 2000 K. Environ 37% de radicaux H et 5% de molécules de dihydrogène sont formés. L'encart est une cage en adamantane légèrement déformée mais toujours entièrement intacte. Les processus de déshydrogénation capturés sont tous des moments métastables avant la relaxation complète. La coupure de distance de liaison H-H était de 0,851 Å. (D) Structure complètement détendue de l'adamantane à 5 GPa et 2000 K à t3. Bien que les couches ne soient pas structurellement planes, Les caractéristiques de type graphène sont clairement observées, comme indiqué par les zones ombrées en gris. (E à G) C–C RDF, ADF, et CN de l'adamantane à 5 GPa et 2000 K. (H) Structure totalement relaxée de l'adamantane à 40 GPa et 2000 K à t3. Colorés en rose sont les atomes de carbone avec une coordination quadruple. (I à K) C–C RDF, ADF, et CN d'adamantane à 40 GPa et 2000 K. Les systèmes sans H ont été simulés pendant 9 ps. t1, t2, et t3 représente 0, 4, et 9ps, respectivement. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aay9405
Parc et al. crédité les similitudes entre les diamantoïdes inférieurs et le diamant en vrac pour clarifier la barrière énergétique réduite observée pour la formation du diamant par rapport aux allotropes de carbone conventionnels. Le calcul de l'AIMD a également montré que les diamantoïdes détenaient une « mémoire » spécifique de la structure du diamant en vrac à P-T élevé. Parmi les diamantoïdes inférieurs étudiés, l'équipe a noté que le triamantane nécessite le P-T le plus bas pour la formation de diamant. Bien que l'adamantane et le diamantane aient nécessité au moins trois cadres de carbone spécifiquement orientés pour former une structure de diamant cubique, seulement deux cadres de carbone de triamantane devaient être liés pour devenir un diamant cubique étendu. La présence d'atomes de carbone quaternaires et d'atomes de carbone tertiaires environnants dans la structure du triamantane a encore facilité ce processus.
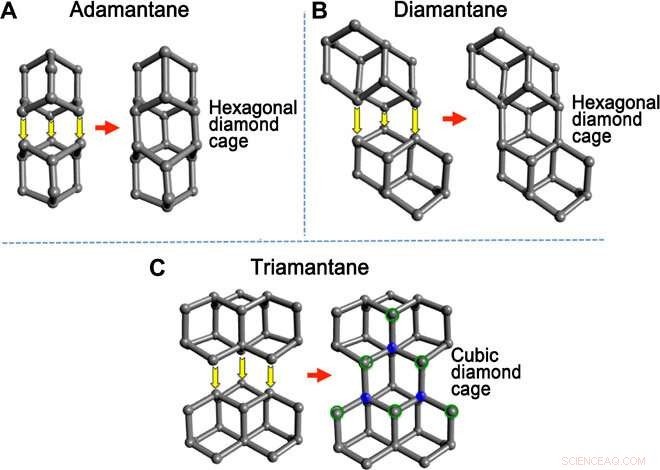
Mécanismes de formation du diamant à partir des diamantoïdes inférieurs. (A) Deux molécules d'adamantane non passivées ne peuvent fusionner que pour former une cage en diamant hexagonale. (B) Deux molécules de diamantane non passivées ne peuvent fusionner que pour former une cage de diamant hexagonale. (C) Deux molécules de triamantane non passivées fusionnent pour former une cage de diamant cubique activée par les atomes de carbone quaternaires (sphères bleues) et les atomes de carbone tertiaires environnants (entourés en vert). Crédit :Avancées scientifiques, doi:10.1126/sciadv.aay9405
De cette façon, Sulgiye Park et ses collègues ont montré que les diamantoïdes étaient des candidats prometteurs pour la synthèse du diamant. Le travail offre une voie énergétiquement supérieure pour former du diamant de l'ordre de la microseconde, sans réactifs supplémentaires qui peuvent altérer la pureté du diamant obtenu. Les résultats ont détaillé les propriétés de base et les voies mécanistiques affectant la conversion facile des hydrocarbures en diamant. Les travaux indiquent une utilisation prometteuse des diamantoïdes pour une synthèse facile du diamant et pour étudier les défauts électroluminescents dans les diamants pour une variété d'applications techniques allant de la physique quantique aux sciences biologiques. Les précurseurs économes en énergie et en temps peuvent être dopés ou fonctionnalisés avec des éléments de défaut ciblés pour que les scientifiques puissent mieux comprendre et découvrir le centre de couleur (défaut cristallin) contenant des diamants.
© 2020 Réseau Science X