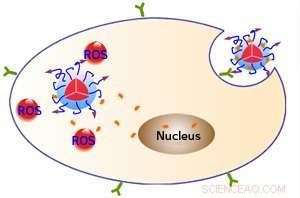
Les peptides de surface (flèches violettes) permettent aux nanoparticules fluorescentes de se lier à une protéine (verte) sur les cellules cibles et d'être absorbées dans les cellules. L'exposition à la lumière incite les nanoparticules à générer des espèces réactives de l'oxygène (ROS), tue les cellules, et libère également le médicament doxorubicine (orange), qui peut alors entrer dans le noyau cellulaire. Crédit :WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Les nanosystèmes « théranostiques »—ils combinent à la fois des fonctions thérapeutiques et diagnostiques—présentent une nouvelle opportunité passionnante pour l'administration de médicaments à des cellules spécifiques et l'identification de sites de maladie. Bin Liu de l'Institut de recherche et d'ingénierie des matériaux A*STAR, et collègues de l'Université nationale de Singapour, ont créé des nanoparticules avec deux fonctions anticancéreuses distinctes et une fonction d'imagerie, le tout stimulé à la demande par une seule source lumineuse. Les nanoparticules comprennent également la propriété de ciblage cellulaire essentielle pour le traitement et l'imagerie aux emplacements corrects.
Le système est construit autour d'un polymère à base de polyéthylène-glycol qui porte un petit composant peptidique qui lui permet de se lier préférentiellement à des types cellulaires spécifiques. Le polymère lui-même sert de photosensibilisateur qui peut être stimulé par la lumière pour libérer des espèces réactives de l'oxygène (ROS). Il contient également le médicament chimiothérapeutique doxorubicine sous forme de promédicament.
La fluorescence naturelle du polymère aide au diagnostic et au suivi de la thérapie car elle montre où les nanoparticules se sont accumulées. Les ROS générés par la stimulation lumineuse ont une activité thérapeutique 'photodynamique' directe, qui détruit les cellules ciblées. Les ROS rompent en outre le lien entre le polymère et la doxorubicine. Ainsi, les cellules cancéreuses peuvent être soumises à une attaque à deux volets de la thérapie ROS et du médicament de chimiothérapie qui est libéré en leur sein (voir image).
« Il s'agit de la première nanoplateforme qui peut offrir une thérapie photodynamique et une chimiothérapie à la demande et guidées par imagerie avec libération de médicament déclenchée via un seul interrupteur, " explique Liu, soulignant l'importance du système.
Les chercheurs ont démontré la puissance de leur plateforme en l'appliquant à un mélange de cellules cancéreuses en culture, dont certains surexprimaient une protéine de surface qui pourrait se lier au peptide de ciblage sur les nanoparticules. L'imagerie par fluorescence a indiqué que les nanoparticules étaient absorbées par les cellules cibles et que les ROS et la doxorubicine étaient libérés dans ces cellules, le tout à des niveaux significativement plus élevés que dans les cellules utilisées comme témoins. La doxorubicine qui était libérée dans le cytoplasme cellulaire pénétrait facilement dans le noyau, son site d'activité. Surtout, la thérapie combinée a eu un effet cytotoxique plus important que n'importe quelle thérapie seule.
"La lumière blanche utilisée dans ce travail ne pénètre pas suffisamment les tissus pour des applications in vivo, " Liu explique, "Mais nous essayons maintenant d'utiliser la lumière laser proche infrarouge pour améliorer la pénétration des tissus et évoluer vers une thérapie anticancéreuse à la demande." Elle suggère également qu'avec quelques modifications, le système peut convenir au diagnostic et au traitement d'autres processus pathologiques, notamment l'inflammation et l'infection par le VIH.