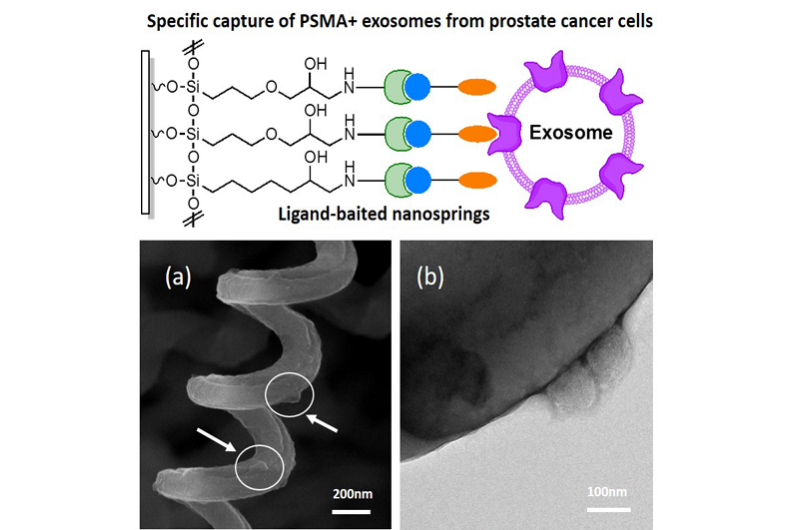
La figure a montre des exosomes capturés sur des nanoressorts à ligand-appât, les exosomes sont indiqués par les flèches. La figure b montre une image MET d'exosomes capturés après une coloration négative avec de l'acide phosphotungstique (PTA) PH =7,1. Crédit :Springer Science+Business Media New York 2017
Dans un nouvel article de Springer's Journal de la science des matériaux , des chercheurs de l'Université d'État de Washington rapportent une nouvelle approche pour la capture efficace d'exosomes dérivés de tumeurs à partir d'une lignée cellulaire de cancer de la prostate. Les exosomes sont de petites vésicules sécrétées qui jouent un rôle clé dans la communication intercellulaire et la progression du cancer.
Le développement d'une technologie de capture sélective efficace et à haut débit pour les exosomes portant le biomarqueur de l'antigène membranaire spécifique de la prostate (PSMA) est essentiel pour l'évaluation diagnostique et pronostique précoce du cancer de la prostate et la planification du traitement. Il est connu que l'enzyme-biomarqueur de tumeur de la prostate PSMA est fortement enrichi en exosomes sécrétés par les cellules cancéreuses de la prostate PSMA+. Une nouvelle nanostructure de silice biofonctionnalisée a été conçue pour capturer de manière sélective les exosomes dérivés de tumeurs grâce à l'interaction d'un ligand PSMA connu avec le PSMA sur les exosomes.
Ces travaux permettent une approche non invasive pour le diagnostic et le pronostic du cancer de la prostate. Il surmonte de nombreuses limitations des approches alternatives qui sont souvent inefficaces pour isoler les exosomes dérivés de tumeurs de ceux dérivés de tissus normaux en raison des faibles rendements de récupération et du temps requis pour le processus.
Le concept a été démontré en utilisant un seul type de cancer (c. cancer de la prostate), mais sur la base des données présentées dans cette étude, les auteurs s'attendent à ce qu'un large panel de ligands de biomarqueurs puisse être appâté sur les nanostructures de silice pour capturer sélectivement les exosomes positifs pour les biomarqueurs à partir d'un éventail de types cellulaires. D'autres avantages de l'approche utilisée dans cette étude sont la capacité d'isoler une sous-population spécifique d'exosomes en s'appuyant sur l'expression d'un marqueur de surface spécifique ainsi qu'un meilleur taux de récupération des exosomes. À l'avenir, les auteurs envisagent un dispositif d'écoulement microfluidique qui permettra une efficacité accrue de capture des exosomes et des applications cliniques.