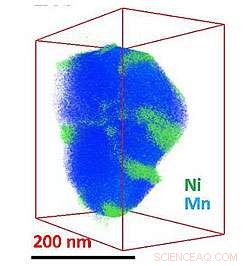
Alors que le manganèse (bleu) remplit uniformément cette nanoparticule de batterie, amas de nickel (vert) dans certaines régions, interférer avec le bon fonctionnement du matériau.
L'examen des matériaux de la batterie à l'échelle nanométrique révèle comment le nickel forme une barrière physique qui semble entraver la circulation des ions lithium dans l'électrode de la batterie, réduire la vitesse de chargement et de déchargement des matériaux, selon les recherches menées par le Pacific Northwest National Laboratory du DOE. Le nickel est un composant essentiel des composés cathodiques pour les batteries lithium-ion. Publié dans Lettres nano , la recherche suggère également un moyen d'améliorer les matériaux.
Les chercheurs, dirigé par le Dr Chongmin Wang, créé des images 3D haute résolution de matériaux d'électrode fabriqués à partir de nanoparticules d'oxyde de lithium-nickel-manganèse, cartographier les éléments individuels. Ces cartes ont montré que le nickel formait des amas à certains endroits des nanoparticules. Une vue à plus fort grossissement a montré que le nickel bloquait les canaux par lesquels les ions lithium se déplacent normalement lorsque les batteries sont chargées et déchargées.
« Nous avons été surpris de voir le nickel ségréger de manière sélective comme il l'a fait. Lorsque les ions lithium en mouvement ont frappé la couche riche en nickel ségréguée, ils rencontrent essentiellement une barrière qui semble les ralentir, " a déclaré Wang. " Le bloc se forme dans le processus de fabrication, et nous aimerions trouver un moyen de l'empêcher."
Les ions lithium sont des atomes chargés positivement qui se déplacent entre les électrodes négatives et positives lorsqu'une batterie est en charge ou en cours d'utilisation. Ils capturent ou libèrent essentiellement les électrons chargés négativement, dont le mouvement à travers un appareil tel qu'un ordinateur portable forme le courant électrique.
Dans les électrodes d'oxyde de lithium-manganèse, les atomes de manganèse et d'oxygène forment des rangées comme un champ de tiges de maïs. Dans les canaux entre les tiges, les ions lithium se dirigent vers les électrodes à chaque extrémité, le sens selon que la batterie est en cours d'utilisation ou en charge.
Les chercheurs savent depuis longtemps que l'ajout de nickel améliore la capacité d'une batterie. Mais les scientifiques n'ont pas compris pourquoi la capacité diminue après une utilisation répétée, une situation que les consommateurs vivent lorsqu'une batterie en panne conserve sa charge de moins en moins longtemps.
Découvrir, l'équipe a utilisé la microscopie électronique à l'EMSL et au Centre national de microscopie électronique pour voir comment différents atomes sont disposés dans les matériaux d'électrode produits par les chercheurs du laboratoire national d'Argonne. Les électrodes étaient à base de nanoparticules de lithium, nickel, et les oxydes de manganèse.
D'abord, l'équipe a pris des images haute résolution qui montraient clairement des rangées d'atomes séparés par des canaux remplis d'ions lithium. À la surface, ils ont vu l'accumulation de nickel aux extrémités des rangées, bloquant essentiellement le lithium d'entrer et de sortir.
Pour savoir comment la couche de surface est répartie sur et dans l'ensemble de la nanoparticule, l'équipe a utilisé une technique appelée cartographie de composition tridimensionnelle. À l'aide d'une nanoparticule d'environ 200 nanomètres, ils ont pris 50 images des éléments individuels pendant qu'ils inclinaient la nanoparticule à différents angles. L'équipe a reconstruit une carte en trois dimensions à partir des cartes élémentaires individuelles, révélant des taches de nickel sur un fond d'oxyde de lithium-manganèse.
La distribution tridimensionnelle du manganèse, les atomes d'oxygène et de lithium le long de la surface et à l'intérieur de la particule étaient relativement uniformes. Le nickel, cependant, s'est garé dans de petites zones à la surface. Intérieurement, le nickel s'est aggloméré sur les bords de régions plus petites appelées grains.
Pour explorer pourquoi le nickel s'agrège sur certaines surfaces, l'équipe a calculé avec quelle facilité le nickel et le lithium traversaient les canaux. Le nickel montait et descendait plus facilement les canaux que le lithium. Alors que le nickel réside normalement dans les cornrows d'oxyde de manganèse, parfois il se glisse dans les canaux. Et quand c'est le cas, cette analyse a montré qu'il s'écoule beaucoup plus facilement à travers les canaux jusqu'au bout du champ, où il s'accumule et forme un bloc.
Avec cette étude, soutenu par l'Initiative d'imagerie chimique du PNNL, complété, l'équipe travaille maintenant sur des expériences plus étroitement contrôlées pour déterminer si une méthode de fabrication particulière produit une meilleure électrode.