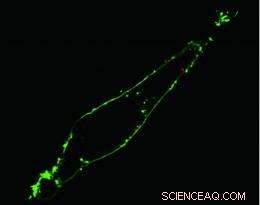
L'image confocale de fluorescence d'une seule cellule HeLa vivante montre que par nanoendoscopie, un groupe de points quantiques (point rouge) a été délivré au cytoplasme à l'intérieur de la membrane (verte) de la cellule. Avec l'aimable autorisation de Berkeley Lab
(PhysOrg.com) -- Un endoscope qui peut fournir des images optiques à haute résolution de l'intérieur d'une seule cellule vivante, ou délivrer précisément des gènes, protéines, médicaments thérapeutiques ou autre cargaison sans blesser ou endommager la cellule, a été développé par des chercheurs du Lawrence Berkeley National Laboratory (Berkeley Lab). Cette sonde optique à base de nanofils hautement polyvalente et mécaniquement robuste peut également être appliquée à la biodétection et à l'électrophysiologie unicellulaire.
Une équipe de chercheurs du Berkeley Lab et de l'Université de Californie (UC) Berkeley a attaché un guide d'ondes à nanofils d'oxyde d'étain à l'extrémité effilée d'une fibre optique pour créer un nouveau système d'endoscope. La lumière voyageant le long de la fibre optique peut être efficacement couplée dans le nanofil où elle est réémise dans l'espace libre lorsqu'elle atteint la pointe. La pointe du nanofil est extrêmement flexible en raison de sa petite taille et de son rapport d'aspect élevé, mais peut supporter des flexions et des flambages répétés, de sorte qu'il peut être utilisé plusieurs fois.
"En combinant les avantages des guides d'ondes nanofils et de l'imagerie de fluorescence par fibre optique, nous pouvons manipuler la lumière à l'échelle nanométrique à l'intérieur de cellules vivantes pour étudier les processus biologiques au sein de cellules vivantes uniques avec une résolution spatiale et temporelle élevée, " dit Peidong Yang, un chimiste à la Division des sciences des matériaux du Berkeley Lab, qui a mené cette recherche. « Nous avons montré que notre endoscope à base de nanofils peut également détecter des signaux optiques provenant de régions subcellulaires et, grâce à des mécanismes activés par la lumière, peut fournir des charges utiles dans des cellules avec une spécificité spatiale et temporelle."
Yang, qui occupe également des postes au département de chimie et au département de science et d'ingénierie des matériaux de l'Université de Californie à Berkeley, est l'auteur correspondant d'un article dans la revue Nature Nanotechnologie décrivant ce travail intitulé « Endoscopie unicellulaire à base de nanofils ». Les co-auteurs de l'article étaient Ruoxue Yan, Parc Ji-Ho, Yeonho Choi, Chul-Joon Heo, Seung-Man Yang et Luke Lee.
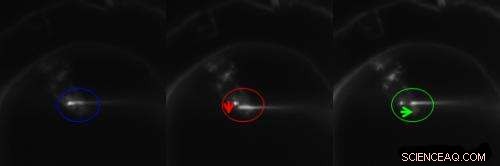
Images d'un endoscope à nanofils en contact étroit avec un amas de points quantiques dans une cellule HeLa (à gauche), et séparés verticalement du cluster de 2 mm (au milieu) et horizontalement de 6 mm (à droite). Des cercles et des flèches de couleur marquent la position du groupe et le mouvement de l'endoscope.
Malgré des avancées significatives en microscopie électronique et à sonde à balayage, la microscopie en lumière visible reste le cheval de bataille pour l'étude des cellules biologiques. Parce que les cellules sont optiquement transparentes, ils peuvent être imagés de manière non invasive avec de la lumière visible en trois dimensions. Aussi, la lumière visible permet le marquage fluorescent et la détection des constituants cellulaires, comme les protéines, acides nucléiques et lipides. Le seul inconvénient de l'imagerie en lumière visible en biologie a été la barrière de diffraction, qui empêche la lumière visible de résoudre les structures inférieures à la moitié de la longueur d'onde de la lumière incidente. Des avancées récentes en nanophotonique ont permis de surmonter cette barrière et de mettre en évidence des composants subcellulaires avec des systèmes d'imagerie optique. Cependant, ces systèmes sont complexes, cher et, assez curieusement, encombrants en taille.
"Précédemment, nous avons montré que les guides d'ondes à nanofils diélectriques sublongueurs d'onde peuvent efficacement transporter la lumière ultraviolette et visible dans l'air et les milieux fluidiques, " dit Yang. "En incorporant l'un de nos composants nanophotoniques dans un à bas prix, installation de fibre optique de paillasse, nous avons pu miniaturiser notre système endoscopique."
Pour tester leur endoscope nanofil comme source de lumière locale pour l'imagerie subcellulaire, Yang et ses co-auteurs l'ont couplé optiquement à un laser d'excitation puis ont guidé la lumière bleue à travers la membrane et à l'intérieur des cellules HeLa individuelles, la lignée cellulaire humaine immortalisée la plus couramment utilisée pour la recherche scientifique.
"La sortie optique de l'émission de l'endoscope était étroitement confinée à la pointe du nanofil et offrait ainsi un éclairage hautement directionnel et localisé, " dit Yang. " L'insertion de notre nanofil d'oxyde d'étain dans le cytoplasme de la cellule
n'a pas induit la mort cellulaire, apoptose, stress cellulaire important, ou rupture de membrane. De plus, éclairer l'environnement intracellulaire des cellules HeLa avec de la lumière bleue à l'aide de la nanosonde n'a pas endommagé les cellules car le volume d'éclairage était si petit, jusqu'à l'échelle du picolitre."
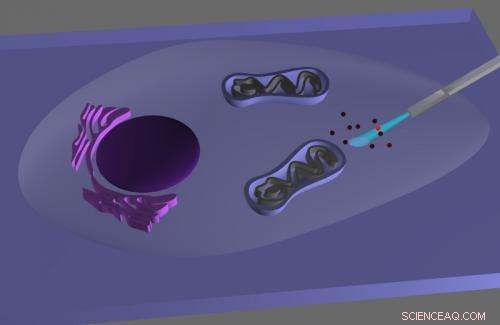
Ce schéma illustre l'imagerie subcellulaire de points quantiques dans une cellule vivante à l'aide d'un endoscope à nanofil. Crédit :(Avec l'aimable autorisation de Berkeley Lab)
Après avoir démontré la biocompatibilité de leur endoscope nanofil, Yang et ses co-auteurs ont ensuite testé ses capacités à livrer des charges utiles à des sites spécifiques à l'intérieur d'une cellule. Alors que des systèmes d'administration à cellule unique à base de nanotubes de carbone et de nitrure de bore ont été signalés, ces systèmes souffrent de délais de livraison allant de 20 à 30 minutes, plus un manque de contrôle temporel sur le processus de livraison. Pour surmonter ces limites, Yang et ses co-auteurs ont attaché des points quantiques à la pointe du nanofil d'oxyde d'étain de leur endoscope à l'aide de lieurs photo-activés qui peuvent être clivés par un rayonnement ultraviolet de faible puissance. En une minute, leur endoscope nanofil fonctionnalisé a pu libérer sa cargaison de points quantiques dans les sites intracellulaires ciblés.
"Le balayage par microscopie confocale de la cellule a confirmé que les points quantiques ont été délivrés avec succès au-delà de la membrane marquée par fluorescence et dans le cytoplasme, " dit Yang. " La photoactivation pour libérer les points n'a eu aucun effet significatif sur la viabilité des cellules. "
La lumière laser bleue hautement directionnelle a été utilisée pour exciter l'un des deux amas de points quantiques situés à seulement deux micromètres l'un de l'autre. Avec la zone d'éclairage étroite et la petite séparation entre la source lumineuse et les points, une faible fluorescence de fond et un contraste d'imagerie élevé ont été assurés.
"À l'avenir, en plus de l'imagerie optique et de la livraison de fret, on pourrait aussi utiliser cet endoscope nanofil pour stimuler électriquement ou optiquement une cellule vivante, " dit Yang.
Les nanofils utilisés dans ces expériences ont été développés à l'origine pour étudier de nouvelles propriétés électroniques et optiques dépendantes de la taille pour des applications énergétiques.