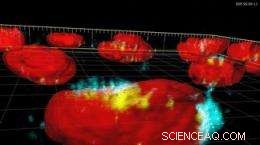
Image :Particules d'oxyde de fer superparamagnétique (bleu et jaune) absorbées dans le noyau d'une cellule (noyau en rouge).
(PhysOrg.com) -- Détecter les cellules cancéreuses et les détruire, injecter des médicaments avec une extrême précision dans les cellules malades du corps humain - ce ne sont que deux exemples de ce que les scientifiques de l'EPFL tentent d'accomplir en utilisant des nanoparticules d'oxyde de fer développées dans le Laboratoire de technologie des poudres (LTP) de l'École.
Seulement 5 à 10 nanomètres de diamètre (un nanomètre correspond à un millionième de millimètre), les nanoparticules d'oxyde de fer superparamagnétiques étudiées par l'équipe LTP du professeur Heinrich Hofmann sont prometteuses, car ils présentent des propriétés magnétiques lorsqu'ils sont exposés à un champ magnétique externe. Cette caractéristique est importante pour certaines applications médicales, comme le diagnostic de maladies telles que l'arthrite, localiser les tumeurs, et détruire les cellules cancéreuses chez les patients.
Détecter le cancer
Les scientifiques de l'EPFL étudient trois applications principales :le diagnostic, traitement et élimination des cellules malignes. « En pratique, les particules d'oxyde de fer sont déjà utilisées comme agents de contraste en imagerie par résonance magnétique (IRM) dans les cas de tumeurs hépatiques, », note Hofmann. « Nous étudions comment appliquer cette méthode à toutes sortes de tumeurs et si possible à d'autres maladies, comme l'arthrite. Ce dernier est l'objectif d'un grand projet de l'UE FP-7 (Nanodiara). une sorte d'identifiant cellulaire. Le revêtement sur les nanoparticules est adapté en conséquence (via des anticorps, par exemple), de sorte qu'une fois injectés par voie intraveineuse, ils ne s'attacheront qu'aux récepteurs des cellules cancéreuses. Et parce qu'une particule d'oxyde de fer modifie le contraste des tissus lorsqu'elle est soumise à un champ magnétique, il est ainsi possible de localiser avec précision l'emplacement exact des cellules cancéreuses à l'aide de l'IRM. « Jusqu'à présent, cette technique n'a été validée que pour les tumeurs du foie, car pour chaque type de cancer, des éléments surfaciques doivent être ajoutés, qui modifient le comportement des particules. Or il est assez difficile de comprendre le comportement des nanoparticules dans un fluide complexe, comme le sang, », explique-t-il.
Traitement ciblé
Un aspect de la recherche se concentre sur une nouvelle application passionnante :l'administration ciblée de médicaments à des cellules spécifiques. « Il est possible que des nanoparticules d'oxyde de fer pénètrent directement dans les organites d'une cellule. Cette propriété ouvre la possibilité de délivrer un médicament jusqu'à l'intérieur d'une cellule, », explique Hofmann. Cela présente des avantages évidents par rapport aux méthodes d'administration de médicaments existantes. Le professeur de radiologie de l'Université de Genève Jean-Paul Vallée déclare :
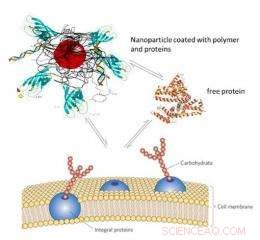
« Dans les traitements médicamenteux systémiques actuels, le médicament n'est pas délivré sélectivement dans le corps, mais largement absorbé. Avec cette nouvelle méthode, nous serions en mesure d'éviter certains effets secondaires et de délivrer le médicament uniquement aux cellules qui doivent être traitées.
Détruire les tumeurs par la chaleur
En plus de détecter des cellules spécifiques et d'y administrer des médicaments directement, les particules d'oxyde de fer ont également la capacité de détruire les tumeurs osseuses par hyperthermie. Dans le cancer des os, les métastases se développent souvent dans la colonne vertébrale. Un traitement actuel consiste à injecter une substance semblable à du ciment dans les corps des vertèbres. Une fois que cette substance à base de polymère est dans le corps, il se solidifie et stabilise ainsi les vertèbres. Selon les chercheurs, si des particules superparamagnétiques ont été ajoutées au ciment avant l'injection, il serait possible de transférer de l'énergie en appliquant un champ magnétique alternatif externe, chauffant ainsi l'implant jusqu'à 46°C. Cette procédure détruirait sélectivement les cellules cancéreuses à proximité, car ils sont moins tolérants à la chaleur que les tissus normaux. « Cette méthode serait moins agressive que les lasers, qui brûlent également des cellules saines et laissent des déchets derrière, », ajoute Hofmann.
Pour le moment, ces trois applications sont au stade pré-clinique, et font partie de plusieurs projets impliquant de nombreux partenaires, comme les Hôpitaux Universitaires de Lausanne (CHUV), l'Université de Genève et le Centre suisse d'électronique et de microtechnique (CSEM), ainsi que des entreprises comme ANTIA ou MERCK-Serono.