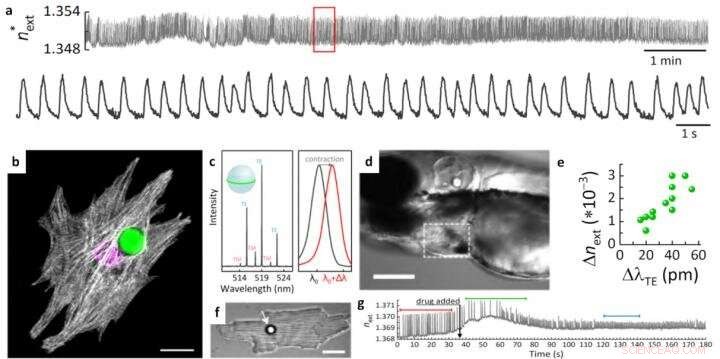
une, Surveillance unicellulaire avec un microlaser intracellulaire. b, Disposition 3D des myofibrilles autour des microbilles dans les cardiomyocytes (CM) néonatals. Noyau cellulaire (magenta) et microlaser (vert). c, Spectre WGM d'un microlaser et son déplacement. ré, Microlaser attaché à l'atrium d'un cœur de poisson zèbre. e, Changement d'indice de réfraction entre la phase de repos, diastole, et pic de contraction, systole, pour 12 cellules individuelles. F, Microlaser extracellulaire sur un CM adulte. Barre d'échelle 30 m. g, Trace d'un CM néonatal battant spontanément lors de l'administration de 500 nM de nifédipine. Adapté avec la permission de Schubert M. et al. Surveillance de la contractilité du tissu cardiaque avec résolution cellulaire à l'aide de microlasers biointégrés. Photonique Nature 14, 452-458, (2020). Crédit :Nikita Toropov, Gema Cabello, Mariana P. Serrano, Rithvik R. Gutha, Matias Rafti, Frank Vollmer
Les microrésonateurs en mode Whispering-gallery-mode (WGM) ouvrent de nombreuses nouvelles directions de recherche qui permettent la détection de protéines, enzymes et ADN, jusqu'à des molécules simples. Une nouvelle classe de capteurs utilise des microrésonateurs actifs pour étendre considérablement les fonctionnalités et la gamme des applications des capteurs WGM, notamment pour les dosages biologiques et chimiques. Nous passons en revue les avancées les plus récentes des microlasers WGM pour la biodétection et donnons un aperçu des nouvelles directions de recherche passionnantes et des applications émergentes des capteurs WGM.
Les capteurs optiques sans étiquette basés sur des microrésonateurs optiques en mode galerie de chuchotement (WGM) présentent une sensibilité extraordinaire pour la détection physique, chimique, et entités biologiques, même jusqu'à des molécules simples. Cette avancée dans la détection optique sans marquage est rendue possible par l'application du microrésonateur optique, c'est-à-dire des microsphères de verre de 100 um, comme cavité optique pour améliorer le signal de détection. Semblable à un micromiroir sphérique, la cavité WGM réfléchit la lumière par réflexion interne presque totale et crée ainsi de multiples passes de cavité qui améliorent la détection optique des molécules d'analyte interagissant avec le champ évanescent.
Contrairement aux microrésonateurs WGM « froids », les microlasers actifs émergents WGM ont le potentiel d'élargir considérablement le nombre d'applications possibles de cette classe de capteurs dans la détection biologique et chimique, et en particulier dans la détection in vivo. Les microlasers WGM peuvent détecter à l'intérieur des tissus, organismes et cellules individuelles, et ils peuvent être utilisés pour améliorer les limites de détection de molécules uniques déjà impressionnantes des capteurs WGM optoplasmoniques à cavité «froide».
Ici, nous passons en revue les avancées les plus récentes des microlasers WGM en biodétection. Contrairement aux capteurs WGM à cavité "froide", les microrésonateurs WGM actifs utilisent des supports de gain tels que des molécules de colorant et des points quantiques pour compenser la perte optique et pour obtenir l'effet laser des modes WGM. Semblable à d'autres lasers conventionnels, l'effet laser est observé à partir de raies spectrales étroites dans les spectres d'émission WGM.
Nous passons en revue les principaux éléments constitutifs des microlasers WGM, mécanismes de détection récemment démontrés, les méthodes d'intégration des milieux à gain dans les capteurs WGM, et les perspectives pour les capteurs WGM actifs de devenir une technologie utile dans les applications du monde réel. Nous passons en revue les expériences de détection par microlaser WGM au niveau moléculaire où les spectres laser sont analysés pour étudier la liaison des molécules, à la détection au niveau cellulaire où les microlasers sont intégrés ou intégrés à des cellules individuelles pour permettre de nouvelles applications de détection in vivo et de suivi de cellule unique (voir figure).