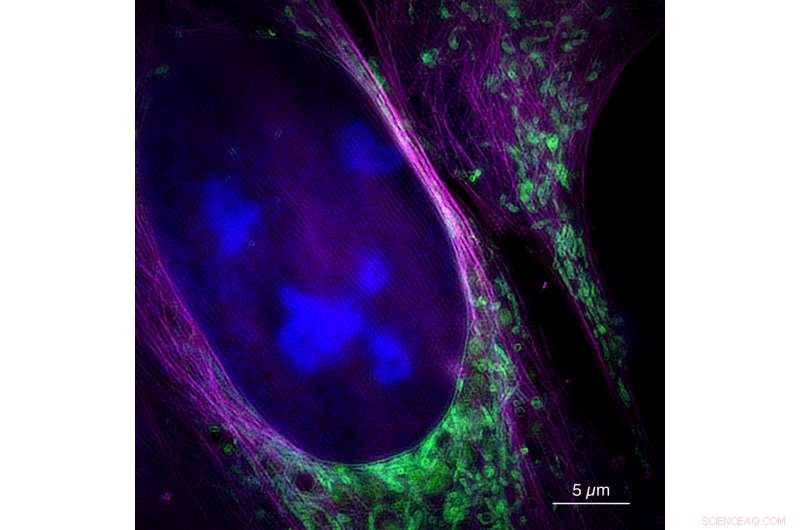
Cette image prise par le nouveau microscope montre une cellule cancéreuse osseuse vivante avec un noyau (bleu), mitochondries (vert) et cytosquelette (magenta). Crédit :Université de Bielefeld/W. Hübner
Ils peuvent rendre visibles de minuscules structures cellulaires :les microscopes optiques de pointe offrent des résolutions de quelques dixièmes de nanomètres, c'est-à-dire un millionième de millimètre. Jusqu'à maintenant, les microscopes à super-résolution étaient beaucoup plus lents que les méthodes conventionnelles, car des données d'image plus nombreuses ou plus fines devaient être enregistrées. En collaboration avec des partenaires d'Iéna, des chercheurs de l'université "Bielefeld" ont maintenant développé le processus SR-SIM à super-résolution. Les universitaires montrent que la SR-SIM est également possible en temps réel et à une cadence d'imagerie très élevée, et donc adaptée à l'observation des mouvements de très petites particules cellulaires, par exemple. Leurs conclusions ont été publiées aujourd'hui (20 septembre) dans la revue Communication Nature .
« C'est ce qui rend ce type de microscopie vraiment utile pour des applications en biologie ou en médecine. Le problème jusqu'à présent est que les microscopes offrant une résolution suffisamment élevée ne peuvent pas afficher les informations à la vitesse correspondante, " dit le professeur Dr Thomas Huser, qui dirige le groupe de travail sur la physique biomoléculaire à l'Université de Bielefeld. Le projet SR-SIM est financé par la Fondation allemande pour la recherche (DFG) et l'Union européenne à travers les actions Marie Skłodowska-Curie.
SR-SIM signifie "microscopie d'illumination structurée à super-résolution" et est une procédure de microscopie à fluorescence. Les objets sont irradiés avec de la lumière laser. Cette lumière excite des molécules fluorescentes spéciales dans l'échantillon afin qu'elles réémettent de la lumière à une longueur d'onde différente. L'image microscopique montre alors la lumière réémise. "Contrairement aux autres méthodes conventionnelles de microscopie à fluorescence, SR-SIM n'éclaire pas les échantillons de manière uniforme, mais avec une amende, motif en forme de grille. Cette technologie spéciale permet une résolution beaucoup plus élevée, " dit Huser.
La procédure se compose de deux étapes :la lumière réémise par l'échantillon est d'abord enregistrée dans plusieurs images individuelles. L'image finie est ensuite reconstruite sur ordinateur à partir de ces données brutes. "La deuxième étape, en particulier, a coûté beaucoup de temps jusqu'à présent, " dit Andreas Markwirth, également membre du groupe de travail sur la physique biomoléculaire de l'Université de Bielefeld et auteur principal de l'étude. Les chercheurs de Bielefeld ont donc collaboré avec le professeur Dr Rainer Heintzmann de l'Institut Leibniz pour les technologies photoniques et de l'Université Friedrich Schiller d'Iéna pour accélérer le processus. Le microscope est maintenant conçu pour générer les données brutes plus rapidement. En outre, la reconstruction d'image prend considérablement moins de temps grâce à l'utilisation du traitement informatique parallèle sur les cartes graphiques modernes.
Pour leur étude, les chercheurs ont testé la nouvelle méthode sur des cellules biologiques et enregistré les mouvements des mitochondries, organites cellulaires d'environ un micromètre. « Nous avons pu produire environ 60 images par seconde, une fréquence d'images supérieure à celle des films de cinéma. Le temps entre la mesure et l'image est inférieur à 250 millisecondes, la technologie permet donc l'enregistrement en temps réel, " dit Markwirth.
Jusqu'à maintenant, les méthodes de super-résolution ont souvent été combinées avec des méthodes conventionnelles :un microscope rapide conventionnel est utilisé pour rechercher d'abord des structures. Ces structures peuvent ensuite être examinées en détail à l'aide d'un microscope à super-résolution. "Toutefois, certaines structures sont si petites qu'elles ne peuvent pas être trouvées avec des microscopes conventionnels, par exemple des pores spécifiques dans les cellules du foie. Notre méthode est à la fois haute résolution et rapide, qui permet aux biologistes d'explorer de telles structures, " dit Huser. Une autre application pour le nouveau microscope est l'étude des particules virales sur leur chemin à travers la cellule. " Cela nous permet de comprendre exactement ce qui se passe pendant les processus d'infection, " dit Huser. Il s'attend à ce que le microscope soit utilisé pour de telles études à l'Université de Bielefeld au cours de l'année à venir.
Les microscopes à super-résolution n'existent que depuis environ 20 ans. En 1873, Ernst Abbe avait découvert que la résolution d'un système optique pour la lumière visible est limitée à environ 250 nanomètres. Dans les années récentes, cependant, plusieurs méthodes optiques ont été développées pour briser ce qui est devenu la barrière de diffraction d'Abbe. En 2014, William E. Moerner et Eric Betzig, tous deux des États-Unis, ainsi que Stefan Hell d'Allemagne ont reçu le prix Nobel de chimie pour avoir développé une super-résolution dans la gamme d'environ 20 à 30 nanomètres.